
科目: 来源: 题型:
【题目】如表列出了①~⑥六种元素在元素周期表中的位置.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ |
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是 (填写元素符号);
(2)元素①③⑥的氢化物的分子式分别是 ; ; .
(3)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】日常生活中的手电筒干电池通常是锌锰电池,其构造示意图如右。据图回答:

(1)作正极的是__________。
(2)负极的电极反应是_____________________________
(3)许多国家对废电池进行回收,其主要原因是_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 如图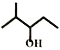 所示的有机物的名称为:2-甲基戊醇
所示的有机物的名称为:2-甲基戊醇
B. 乙烯能使酸性高锰酸钾溶液褪色,聚乙烯也能使酸性高锰酸钾褪色
C. 蛋白质能发生水解反应,水解生成的氨基酸能和酸反应,也能和碱反应
D. 分子式为C4H9Cl的氯代烃有4种,C4H10O的醇有4种,C4H8O的酸也有4种
查看答案和解析>>
科目: 来源: 题型:
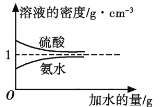
【题目】已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
溶质的物质的量浓度/mol·L1 | 溶液的密度/g·cm3 | |
硫酸 | c1 | ρ1 |
氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为 (不写单位,用含c1、 ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为 mol·L1。
(3)将物质的量浓度分别为c2 mol·L1和![]() c2 mol·L1的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”,下同)ρ2 g·cm3,所得溶液的物质的量浓度
c2 mol·L1的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”,下同)ρ2 g·cm3,所得溶液的物质的量浓度 ![]() c2 mol·L1(设混合后溶液的体积变化忽略不计)。
c2 mol·L1(设混合后溶液的体积变化忽略不计)。
查看答案和解析>>
科目: 来源: 题型:
【题目】
(1)室温时纯水中c(H+)=c(OH-),向纯水中加入少量下列固体物质:
A.NaOH B.Na2SO4 C.NH4Cl
试回答如下问题:
I.溶液中H+、OH-浓度变化情况(填“变大”“减小”或“不变”)
II. c(H+)与c(OH-)大小比较(填“>”“<”或“=”)
III.溶液的酸碱性(填“酸性”“碱性”或“中性”)
请按上述要求补完整表中相关内容
A.NaOH | a Na2SO4 | C.NH4C1 | |
c(H+) | 减少 | ①________ | 增大 |
c(OH-) | ②_______ | 不变 | ③_____ |
c(H+)与c(OH-)的大小比较 | ④_______ | = | > |
溶液的酸碱性 | 碱性 | ⑤_______ | 酸性 |
(2)己知25℃合成氨反应中,1 mol N2完全转化为NH3时释放的能量为92.4 kJ。X现将1 molN2和3 mol H2混合置于2 L密闭容器中,反应进行到2 s末测得NH3为0.4mol。试回答:
①该反应的热化学方方程式为 ________________________。
②该反应达到平衡后,升髙温度平衡向_____(填“正”或“逆”)反应方向移动;增大压强平衡向_____ (填“正”或“逆”)反应方向移动;加入催化剂平衡________(填“能”或“不能”)移动。
③前2 s内v(H2)为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】
(1)下列六种生活中常见物质:
①食盐 ②食用油 ③靑霉素 ④鸡蛋 ⑤西红柿 ⑥塑料
按要求用物质序号填空:
作调味剂的是___________;作抗生素的是___________;富含蛋白质的是___________;富含维生素的是___________;富含油脂的是___________;属于合成材料的是___________。
(2)一个体重50 kg的健康人,体内约含有2 g铁,这2 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+, 有利于人体吸收。
i.在人体中进行Fe2+ ![]() Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
ii.服用维生索C,可使食物中的Fe3+还原成Fe2+这句话指出,维生素C在这一反应中作 ____________(填“氧化剂”或“还原剂”)
iii.市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸 (HC1)的作用下转化成亚铁盐。此反应的离子方程式为___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现将AlCl3、MgCl2、MgSO4、Al2(SO4)3四种物质溶于水,形成的混合溶液中c(Al3+)=0.1mol·L-1、c(Mg2+)=0.25mol·L-1、c(Cl-)=0.2mol·L-1,则该溶液中c(SO42-)为
A. 0.15mol·L-1
B. 0.20mol·L-1
C. 0.25mol·L-1
D. 0.30mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用地下水稀释浓硫酸,将浓硫酸沿玻璃棒注入盛地下水的烧杯中时,发现烧杯中溶液变浑浊,由此推测地下水中可能含有的离子是
A.Na+ B.Ba2+ C.Mg2+ D.K+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应属于氧化还原反应的是 ( )
A. H2SO4+2NaOH=Na2SO4+2H2O B. CuO+H2![]() Cu+ H2O
Cu+ H2O
C. NH3+HCl=NH4Cl D. 2NaHCO3![]() Na2CO3+ H2O +CO2↑
Na2CO3+ H2O +CO2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,下列说法正确的是( )

A. 若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
B. 若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
C. 若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
D. 若四种元素中只有一种为金属,则Z与Y两者的最高价氧化物对应的水化物能反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com