
科目: 来源: 题型:
【题目】下列物质的分类正确的是( )
选项 | 碱 | 酸 | 盐 | 酸性氧化物 |
A | 苏打 | 硫酸 | 小苏打 | 二氧化硫 |
B | 苛性钠 | 碳酸 | 胆矾 | 一氧化氮 |
C | 烧碱 | 硝酸 | 石灰石 | 二氧化硅 |
D | 纯碱 | 醋酸 | 碘化钾 | 一氧化碳 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】不能作为判断元素的非金属性强弱依据的是( )
A. 元素的最高价氧化物对应水化物的酸性强弱
B. 元素的单质跟氢气反应生成气态氢化物的难易程度
C. 非金属元素对应的气态氢化物的稳定性
D. 非金属元素单质的熔点和沸点的高低
查看答案和解析>>
科目: 来源: 题型:
【题目】关于电解NaCl水溶液,下列叙述正确的是
A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
C.若在阴极附近的溶液中滴入酚酞溶液,溶液呈无色
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应既属于非氧化还原反应,又属于吸热反应的是( )
A.高温下炭与CO2的反应
B.Ba(OH)28H2O与NH4Cl的反应
C.生石灰溶于水的反应
D.盐酸与烧碱溶液的中和反应
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用CO2和H2催化氢化可以制取甲烷。
(1)已知 ①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH= -890 kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH= -572 kJ·mol-1
③H2O(l)=H2O(g) ΔH= +44 kJ·mol-1
CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) ΔH=a kJ·mol-1
CH4(g)+2H2O(g) ΔH=a kJ·mol-1
据此,a=_________;升高温度,该反应的v(逆)_____(填“增大”或“减小”)。
(2)在一定压强、不同温度下,两种催化剂分别催化CO2加氢甲烷化反应2h的结果如图1所示(一定温度下仅改变催化剂,其他条件不变):a、b-催化剂I; c、d-催化剂II。甲烷化选择性:指含碳产物中甲烷的物质的量分数。请据图1分析:
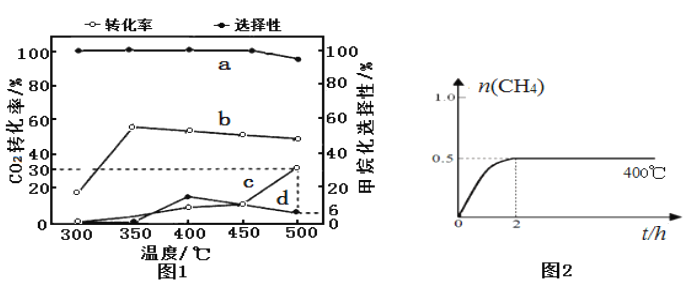
①催化剂I实验,400 ℃~450℃时CO2转化率下降的原因可能为___________(写1条)。
②催化剂II实验,检测密闭容器中产物发现,温度升高甲烷的选择性下降是发生了:CO2(g)+ H2(g)![]() CO(g)+H2O(g) ΔH>0。若保持温度不变,提高甲烷化选择性可以采取的措施:______________(写2条)。
CO(g)+H2O(g) ΔH>0。若保持温度不变,提高甲烷化选择性可以采取的措施:______________(写2条)。
(3)下列与甲烷化反应有关的描述中,正确的是______:
A.单位时间内断裂1molC=O键的同时断裂1molC-H,说明该反应已达平衡
B.照上述反应使用催化剂,其Ⅰ的活化能比Ⅱ的活化能大
C.在绝热的密闭容器中进行时,当容器中温度不变时说明达到平衡
D.催化剂Ⅰ下,300-450℃内,选择性保持不变的主要原因是其它副反应的速率很慢
(4)催化剂I实验, 400℃时,向2L固定体积的密闭容器中通入1mol CO2和4mol H2,CH4物质的量随时间的变化趋势如图2时所示,则2h内H2平均反应速率为____________;平衡常数K=____________。若其他条件不变,反应在恒压条件下进行,请在图2中画出反应体系中n(CH4)随时间t变化的趋势图____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)用硫酸分解磷尾矿[主要成份为Ca5(PO4)3F]可制得中强酸磷酸H3PO4。请回答:
①Na2HPO4溶液呈碱性,则在该溶液中c(H2PO4-)_____c(PO43-)(填“>”、“<”、“=”),
向Na2HPO4溶液中加入足量的CaCl2溶液,溶液显酸性,溶液显酸性的原因是(从电离平衡移动角度分析):_____________________________。
②已知:25℃时,H3PO4的电离平衡常数:K1=7.52×10-3;K2=6.23×10-8;K3=6.23×10-13则:H3PO4(aq)+OH-(aq)![]() H2PO4-(aq)+H2O (l)的平衡常数K=______。
H2PO4-(aq)+H2O (l)的平衡常数K=______。
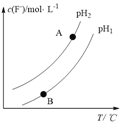
③Ca5(PO4)3F(s) +OH-(aq)![]() Ca5(PO4)3(OH) (s)+F-,该温度下,溶液中c(F-)随溶液的pH和温度(T)的变化曲线如右图所示。则:pH1___pH2(填“>”、“<”、“=”);A、B两点的溶液中F-的速率v(A)____v(B)(填“>”、 “<”、“=”)。
Ca5(PO4)3(OH) (s)+F-,该温度下,溶液中c(F-)随溶液的pH和温度(T)的变化曲线如右图所示。则:pH1___pH2(填“>”、“<”、“=”);A、B两点的溶液中F-的速率v(A)____v(B)(填“>”、 “<”、“=”)。
(2)处理含镍酸性废水可用电解法实现铁上镀镍,其装置如右图所示。

①电流方向是_____(填:a.碳棒→铁棒;b.铁棒→碳棒);
②中间隔室的可以得到的物质X是_______(填化学式);
③阳极的电极反应式为_______________;电解总反应的离子方程式为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】500 mL KNO3和Cu(NO3)2的混合溶液中c(![]() )= 6.0 mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为
)= 6.0 mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为
500 mL,下列说法正确的是
A.原混合溶液中c(K+)为2 mol/L B.上述电解过程中共转移2 mol电子
C.电解得到的Cu的物质的量为0.5 mol D.电解后溶液中c(H+)为2 mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】TiO2在光照射下可使水分解:2H2O![]() 2H2↑+O2↑,该过程类似植物的光合作用。图中是光照射下TiO2分解水的装置示意图。下列叙述正确的是
2H2↑+O2↑,该过程类似植物的光合作用。图中是光照射下TiO2分解水的装置示意图。下列叙述正确的是
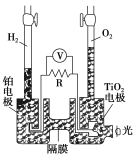
A.该装置可以将光能转化为电能,同时也能将其转化为化学能
B.TiO2电极上发生的反应为:2H++2e-===H2↑
C.该装置工作时,电流由TiO2电极经R流向铂电极
D.该装置工作时,TiO2电极附近溶液的pH变大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com