
科目: 来源: 题型:
【题目】周期表前四周期的元素a、b、c、d、e,原子序数依次增大.A的核外电子总数与其电子层数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同主族,e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
(1)b、c、d中第一电离能最大的是(填元素符号),e的价层电子轨道示意图为 .
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为;分子中既含有极性共价键,又含有非极性共价键的化合物是(填化学式,写两种).
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是;酸根呈三角锥结构的酸是 . (填化学式)
(4)c和e形成的一种离子化合物的晶体结构如图1,则e离子的电荷为 .
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,阳离子呈轴向狭长的八面体结构(如图2所示).该化合物中阴离子为 , 阳离子中存在的化学键类型有;该化合物加热时首先失去的组分是 , 判断理由是 . 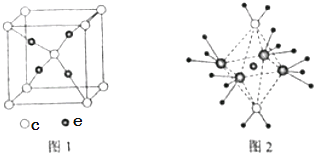
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物Ⅰ(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基.Ⅰ可以用E和H在一定条件下合成: 
已知以下信息:
A的核磁共振氢谱表明其只有一种化学环境的氢;R﹣CH═CH2 ![]() R﹣CH2CH2OH
R﹣CH2CH2OH
化合物F苯环上的一氯代物只有两种;
通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基.
回答下列问题:
(1)A的化学名称为 .
(2)D的结构简式为 .
(3)E的分子式为 .
(4)F生成G的化学方程式为 , 该反应类型为 .
(5)I的结构简式为 .
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基,②既能发生银镜反应,又能和饱和NaHCO3溶液反应放出CO2 , 共有种(不考虑立体异构).J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组中,两种气体的分子数一定相等的是( )
A.温度相同、体积相同的O2和N2
B.体积相等、密度不等的CO和C2H4
C.质量相等、密度不等的N2和C2H4
D.压强相同、体积相同的N2和O2
查看答案和解析>>
科目: 来源: 题型:
【题目】从海水中提取镁涉及到的化学反应有:①CaO+H2O=Ca(OH)2、②Mg2++2OH﹣=Mg(OH)2↓、③Mg(OH)2+2HCl=MgCl2+2H2O、④MgCl2 ![]() Mg+Cl2↑没有涉及到的反应类型是( )
Mg+Cl2↑没有涉及到的反应类型是( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.CO2通入足量氢氧化钠溶液中:CO2+2OH﹣=CO ![]() +H2O
+H2O
B.用小苏打治疗胃酸过多: ![]() +OH﹣=CO2↑+H2O
+OH﹣=CO2↑+H2O
C.将Cl2通入水中:Cl2+H2O=Cl﹣+2H++ClO﹣
D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+
查看答案和解析>>
科目: 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下: 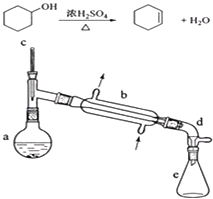
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置a的名称是 .
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的(填“上口倒出”或“下口放出”).
(4)分离提纯过程中加入无水氯化钙的目的是 .
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有(填正确答案标号).
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验中最容易产生的副产物的结构简式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】SO2直接排放会对环境造成危害.SO2的尾气处理通常有以下几种方法: 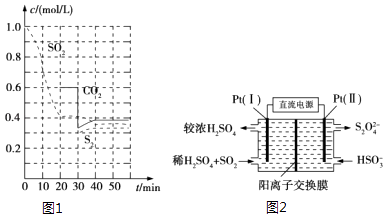
(1)活性炭还原法 反应原理:恒温恒容时2C(s)+2SO2(g)S2(g)+2CO2(g).
反应进行到不同时间测得各物质的浓度如图1:
①0~20min反应速率表示为v(SO2)=;
②30min时,改变某一条件平衡发生移动,则改变的条件最有可能是;
③能说明上述反应达到平衡状态的是 .
a.SO2 的消耗速率与CO2 的生成速率相同 b.混合气体的密度不变
c.S2的浓度不变 d.SO2 与S2的物质的量之比为2:1
(2)亚硫酸钠吸收法 ①Na2SO3溶液吸收SO2的离子方程式为;
②常温下,当吸收至NaHSO3时,吸收液中相关离子浓度关系一定正确的是(填序号).
a.c(Na+)+c(H+)>c(SO32﹣)+c(HSO3﹣)+c(OH﹣)
b.c(Na+)=c(SO32﹣)+c(HSO3﹣)+c(H2SO3)
c.c(Na+)>c(HSO3﹣)>c(H+)>c(SO32﹣)
d.水电离出c(H+)=1×10﹣8 mol/L
(3)电化学处理法 ①如图2所示,Pt(Ⅰ)电极的电极反应式为;
②当电路中转移0.02mol e﹣时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加mol离子.
查看答案和解析>>
科目: 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下: 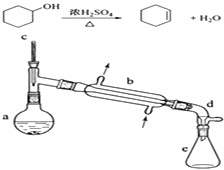
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置a的名称是 .
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的(填“上口倒出”或“下口放出”).
(4)分离提纯过程中加入无水氯化钙的目的是 .
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有 ABE (填正确答案标号).
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验所得到的环己烯产率是 . (保留两位有效数字)
(注:产率= ![]() ×100%)
×100%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com