
科目: 来源: 题型:
【题目】已知25 ℃时有关弱酸的电离平衡常数如下表:
弱酸的化学式 | CH3COOH | HCN | H2CO3 |
电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
则下列有关说法正确的是( )
A. 各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
B. a mol·L-1HCN溶液与b mol·L-1NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b
C. 冰醋酸中逐滴加水,则溶液的导电性和pH均先增大后减小
D. NaHCO3和Na2CO3混合溶液中,一定有2c(Na+)=3〔c(H2CO3)+c(HCO![]() )+c(CO
)+c(CO![]() )〕
)〕
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g)2NH3(g)△H<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响(P2>P1) | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
图示 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-![]() H++B2-,则下列说法中一定正确的是
H++B2-,则下列说法中一定正确的是
A. 在Na2B溶液中一定有:c(OH![]() )=c(H
)=c(H![]() )+c(HB
)+c(HB![]() )+2c(H2B)
)+2c(H2B)
B. NaHB溶液可能存在以下关系:c(Na![]() )>c(HB
)>c(HB![]() )>c(OH
)>c(OH![]() )>c(H
)>c(H![]() )
)
C. NaHB水溶液中一定有:c(Na![]() )+c(H
)+c(H![]() )=c(HB
)=c(HB![]() )+c(OH
)+c(OH![]() )+c(B
)+c(B![]() )
)
D. NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
查看答案和解析>>
科目: 来源: 题型:
【题目】研究物质的微观结构,有助于人们理解物质变化的本质。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
电离能 | I1 | I2 | I3 | I4 | I5 | …… |
Im/kJ·mol-1 | 578 | 1817 | 2745 | 11575 | 14830 | …… |
则该元素是______(填元素符号)。
(2)氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
①维生素B4结构如图所示,则碳原子的轨道杂化类型是_________;1 mol维生素B4分子中含有σ键的数目为________。
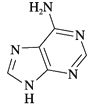
②NF3的空间构型为______(用文字描述);与NF3分子互为等电子体的阴离子为______(填化学式)。
(3)过渡元素常与H2O、NH3、CN-、SCN-等形成配合物。
①C、N、O三种元素的电负性由大到小的顺序为________。
②X、Y均为第四周期元素。X基态原子的内层轨道全部排满电子,且最外层电子数为1。Y基态原子在同周期元素中未成对电子数最多,则X+基态核外电子排布式________;元素Y在周期表中位于第________族。
③在配离子[Fe(SCN)]2+中,提供空轨道的是________;[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,则[Zn(CN)4]2-的结构可用示意图表示为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有“锂”走遍天下。氧化锂(Li2O)是锂电池工业的重要原料,以粗碳酸锂为原料制备氧化锂的一种工艺流程如下:
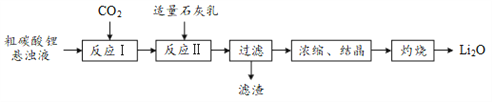
注:常温下,碳酸锂微溶于水,氢氧化锂可溶于水。
(1)反应Ⅰ中通入CO2需加压的原因是______。
(2)反应Ⅱ生成LiOH的化学方程式为______。
(3)浓缩、结晶所得LiOH·H2O通过灼烧得到Li2O。LiOH·H2O中常含有少量的Li2CO3,但该物质对所制Li2O的纯度无影响,其原因是______。
(4)锂离子电池大量应用在手机、笔记本电脑和家用小电器上。标记为Li-ion的锂离子电池的电池反应可表示为:Li + 2Li0.35NiO2![]() 2Li0.85NiO2。
2Li0.85NiO2。
①放电时,负极的电极反应式为______。
②充电时,能量转化形式主要是______。
③锂离子电池使用非水溶液做离子导体的原因是______(用离子方程式表示)。
④安全使用锂离子电池的措施有______。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知下列热化学方程式:
⑴CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=﹣870.3kJ/mol
⑵C(s)+O2(g)═CO2(g)△H2=﹣393.5kJ/mol
⑶H2(g)+ ![]() O2(g)═H2O(l)△H3=﹣285.8kJ/mol
O2(g)═H2O(l)△H3=﹣285.8kJ/mol
则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l)的焓变为( )
A.﹣488.3 kJ/mol
B.﹣244.15 kJ/mol
C.488.3 kJ/mol
D.244.15 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度时,N2与H2反应过程中能量变化的曲线如图.下列叙述正确的是( )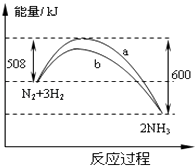
A.该反应的热化学方程式为:N2+3H22NH3△H=﹣92kJ/moL
B.b曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的放热增多
D.加入催化剂可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是( )
A.原子序数: X<YB.原子半径:X<Y
C.离子半径:X<Y D.原子最外层电子数:X<Y
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组按如下流程,进行海带中碘含量的测定。
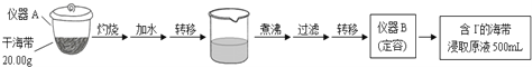
(1)写出仪器名称:A______,B______。
(2)取20.00 mL上述海带浸取原液,加稀H2SO4和足量KIO3,使I-和IO3-完全反应。再以淀粉为指示剂,用2.0×10-3mol/L的Na2S2O3溶液滴定,当I2恰好完全反应时,用去Na2S2O3溶液20.00mL。(已知:5I-+ IO3-+ 6H+=3I2 + 3H2O;I2 + 2S2O32-=2I-+ S4O62-)
①判断用Na2S2O3溶液滴定恰好完全反应的现象是______。
②计算该干海带中碘的质量分数______。(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌。“一滴香”的分子结构如图所示,下列说法正确的是

A. 该有机物分子式为:C7H10O3
B. 该有机物所有质子可能在同—平面
C. 该有机物能发生取代、加成、氧化、还原反应
D. 该有机物的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com