
科目: 来源: 题型:
【题目】FeCl3蚀刻液由FeCl3和盐酸等组成,可用于蚀刻铜及铜合金等。
(1)加入盐酸可抑制Fe3+及生成的Cu2+的水解, Fe3+水解的离子方程式为____。
(2)FeCl3溶液蚀刻铜的化学方程式为____。
(3)测定某废蚀刻液中Cu2+含量的实验步骤如下:量取25.00mL废蚀刻液,加入足量的NH4HF2(掩蔽Fe3+,消除干扰),加入稍过量KI溶液(2Cu2++4I-=2CuI↓+ I2),在暗处静置5min,然后用0.02000mol·L-1Na2S2O3标准溶液滴定(I2+2S2O![]() =2I-+S4O
=2I-+S4O![]() ),接近终点时,加入淀粉和10mL10%NH4SCN溶液(CuI可吸附少量I2, CuSCN不吸附I2),继续滴定至终点,消耗Na2S2O3溶液20.00mL。
),接近终点时,加入淀粉和10mL10%NH4SCN溶液(CuI可吸附少量I2, CuSCN不吸附I2),继续滴定至终点,消耗Na2S2O3溶液20.00mL。
①不加NH4HF2会导致测得的铜的含量____(填:“偏高”“偏低”或“不变”)。
②通过计算确定该废蚀刻液中铜的含量(单位g·L-1,写出计算过程)____。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物I是一种用于制备抗高血压药物阿替洛尔的中间体。其合成路线流程图如下:

(1)I中含氧官能团名称是____和____。
(2)B→C的反应类型是____。
(3)已知B的分子式为C9H10O2,写出B的结构简式:____。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式:____。
①含有二个苯环;
②能与NaHCO3反应生成CO2;
③分子中有5种不同化学环境的氢。
(5)以流程图中化合物A为原料可通过四步转化制备化合物![]() 。请用课本上学过的知识在横线上补充①~④的反应试剂和反应条件(样式:
。请用课本上学过的知识在横线上补充①~④的反应试剂和反应条件(样式:![]() )______。
)______。

(6)请写出以C2H5OH和![]() 为原料制备
为原料制备![]() 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)______。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如右图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )

A. 6:1 B. 3:1 C. 2:1 D. 1:2
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3![]() 2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为( )
2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为( )
A. 5∶3 B. 5∶4 C. 1∶1 D. 3∶5
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
A. 28g以任意比组成的CO与N2混合气体中含有原子数为2NA
B. 将100mL0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.01 NA
C. 在H2O2 + Cl2 =2HCl + O2反应中,每生成32g氧气,则转移4NA个电子
D. 1L 1 mol/L 的盐酸中有NA 个HCl分子
查看答案和解析>>
科目: 来源: 题型:
【题目】回答下列问题:
(1)用“>”或“<”填写下表。
第一电离能 | 熔点 | 沸点(同压) | 键能 |
P____S | MgO____CaS | CF4____SiCl4 | H-Cl____ H-Br |
(2)一种制取NH2OH的反应为2NO2-+4SO2 + 6H2O+ 6NH3 = 4SO![]() +6NH4++2NH2OH。
+6NH4++2NH2OH。
①N、H、O的电负性从小到大的顺序为____。
②NH3分子的空间构型为____。
③NH2OH极易溶于H2O,除因为它们都是极性分子外,还因为____。
(3)配合物K[PtCl3(NH3)]中[PtCl3(NH3)]-的结构可用示意图表示为____(不考虑空间构型)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学兴趣小组对SO2的性质和回收利用等问题进行探究,对环境保护具有重要意义。SO2溶于水生成亚硫酸,亚硫酸的酸性强于次氯酸。选择下面的装置和药品来探究亚硫酸与次氯酸的酸性强弱。
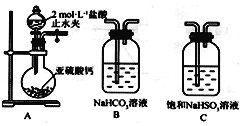
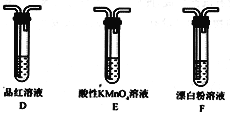
(1)装置A中盛放亚硫酸钙的仪器名称是_________________,其中发生反应的化学方程式为_____________________________________________________;
(2)装置正确的连接顺序为A→____→ → → D → F ,其中装置B的作用是_________。证明亚硫酸的酸性强于次氯酸的现象为________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫化氢裂解制取氢气的反应为2H2S(g)![]() 2H2(g)+S2(g)。向恒容密闭容器中充入一定量的H2S气体,测得体系中气体的平衡组成与温度的关系如图所示。下列说法正确的是
2H2(g)+S2(g)。向恒容密闭容器中充入一定量的H2S气体,测得体系中气体的平衡组成与温度的关系如图所示。下列说法正确的是

A. 该反应平衡常数随温度升高而增大
B. M点时容器内气体总压强比N的大
C. M点时,H2S的平衡转化率为50%
D. 维持M点温度不变,向容器中再充入0.2molH2S、0.2molH2、0.1molS2(g),则v(正) = v(逆)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com