
科目: 来源: 题型:
【题目】化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热量的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等。
(1)下列△H表示物质燃烧热的是 ______ ;表示物质中和热的是 ______ (填“△H1”、“△H2”、“△H3”等).
A.2H2(g)+O2(g)═2H2O(l)△H1
B.C(s)+1/2O2(g)═CO(g)△H2
C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H3
D.C(s)+O2(g)═CO2(g)△H4
E.C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H5
F.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H6
G.2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H7
H.CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H8
(2)依据事实,写出下列反应的热化学方程式.
Ⅰ、在25℃、101kPa下,1gCH3OH燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为 _______________________;
Ⅱ、1.00L1.00mol/LH2SO4溶液与2.00L1.00mol/LNaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为 ________________________;
Ⅲ、已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、 946kJ,则N2与H2反应生成NH3的热化学方程式为 _______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2SO2(g)+O2(g)2SO3(g),反应过程的能量变化如图所示.
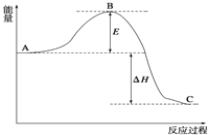
已知1molSO2(g)氧化为1molSO3(g)的△H=-99kJ/mol.
请回答下列问题:
(1)E的大小对该反应的反应热 ______ 影响?(填“有”或“无”).该反应通常用V2O5作催化剂,加V2O5会使图中B点 ______ (填“升高”或“降低”);
(2)图中△H= ______ kJ/mol;
(3)如果反应速率υ(SO2)为0.05mol/(Lmin),则υ(O2)= ______ mol/(Lmin);
(4)1molSO2(g)氧化为1molSO3(g)的反应热△H1 ______ 1molSO3(g)还原为1molSO2(g)的反应热△H2(填“>、<或=”) 。
(5)已知单质硫的燃烧热为296kJ/mol,计算由S(s)生成3molSO3(l)的△H= _________________
查看答案和解析>>
科目: 来源: 题型:
【题目】CO(g)与H2O(g)反应的能量变化如图所示,有关两者反应的说法正确的是( )

A. 该反应为吸热反应
B. 该反应不需要加热就能进行
C. 1 molCO(g)和1mol H2O(g)具有的总能量大于1 molCO2(g)和1 molH2(g)具有的总能量
D. 1 molCO2(g)和1 molH2(g)反应生成1 molCO(g)和1mol H2O(g)要放出41 kJ热量
查看答案和解析>>
科目: 来源: 题型:
【题目】某合金与铁的物理性质的比较如下表所示:(注:硬度以金刚石为10作标准,导电性以银的导电性100为标准)
熔点 | 密度 | 硬度 | 导电性 | |
某合金 | 32000C | 3.20g/cm3 | 7.5 | 3.5 |
铁 | 15350C | 7.86g/cm3 | 4.5 | 17 |
已知该合金耐腐蚀、强度大,从性能看,该合金不适合制
A.门窗框B.炉具C.电源线D.飞机外壳
查看答案和解析>>
科目: 来源: 题型:
【题目】银的冶炼有很多方法, 在《 天工开物》 均有记载, 而现代流行的“ 氰化法”, 用 NaCN溶液浸出矿石中的银的方法是最常用的方法。 该方法具备诸多优点: 银的回收率高; 对游离态和化合态的银均能浸出; 对能源消耗相对较少; 生产工艺简便等, 但氰化物通常有毒。 其炼制工艺简介如下:

(1)矿石需要先进行破碎、 研磨, 其目的是__________。
(2)写出该工艺的一个明显的缺点__________ 。
(3)用 NaCN 浸泡矿石( 该矿石是辉银矿, 其主要成分是 Ag2S) 时, 反应容器处于开口状态, 产生的银以[Ag(CN)2]- 形式存在, 硫元素被氧化至最高价, 试写出主要反应的离子方程式__________。
(4)银往往和锌、 铜、 金等矿伴生, 故氰化法得到的银中往往因含有上述金属而不纯净, 需要进一步纯化, 从而获得纯净的银。 其中方法之一就是进行电解精炼, 在精炼过程中, 含有杂质的银作__________极( 填“阴” 或“阳”), 该电极上发生的主要反应式为__________, 金以__________形式存在。
(5)有人提出了另外的提纯银的方案, 先将锌粉还原后的混合金属用略过量的硝酸溶解, 通过精确调整溶液的 pH 来进行金属元素分离, 已知:
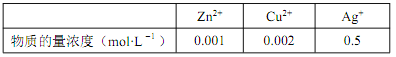
①溶解后的离子浓度如下表:
②某些金属离子的氢氧化物 Ksp如下:
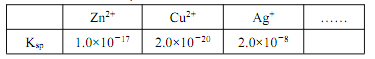
( 已知 lg2=0.3),该设计方案_______(填“ 可行” 或“ 不可行”),其原因是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】能源是人类生存和发展的重要支柱。根据要求回答下列问题。
(1)下列说法中错误的是______。

A.都是清洁能源
B.电能,H2属于二次能源,水力是一级能源
C.煤和石油属于化石燃料,燃烧会产生温室气体
D.氢能热值高,对环境无污染
(2)我国目前使用的主要能源是化石燃料,近年来我国能源总消费量与人均能源消费量如图。
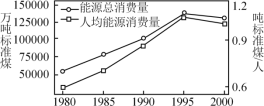
①在我国,煤的消费量巨大,且煤属于不可再生能源,寻找新能源是能源研究的主要课题之一。下列不属于新能源的是______。
A.太阳能 B.氢能 C.地热能 D.海洋能
E.生物质能 F.石油 G.天然气
②已知,1 kg煤大约放热2.9×104 kJ。风能能量巨大,地球上一年可利用的风能相当于5×1014 kw·h的电能。试计算,一年的风能若能全部利用,可相当于节省______吨燃煤。(已知,1 kw·h=3.6×103 kJ)
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应速率是通过实验测定的,下列化学反应速率的测量中,测量依据不可行的是
选项 | 化学反应 | 测量依据(单位时间内) |
A | CO(g)+H2O(g)=CO2(g)+H2(g) | 压强变化 |
B | Zn+H2SO4=ZnSO4+H2 | H2体积 |
C | 2NO2(红棕色)N2O4(无色) | 颜色深浅 |
D | Ca(OH)2+Na2CO3=CaCO3↓+2NaOH | 沉淀质量 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W代表四种短周期元素,有关它们的部分结构信息及性质信息如表所示。
元素 | 部分结构信息 | 部分性质信息 |
X | X的单质由双原子分子构成 | X的氢化物水溶液呈碱性 |
Y | Y原子的最外层电子数是其内层电子数的两倍 | Y能形成多种气态氢化物 |
Z | Z原子有三个电子层 | 含有Z元素的化合物的焰色反应呈黄色 |
W | W原子的最外层电子数等于(2n+1)(n为原子核外电子层数) | W和Z能按1∶1的原子个数比形成离子化合物 |
请按要求回答下列问题:
(1)W在元素周期表中的位置是______。
(2)X简单气态氢化物的分子式为______。(用化学式表示)
(3)X、Y、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是______。(用化学式表示)
(4)Z单质在W单质中发生反应的实验现象是______。
(5)写出W的单质与二氧化硫的混合气体通入水中所发生反应的离子方程式:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】航天飞船用高氯酸铵固体作燃料,点燃时的反应:2NH4ClO4![]() N2↑+4H2O+Cl2↑+2O2↑。下列对该反应的叙述中不正确的是( )
N2↑+4H2O+Cl2↑+2O2↑。下列对该反应的叙述中不正确的是( )
A. 该反应中反应物的总能量小于生成物的总能量
B. 该反应属于分解反应、氧化还原反应、放出能量的反应
C. 高氯酸铵是一种盐,属于离子化合物
D. 在能量变化上,该反应主要是化学能转变为热能和动能
查看答案和解析>>
科目: 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.下列叙述中不正确的是( )
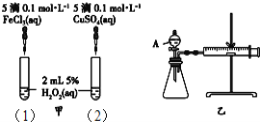
A. 实验中H2O2分解的速率为(1)>(2)
B. 图乙实验可通过测定相同状况下,产生的气体体积与反应时间来比较反应速率
C. H2O2分解的热化学方程式2H2O2(l)═2H2O(l)+O2(g)△H>0
D. 图甲中(1)、(2)两个实验中H2O2分解的△H相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com