
科目: 来源: 题型:
【题目】某小组探究化学反应2Fe2++I2 ![]() 2Fe3++2I-,完成了如下实验:
2Fe3++2I-,完成了如下实验:
已知:Agl是黄色固体,不溶于稀硝酸。新制的AgI见光会少量分解。

(1)Ⅰ、Ⅱ均未检出Fe3+,检验Ⅱ中有无Fe3+的实验操作及现象是:取少量Ⅱ中溶液,___________。
(2)Ⅲ中的黄色浑浊是___________。
(3)经检验,Ⅱ→Ⅲ的过程中产生了Fe3+。进一步探究表明产生Fe3+的主要原因是Fe2+被I2氧化。Fe3+产生的其它途径还可能是___________(用离子方程式表示)。
(4)经检验,Ⅳ中灰黑色浑浊中含有AgI和Ag。为探究Ⅲ→Ⅳ出现灰黑色浑浊的原因,完成了实验1和实验2。
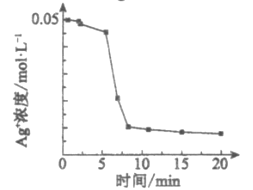
(实验1)向1 mL0.1mol/L FeSO4溶液中加入1 mL0.1mol/LAgNO3溶液,开始时,溶液无明显变化。几分钟后,出现大量灰黑色浑浊。反应过程中温度几乎无变化。测定溶液中Ag+浓度随反应时间的变化如下图。
(实验2)实验开始时,先向试管中加入几滴Fe2(SO4)3溶液,重复实验1,实验结果与实验1相同。
①实验1中发生反应的离子方程式是___________。
②通过以上实验,小组同学怀疑上述反应的产物之一可作反应本身的催化剂。则Ⅳ中几秒钟后即出现灰黑色浑浊的可能原因是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 5.6g铁与稀硝酸反应,转移电子数一定为0.3NA
B. 密闭容器中,1molN2和3molH2催化反应后分子总数大于2NA
C. 3.2gN2H4中含有共用电子对的总数为0.6NA
D. 室温下,pH=1的H3PO4溶液中,含有0.1NA个H+
查看答案和解析>>
科目: 来源: 题型:
【题目】2018年报道了使用α-溴代羰基化合物合成大位阻醚和硫醚的有效方法,可用于药物化学和化学生物学领域。用此法合成化合物J的路线如下:

已知:
回答下列问题:
(1)A的结构简式为____________。D中含有的官能团名称是____________。
(2)由B生成C的化学方程式是______________________。
(3)C→D所需试剂和反应条件为_____________________。
(4)G的化学名称为_____________,F+H→J的反应类型是___________。
(5)F与C在CuBr和磷配体催化作用下也可合成大位阻醚,写出一种有机产物的结构简式:_____________。
(6)化合物X是E的同分异构体,分子中不含羧基,既能发生水解反应,又能与金属钠反应。符合上述条件的X的同分异构体有_____种(不考虑立体异构),其中能发生银镜反应,核磁共振氢谱有3组峰,峰面积之比为1:1:6的结构简式为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:

(1)碳原子价层电子的轨道表达式为__________,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_______。NH3比PH3的沸点高,原因是_________。
(3)氮元素的第一电离能比同周期相邻元素都大的原因是____________。
(4)EMIM+离子中,碳原子的杂化轨道类型为______。分子中的大π键可用符号![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为![]() ),则EMIM+离子中的大π键应表示为________。
),则EMIM+离子中的大π键应表示为________。

(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于_______晶体,其中硼原子的配位数为_______。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为NA,则该晶胞中原子的空间利用率为________(列出化简后的计算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究CO、CO2的回收利用既可变废为宝,又可减少碳的排放。回答下列问题:
(1)二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料”,由CO和H2制备二甲醚的反应原理如下:
CO(g)+2H2(g)![]() CH3OH(g) ΔH=-90.1kJ/mol
CH3OH(g) ΔH=-90.1kJ/mol
2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH=-24.5kJ/mol
CH3OCH3(g)+H2O(g) ΔH=-24.5kJ/mol
已知:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=-41.0kJ/mol
CO2(g)+H2(g) ΔH=-41.0kJ/mol
则2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)的ΔH=__________,有利于提高该反应中CO2平衡转化率的条件是______(填标号)。
CH3OCH3(g)+3H2O(g)的ΔH=__________,有利于提高该反应中CO2平衡转化率的条件是______(填标号)。
A.高温低压 B.高温高压 C.低温低压 D.低温高压
(2)T1K时,将1mol二甲醚引入一个抽空的150L恒容容器中,发生分解反应: CH3OCH3(g)![]() CH4(g)+H2(g)+CO(g),在不同时间测定容器内的总压,所得数据见下表:
CH4(g)+H2(g)+CO(g),在不同时间测定容器内的总压,所得数据见下表:
反应时间t/min | 0 | 6.5 | 13.0 | 26.5 | 52.6 | ∞ |
气体总压p总/kPa | 50.0 | 55.0 | 65.0 | 83.2 | 103.8 | 125.0 |
①由表中数据计算:0~6.5min内的平均反应速率v(CH3OCH3)=_________,反应达平衡时,二甲醚的分解率为_______,该温度下平衡常数K=__________。
②若升高温度,CH3OCH3的浓度增大,则该反应为______反应(填“放热”或“吸热”),要缩短达到平衡的时间,可采取的措施有___________、__________。
(3)在T2K、1.0×104kPa下,等物质的量的CO与CH4混合气体发生如下反应: CO(g)+CH4(g)![]() CH3CHO(g),反应速率v=v正v逆=k正p(CO)·p(CH4)-k逆p(CH3CHO),k正、k逆分别为正、逆向反应速率常数,p为气体的分压(气体分压p=气体总压p总×体积分数)。用气体分压表示的平衡常数Kp=4.5×10-5(kPa)-1,则CO转化率为20%时
CH3CHO(g),反应速率v=v正v逆=k正p(CO)·p(CH4)-k逆p(CH3CHO),k正、k逆分别为正、逆向反应速率常数,p为气体的分压(气体分压p=气体总压p总×体积分数)。用气体分压表示的平衡常数Kp=4.5×10-5(kPa)-1,则CO转化率为20%时![]() =_______。
=_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应最终不能生成三价铁的是( )
A.少量Fe与足量稀HNO3反应B.铁丝在硫蒸气中燃烧
C.Fe(OH)2露置于空气中D.向FeBr2溶液中通入足量Cl2
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,反应N2O4(g)![]() 2NO2(g)△H>0,在密闭容器中达到平衡。下列说法不正确的是( )
2NO2(g)△H>0,在密闭容器中达到平衡。下列说法不正确的是( )
A. 加压时(体积变小),将使正反应速率增大
B. 保持体积不变,升高温度,再达平衡时颜色变深
C. 保持体积不变,加入少许N2O4,再达到平衡时,颜色变深
D. 保持体积不变,加入少许NO2,将使正反应速率减小
查看答案和解析>>
科目: 来源: 题型:
【题目】研究烟气中SO2的转化具有重要意义。
(1)二氧化硫—空气质子交换膜燃料电池是利用空气将烟气中所含SO2转化为SO42-,其装置如图所示:

①装置内质子(H+)的移动方向为___________(填“从A→B”或“从B→A”)。
②负极的电极反应式为___________。
(2)脱除燃煤烟气中SO2的一种工业流程如下:

①用纯碱溶液吸收SO2将其转化为HSO3-,反应的离子方程式是___________。
②再生池中加过量的石灰乳实现再生,部分产物可排回吸收池吸收SO2。用于吸收SO2的产物是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com