
科目: 来源: 题型:
【题目】下列条件下,两瓶气体所含原子数不相等的是( )
A.同质量、不同密度的![]() 和COB.同温度、同压强、同体积的
和COB.同温度、同压强、同体积的![]() 和
和![]()
C.同体积、同密度的![]() 和
和![]() D.同质量、同体积的
D.同质量、同体积的![]() 和
和![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室模拟侯氏制碱法原理,可以制备一些常见的化合物。
i. 30℃时,向饱和NaCl溶液中加入NH4HCO3细粉,制备NaHCO3晶体。
(1)已知30℃时几种盐的溶解度为:
物质 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
S(g/100gH2O) | 36.3 | 27.0 | 11.1 | 41.1 |
书写化学方程式_______________________。根据反应原理结合信息解释NaHCO3易析出的原因__________________________。

(2)过滤出NaHCO3晶体后,为继续分离滤液中的物质,设计如图装置。左侧发生装置可制取氨气,原因是_____________。一段时间后,试管中析出白色晶体为_______。用冰水浴降温目的是_____________。
ii. 制取(NH4)2SO4晶体的流程如下:

(3)“转化”步骤中CO2不宜过量,原因是__________________。
(4)操作I和II所需的实验步骤顺序是____________(选填编号,可重复选择)。
a. 蒸发浓缩 b. 蒸馏 c. 过滤 d. 萃取 e. 分液 f. 冷却结晶
(5)为测定某硫酸铵样品(杂质为碳酸铵)纯度。先准确称取5.000g样品溶于水,加入足量的_______,再加入足量BaCl2溶液充分反应后过滤、洗涤沉淀并烘干至恒重,最终所得固体为8.155g。则硫酸铵样品的纯度为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有原子序数之和为51的5种短周期元素A,B,C,D,E。已知A的单质在常温下为无色气体;B原子的最外层电子数比次外层电子数多3个;C和B属于同一主族;D的最高正价与负价的代数和为4,其最高价氧化物对应的水化物的酸性在同主族元素中最强,E元素最外层电子数与其K层电子数相同。
(1)试写出它们的元素符号。__________________________________________。
(2)写出B的氢化物的电子式_____________________________。
(3)由A、D两种元素形成的化合物是________化合物(填“离子”或“共价”),化合物内存在________键(填“离子”或“共价”)。
(4)由D、E两种元素形成的化合物的电子式为________,它属于________化合物,化合物内存在________键。
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是________(多选)。
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
查看答案和解析>>
科目: 来源: 题型:
【题目】E是一种能发生加聚反应的有机合成中间体,合成E的路线如下。

(1)反应①的类型是________________;反应②的试剂和条件是__________________。
(2)写出反应③的化学方程式_______________________________。
(3)D的结构简式___________。
D有多种同分异构体,写出一种符合下列要求的结构简式____________。
i. 含有苯环 ii. 能发生水解反应 iii. 苯环上的一溴代物有两种
(4)通过反应⑤得到E的产率不高,原因是___________________________。
(5)设计一条由CH3CH=CHCH3为原料制备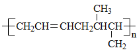 的合成路线。___________
的合成路线。___________
(合成路线常用的表示方法为:X![]() Y……
Y……![]() 目标产物)
目标产物)
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化钠中混有硫酸镁、硫酸钙、氯化镁杂质,除去杂质,加入的试剂顺序为( )
①![]() 、NaOH、
、NaOH、![]() 、HCl ②
、HCl ②![]() 、HCl、
、HCl、![]() 、NaOH
、NaOH
③NaOH、![]() 、
、![]() 、HCl ④
、HCl ④![]() 、
、![]() 、NaOH、HCl
、NaOH、HCl
A.①③B.①④C.②④D.②③
查看答案和解析>>
科目: 来源: 题型:
【题目】请回答下列问题:
(1)羰基铁[Fe(CO)5]会使合成甲醇和合成氨等生产过程中的催化剂中毒.Fe(CO)5常温下呈液态,熔点为﹣20.5℃,沸点为103℃,易溶于非极性溶剂.据此可以判断Fe(CO)5晶体类型为__。
(2)科学家通过X射线探明,MgO、CaO的晶体结构与NaCl晶体结构相似(如图所示)

①比较晶体熔点的高低MgO__CaO(填“高于”或“低于”),
②Mg2+的配位原子所构成的立体几何构型为__,③MgCO3晶格能大于CaCO3,为何MgCO3更易分解__。
(3)Ni的堆积与MgO中氧原子堆积相同,Ni可以吸附H2,氢以单个原子形式填入四面体空隙,则Ni最大量吸收H2后,n(Ni):n(H)=__。
查看答案和解析>>
科目: 来源: 题型:
【题目】元素A、B、C都是短周期元素,它们的原子序数大小为A<B<C。A元素原子的最外层电子数为次外层电子数的2倍;B元素原子的次外层电子数是最外层电子数的2倍。B与C可形成共价化合物BC4。请回答下列问题:
(1)这三种元素所对应的气态氢化物中最不稳定的是__________(填化学式),该氢化物在空气中燃烧的化学方程式为__________________________________________________________。
(2)它们的最高价氧化物对应的水化物中酸性最强的是__________,最弱的是__________(填酸的化学式)。
(3)BC4的化学式是__________。BC4不稳定,遇水易形成B的含氧酸及C的氢化物。近代海战中为了掩蔽军事目标,通常采用喷BC4和液氨的方法以形成烟幕,有关化学反应用方程式表示为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】同周期的X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HZO4![]() H2YO4
H2YO4 ![]() H3XO4,下列判断正确的是 ( )
H3XO4,下列判断正确的是 ( )
①阴离子的还原性按X、Y、Z顺序减弱
②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小
④气态氢化物的稳定性按X、Y、Z顺序减弱
①②A. ②③ B. ①②③ C. ①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)钒在元素周期表中的位置为__________,其价层电子排布图为____________。
(2)基态镓(Ga)原子的电子排布式:__________________。
(3) Fe3+的电子排布式为__________________。
(4)基态铜原子的核外电子排布式为__________________。
(5) Ni2+的价层电子排布图为_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)X原子在第二电子层上只有一个空轨道,则X是__;其轨道表示式为__;R原子的3p轨道上只有一个未成对电子,则R原子可能是__、 ;Y原子的核电荷数为29,其电子排布式是__,其在元素周期表中的位置是__,是属于__区的元素。
(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:__、__、__。
(3)下列分子中若有手性原子,请用“*”标出其手性碳原子__。![]()
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)__。
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4__H2SO3;H3PO4__H3PO3。
(6)根据价层电子对互斥理论判断下列问题:
H2O中心原子的杂化方式为__杂化,分子的立体构型为__。
BF3分子中,中心原子的杂化方式为__杂化,分子的立体构型为__。
(7)H2O的沸点(100℃)比H2S的沸点(﹣61℃)高,这是由于________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com