
科目: 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图。请回答下列问题:
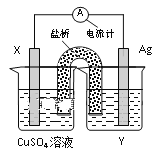
(1)电极X的材料名称是___;电解质溶液Y溶质的化学式是___;
(2)银电极为电池的___极,发生的电极反应为___;
(3)外电路中的电子是从___电极流向___电极。(填电极材料名称)。
(4)当有1.6g铜溶解时,银棒增重___g。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)常温下常压下,1g固态碳与水蒸气恰好完全反应,反应生成气体CO和H2,吸收10.94kJ热量,此反应的热化学方程式为___。
(2)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-Q1kJ·mol-1,
②2H2(g)+O2(g)=2H2O(g) ΔH2=-Q2kJ·mol-1,
③2H2(g)+O2(g)=2H2O(l) ΔH3=-Q3kJ·mol-1。
常温下,取体积比4∶1的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为___kJ。
(3)以H2为燃料可制成氢氧燃料电池。已知:2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1,某氢氧燃料电池释放228.8kJ电能时,生成1mol液态水,该电池的能量转化率为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】由芳香烃X可合成多种在化工、医药等领域的物质,过程如下(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H为聚合物。
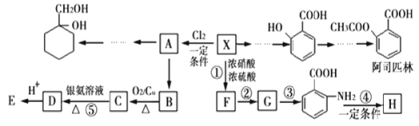
已知:
Ⅰ.芳香烃X的质谱图如图所示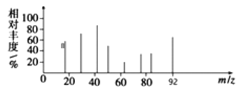
II.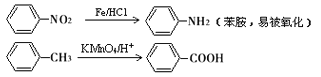
(1)X的分子式为______________,B的结构简式为________________;
(2)阿司匹林中含氧官能团的名称为__________________________;
(3)③的反应类型为___________;由A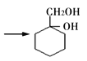 的过程中发生的反应为:苯环的加成反应→消去反应→加成反应→__________________;
的过程中发生的反应为:苯环的加成反应→消去反应→加成反应→__________________;
(4)反应④的化学方程式为____________________________________________;
(5)反应⑤的化学方程式为____________________________________________;
(6)![]() 的一种同系物
的一种同系物![]() 有多种同分异构体,其中符合下列要求的共有_____________种(不考虑立体异构);
有多种同分异构体,其中符合下列要求的共有_____________种(不考虑立体异构);
①能与NaHCO3反应放出CO2 ②能与FeCl3溶液发生显色反应
写出其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的结构简式__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有几种有机物的键线式结构如图:
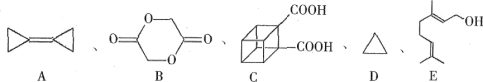
回答下列问题:
(1)有机物B所含官能团的名称是____。
(2)C的官能团位置异构体有___种。
(3)E的分子式为____。
(4)A与溴的四氯化碳反应,其产物的结构简式为____,该反应类型是____。
(5)在镍,80℃作用下,D与氢气反应生成丙烷。写出化学方程式:____。
查看答案和解析>>
科目: 来源: 题型:
【题目】中和热的测定是高中重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
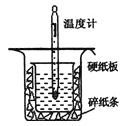
(1)从图中实验装置看,其中尚缺少的一种玻璃用品是___;
(2)为保证该实验成功该同学采取了许多措施,如图的碎纸条的作用在于___。
(3)若改用60mL0.25mol·L-1H2SO4和50mL0.55mol·L-1NaOH溶液进行反应与上述实验相比,所放出的热量___(填“相等”、“不相等”),若实验操作均正确,则所求中和热___(填“相等”、“不相等”)
(4)50mL0.55mol/LNaOH溶液和50mL0.25mol/L硫酸溶液的实验数据如下表:
请填写下表中的空白:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ①___ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为50mL0.55mol/LNaOH溶液和50mL0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=___J/mol(取小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是___(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素a、b、c、d、e的原子序数依次增大。a的简单阴离子与锂离子具有相同的电子层结构,b原子最外层电子数等于内层电子数的2倍。d的单质与稀盐酸剧烈反应放出a2。在1L0.2mol·L-1a2e的水溶液中缓慢通入ec2气体,该溶液的pH与ec2气体体积(标准状况)的关系如图所示。下列说法不正确的是
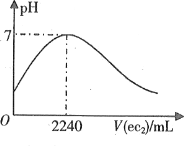
A.a和b可构成所有原子共平面的分子
B.在b、c、e的气态氢化物中,c的最稳定
C.d的氯化物一定能破坏水的电离平衡
D.e的最高价含氧酸与其氢化物可能发生氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)请写出以下物质的电子式:
Na2O2:___;H2S:___;NaHS:___。
(2)用“>”或“<”回答下列问题:
酸性:H2SiO3___H3PO4;稳定性:HCl___CH4;氧化性:Cu2+___Fe3+。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机化学反应因反应条件不同,可生成不同的有机产品。例如:
(1)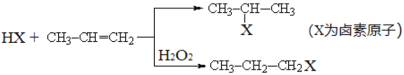
(2)苯的同系物与卤素单质混合,若在光照条件下,侧链上氢原子被卤素原子取代;若在催化剂作用下,苯环上的氢原子被卤素原子取代。
工业上利用上述信息,按下列路线合成结构简式为![]() 的物质,该物质是一种香料。
的物质,该物质是一种香料。
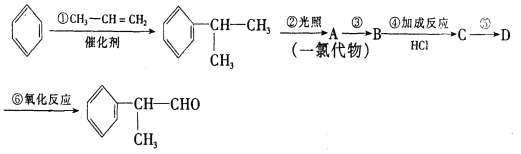
请根据上述路线,回答下列问题:
(1)A的结构简式可能为_______________________________。
(2)反应①、③的反应类型分别为______________、______________。
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):______________。
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是___________________________________。
(5)这种香料具有多种同分异构体,其中某些物质有下列特征:①其水溶液遇FeCl3溶液呈紫色②分子中有苯环,且苯环上的一溴代物有两种。写出符合上述条件的物质可能的结构简式(只写两种):_____________、________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W和X的最高价氧化物的水化物之间可以相互反应生盐和水,该反应的离子方程式为___。
(2)W与Y可形成化合物W2Y,该化合物的电子式为___。
(3)比较Y、Z气态氢化物的稳定性 > (用化学式表示)___。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为___。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > (用离子符号表示)___。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,在体积均为20mL、浓度均为0.1mol·L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加氢氧化钠溶液体积的关系如图所示。
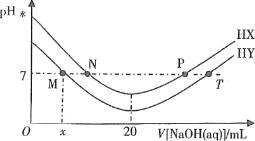
下列推断正确的是
A.HX的电离方程式为HX=H++X-
B.T点时c(Na+)=c(Y-)>c(H+)=c(OH-)
C.常温下用蒸馏水分别稀释N、P点溶液,pH都降低
D.常温下,HY的电离常数![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com