
科目: 来源: 题型:
【题目】氮、磷、砷、铁等元素及其化合物在现代农业、科技、国防建设中有着许多独特的用途。
(1)基态砷原子中核外电子占据最高能层的符号为__,该能层的原子轨道数有__个。
(2)氮的一种氢化物N2H4是一种良好的火箭发射燃料,传统制备肼的方法是:NaClO+2NH3=N2H4+NaCl+H2O,又知肼的熔点、沸点分别为1.4℃、113.5℃,氨气的熔点、沸点分别为-77.7℃、-33.5℃。
①N2H4中氮原子的杂化轨道类型为__杂化,基态N原子电子占据最高能级的电子云轮廓图为___形。
②肼与氨气熔点、沸点差异最主要的原因是__。
(3)氨分子是一种常见配体,配离子[Co(NH3)6]3+中存在的化学键有__(填序号)。
A.离子键 B.极性键 C.配位键 D.氢键
查看答案和解析>>
科目: 来源: 题型:
【题目】在钯基催化剂表面上,甲醇制氢的反应历程如图所示,其中吸附在钯催化剂表面上的物种用*标注。
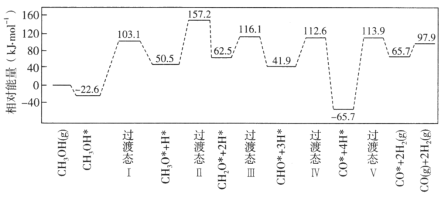
(1)![]() 的△H=_____________kJ·mol-1;该历程中最大能垒(活化能)E正=____________kJ·mol-1,写出该步骤的化学方程式_________________。
的△H=_____________kJ·mol-1;该历程中最大能垒(活化能)E正=____________kJ·mol-1,写出该步骤的化学方程式_________________。
(2)在一定温度下,CO和H2混合气体发生反应:![]() ,反应速率υ=υ正-υ逆=k正c(CO)·c2(H2)-k逆c(CH3OH),k正、k逆分别为正、逆反应速率常数。达到平衡后,若加入高效催化剂,
,反应速率υ=υ正-υ逆=k正c(CO)·c2(H2)-k逆c(CH3OH),k正、k逆分别为正、逆反应速率常数。达到平衡后,若加入高效催化剂,![]() 将___________(填“增大”、“减小”或“不变”);若升高温度,
将___________(填“增大”、“减小”或“不变”);若升高温度,![]() 将____________(填“增大”、“减小”或“不变”)。
将____________(填“增大”、“减小”或“不变”)。
(3)353K时,在刚性容器中充入CH3OH(g),发生反应:![]() 。体系的总压强p随时间t的变化如表所示:
。体系的总压强p随时间t的变化如表所示:
t/min | 0 | 5 | 10 | 15 | 20 | ∞ |
p/kPa | 101.2 | 107.4 | 112.6 | 116.4 | 118.6 | 121.2 |
①若升高反应温度至373K,则CH3OH(g)分解后体系压强p∞(373K)___________121.2kPa(填“大于”、“等于”或“小于”),原因是________________________。
②353K时,该反应的平衡常数KP=__________(kPa)2(KP为以分压表示的平衡常数,计算结果保留1位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组探究SO2与AgNO3溶液的反应,实验记录如下:
序号 | Ⅰ | Ⅱ | Ⅲ |
实验 步骤 |
|
|
|
实验现象 | 得到无色溶液a和白色沉淀b | 产生无色气体,遇空气变为红棕色 | 产生白色沉淀 |
下列说法正确的是
A.透过测Ⅰ中无色溶液a的pH可以判断SO2是否被氧化
B.实验Ⅱ说明白色沉淀b具有还原性
C.实验Ⅲ说明溶液a中一定有![]() 生成
生成
D.实验Ⅰ、Ⅱ、Ⅲ说明SO2与AgNO3溶液反应既有Ag2SO4生成,又有Ag2SO3生成
查看答案和解析>>
科目: 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
![]()
![]()
![]()
![]()
![]()
![]()
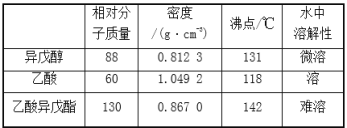
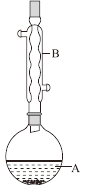
实验步骤:在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50 min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g。下列问题:
(1)仪器B的名称是____________。
(2)在洗涤操作中,第一次水洗的主要目的是______,第二次水洗的主要目的是______。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是_________。
(5)实验中加入少量无水MgSO4的目的是_________。
(6)本实验的产率是________(填标号)。
a.30% b.40% c.60% d.90%
(7)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏______![]() 填“高”或“低”
填“高”或“低”![]() ,其原因是______。
,其原因是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,分别取未知浓度的AOH和BOH两种碱的稀溶液,加水稀释至原体积的n倍。两溶液稀释倍数的对数值(lgn)与溶液的pH变化关系如图所示。下列叙述正确的是
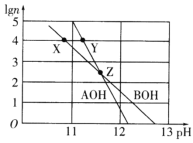
A.水的电离程度:Z>X=Y
B.常温下,Kb(BOH)<Kb(AOH)
C.中和等体积X、Y两点溶液,后者消耗HC1的物质的量多
D.物质的量浓度相同的AC1溶液和BC1溶液,前者阳离子浓度之和小于后者
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸盐与钴(Ⅲ)形成的一种配合物[Co(NH3)5NO2]Cl2的制备流程如下:
CoCl2·6H2O![]() [Co(NH3)5Cl]Cl2
[Co(NH3)5Cl]Cl2![]() [Co(NH3)5NO2]Cl2
[Co(NH3)5NO2]Cl2
(1)Co2+基态核外电子排布式为___。
(2)配合物[Co(NH3)5Cl]Cl2中与Co3+形成配位键的原子为___(填元素符号);配离子[Co(NH3)5NO2]2+的配体中氮原子的杂化轨道类型为___。
(3)NO![]() 的空间构型为___,与它互为等电子体的分子为___(写化学式)。
的空间构型为___,与它互为等电子体的分子为___(写化学式)。
(4)H2O2与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为___。
(5)1mol[Co(NH3)5Cl]Cl2中含有σ键的数目为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】CO的催化氧化在消除环境污染、净化空气等方面有重要价值。最新研究发现:常温下CO在Au/BN表面很难被O2氧化,但在H2O的参与下反应很容易发生,转化示意图如图:
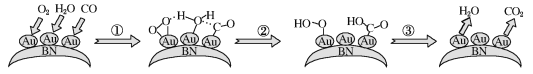
下列说法正确的是( )
A.CO2和H2O均只含极性共价键,且为极性分子
B.过程①有氢键形成
C.催化剂可以改变反应的路径,但不会改变反应速率和限度
D.在H2O和Au/BN的共同作用下,CO易被O2氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空:
(1)命名下列有机物:
CH3CHOHCH3____________
HOCH2CH2CHO____________
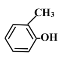 _________________
_________________
(2)燃烧某有机物A 1.50 g,生成1.12 L(标准状况)CO2和0.05 mol H2O,该有机物的蒸气对空气的相对密度是1.04,则该有机物的分子式为_____。
(3)已知端炔烃在催化剂存在下可发生偶联反应:![]() +H2, 称为Glaser反应,回答下列问题:
+H2, 称为Glaser反应,回答下列问题:
已知: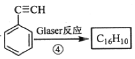 ,该转化关系的产物E(C16H10)的结构简式是_______,用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气____mol。
,该转化关系的产物E(C16H10)的结构简式是_______,用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气____mol。
(4)已知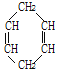 可简写为
可简写为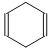 ,现有某化合物W的分子结构可表示为
,现有某化合物W的分子结构可表示为![]()
![]() 的一氯代物有______种
的一氯代物有______种![]()
![]() 下列有关W的说法不正确的是______
下列有关W的说法不正确的是______![]() 填编号
填编号![]() ;
;
a.能发生还原反应
b.能发生氧化反应
c.等质量的W与苯分别完全燃烧所消耗的氧气量,前者大
d.与苯互为同分异构体
![]() 写出W的芳香族同分异构体
写出W的芳香族同分异构体![]() 能发生聚合反应
能发生聚合反应![]() 的结构简式_________;该聚合反应的化学方程式为_________;
的结构简式_________;该聚合反应的化学方程式为_________;
![]() 属于______
属于______![]() 填编号
填编号![]() 。
。
![]() 芳香烃
芳香烃![]() 环烃
环烃![]() 不饱和烃
不饱和烃![]() 炔烃
炔烃
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 乳酸薄荷醇酯(![]() )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
B. 乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C. 用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3
D. 分子式为C9H12的苯的同系物,若苯环上只有一个取代基,则其一溴代物最多有6种
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年诺贝尔化学奖授予三位开发锂离子电池的科学家。某高能锂离子电池的反应方程式为![]() (x<1)。以该锂离子电池为电源、苯乙酮为原料制备苯甲酸的装置如图所示(苯甲酸盐溶液酸化后可以析出苯甲酸)。下列说法正确的是
(x<1)。以该锂离子电池为电源、苯乙酮为原料制备苯甲酸的装置如图所示(苯甲酸盐溶液酸化后可以析出苯甲酸)。下列说法正确的是
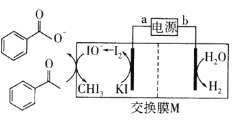
A.电池放电时,Li+向b极移动
B.电池充电时,a极反应式为LiCoO2-xe-=Lil-xCoO2+xLi+
C.M为阳离子交换膜
D.生成苯甲酸盐的反应为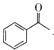 +3IO→
+3IO→![]() + CHI3+2OH-
+ CHI3+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com