
科目: 来源: 题型:
【题目】如图曲线表示其他条件一定时,反应2NO+O2![]() 2NO2(正反应为放热反应)达平衡时NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是()
2NO2(正反应为放热反应)达平衡时NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是()
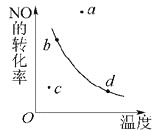
A.a点B.b点C.c点D.d点
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,下列有关说法不正确的是( )
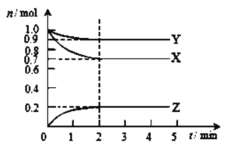
A.该反应的化学方程式为:3X+Y![]() 2Z
2Z
B.反应开始至2min,用Z表示的平均反应速率为:0.05mol·L﹣1·min﹣1
C.混合气体的总质量不随时间的变化而变化,说明反应已达化学平衡状态
D.平衡后X的转化率为30%
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,在水溶液中1molCl-、ClO![]() (x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是( )
(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是( )
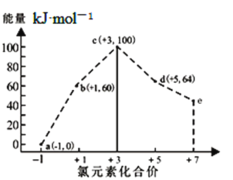
A.a、b、c、d、e中,c最稳定
B.b→a+c反应的活化能为60kJ·mol-1
C.b→a+d反应的热化学方程式为3ClO-(aq)=ClO![]() (aq)+2Cl-(aq)△H=-116kJ·mol-1
(aq)+2Cl-(aq)△H=-116kJ·mol-1
D.e是ClO![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】“84消毒液”广泛应用于杀菌消毒,其有效成分是NaClO。实验小组制备消毒液,并利用其性质探索制备碘水的方法。
资料:i.HClO的电离常数为Ka=4.7×10-8;
H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11。
ii.碘的化合物主要以I-和IO3-的形式存在,IO3-+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I-![]() I3-(I3-低浓度时显黄色,高浓度时为棕色)。
I3-(I3-低浓度时显黄色,高浓度时为棕色)。
Ⅰ.制备消毒液(夹持装置略)
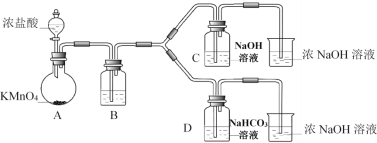
(1)制备NaClO消毒液的装置是__________(填C或D)。
(2)制备完成后,向C装置的溶液中添加NaOH、Na2SiO3等物质,得到与某品牌成份相同的消毒液,用平衡移动原理解释NaOH的作用___________________。
(3)结合资料i,写出D中反应的化学方程式______________________。
Ⅱ.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
方案 | 操作 | 现象 | 反应后加淀粉溶液 |
1 | 烧杯1溶液中加入9gKI固体 | 溶液为橙黄色 | …… |
2 | 烧杯2溶液中加入9gKI固体再加入1mo/L盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
3 | 烧杯3溶液中加入少量KI固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
(4)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是________。
(5)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为IO3-。
设计实验证实了假设1成立。NaClO氧化I2生成IO3-的离子方程式是_____________。
假设2:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设2成立,实验a的操作及现象是______________________。
(6)某小组检验烧杯3所得溶液中含IO3-:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在IO3-,说明理由______________________。
(7)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在固定容积的密闭容器中进行如下反应:2SO2(g)+O2(g)![]() 2SO3(g),已知反应过程中某一刻SO2、O2、SO3浓度分别为0.2mol/L、0.2mol/L、0.2mol/L,达到平衡时浓度可能是( )
2SO3(g),已知反应过程中某一刻SO2、O2、SO3浓度分别为0.2mol/L、0.2mol/L、0.2mol/L,达到平衡时浓度可能是( )
A.SO2、O2分别为0.4mol/L、0.3mol/L
B.O2为0.05mol/L
C.SO2、SO3浓度均为0.15mol/L
D.SO2为0.24mol/L、SO3为0.16mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学反应包括A(g)→B(g)、B(g)→C(g)两步反应,整个反应过程中的能量变化如图所示。下列说法正确的是( )
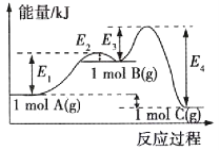
A.两步反应均为吸热反应
B.1mol A(g)的总键能大于1mol C(g)的总键能
C.1mol C(g)与1mol A(g)的能量差为![]()
D.反应A(g)→B(g)一定要加热才能发生
查看答案和解析>>
科目: 来源: 题型:
【题目】将4molA和2molB在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(s)+B(g)2C(g),若经2s后测得C的浓度为0.6mol·L-1,现有下列几种说法:①用物质A表示的反应的平均速率为0.3mol·L-1·s-1②用物质B表示的反应的平均速率为0.6mol·L-1·s-1③2s时物质A的转化率为30%④2s时物质B的浓度为0.7mol·L-1其中正确的是( )
A. ①③B. ①④C. ②③D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】二环[1,0,0]丁烷(![]() )是最简单的桥环化合物。下列关于该化合物的说法错误的是
)是最简单的桥环化合物。下列关于该化合物的说法错误的是
A. 该化合物的二溴代物有4种
B. 生成1molC4H10需要2molH2
C. 该化合物与1,3-丁二烯互为同分异构体
D. 该化合物中4个碳原子可能处于同一平面
查看答案和解析>>
科目: 来源: 题型:
【题目】肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如下图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是:

A. 194 B. 391 C. 516 D. 658
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com