
科目: 来源: 题型:
【题目】如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内的气体是( )
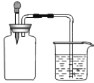
① CO、O2 ② Cl2、CH4 ③ NO2、O2 ④ N2、H2
A.①②B.②C.③④D.②③
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下面的信息,下列叙述正确的是( )
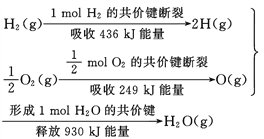
A. 2 mol H2(g)跟 1 mol O2(g)反应生成 2 mol H2O(g)吸收能量为490 kJ
B. 化学反应中能量变化的大小与反应物的质量多少无关
C. 1 mol H2(g) 跟0.5mol O2(g) 反应生成 1 mol H2O(l)释放能量为245 kJ
D. 2molH2O (g)的能量比2 mol H2(g)与1 mol O2(g)的能量之和低
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入lmolCO2和3mo1H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入lmolCO2和3mo1H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是

A. 升高温度平衡常数K增大
B. 反应达到平衡状态时,CO2的平衡转化率为75%
C. 3min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率
D. 从反应开始到平衡,H2的平均反应速率v(H2)=0.075 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,将3 mol A气体和1 mol B气体混合于固定容积为2 L的密闭容器中,发生反应:3A(g)+B(g) ![]() C(g)+2D(s)。2 min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是( )
C(g)+2D(s)。2 min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是( )
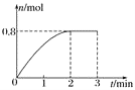
A. 若混合气体的密度不再改变时,该反应不一定达到平衡状态
B. 2 min后,加压会使正反应速率加快,逆反应速率变慢
C. 反应过程中A和B的转化率之比为3∶1
D. 开始到平衡,用A表示的化学反应速率为0.3 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,0.1 mol·L-1的HA溶液中c(OH-)/c(H+)=1×10-8,下列叙述中正确的是( )
A. 0.01 mol·L-1HA的溶液中c(H+)=1×10-4mol·L-1
B. pH=3的HA溶液与pH=11的NaOH溶液等体积混合后所得溶液中c(Na+)>c(A-)>c(OH-)>c(H+)
C. 浓度均为0.1 mol·L-1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(OH-)-c(H+)<c(HA)-c(A-)
D. pH=3的HA溶液与pH=11的NaOH溶液按体积比1:10混合后所得溶液中c(OH-)+c(A-)=c(H+)+c(Na+)
查看答案和解析>>
科目: 来源: 题型:
【题目】将TiO2转化为TiCl4是工业冶炼金属钛的主要反应之一。已知:
TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH=+140.5 kJ·mol-1
C(s,石墨)+O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
则反应TiO2(s)+2Cl2(g)+2C(s,石墨)===TiCl4(l)+2CO(g)的ΔH是
A.-80.5 kJ·mol-1 B.+30.0 kJ·mol-1
C.-30.0 kJ·mol-1 D.+80.5 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是![]()
![]()
A. 氢氧燃料电池工作时,![]() 在负极上失去电子
在负极上失去电子
B. ![]() 溶液加热后,溶液的pH减小
溶液加热后,溶液的pH减小
C. 常温常压下,![]() 中含有的分子数为
中含有的分子数为![]() 个
个
D. 室温下,稀释![]() 溶液,溶液的导电能力增强
溶液,溶液的导电能力增强
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年IUPAC命名117号元素为Ts(中文名“![]() ”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】目前手机屏幕主要由保护玻璃、触控层以及下面的液晶显示屏三部分组成。下面是工业上用丙烯(A)和有机物C(C7H6O3)为原料合成液晶显示器材料(F)的主要流程:

(1)化合物C的官能团名称为____________________。B的结构简式为_____________。
(2)反应①的反应类型为_____________。
(3)写出C与过量NaHCO3水溶液反应的化学方程式______________________________。
(4)下列关于化合物D的说法正确的是__________(填字母)。
A.属于烯烃B.1molD最多能与4molH2发生加成反应
C.一定条件下发生缩聚反应D.核磁共振氢谱有6组峰
(5)满足下列条件下的D的同分异构体有多种,写出2个互为顺反异构的结构简式。顺式结构:_______________,反式结构_______________。
①能发生银镜反应和水解反应②存在手性碳原子
(6)请参照上述制备流程,写出以有机物C、乙烯和![]() 为原料制备
为原料制备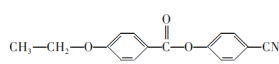 的合成路线流程图(无机试剂任用)___。
的合成路线流程图(无机试剂任用)___。
查看答案和解析>>
科目: 来源: 题型:
【题目】间氯苯甲醛是新型农药、医药等有机合成的中间体,是重要的有机化工产品。实验室制取间氯苯甲醛的过程如下。
Ⅰ.Cl2的制备
舍勒发现氯气的方法至今还用于实验室制备氯气。本实验中利用该方法制备Cl2。
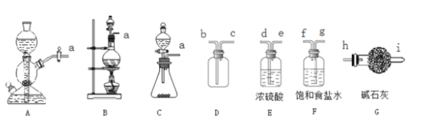
(1)该方法可以选择图中的_____(填字母标号)为Cl2发生装置,反应中氧化剂和还原剂的物质的量之比为_______。
(2)选择图中的装置收集一瓶纯净干燥的Cl2,接口的连接顺序为a→___________(按气流方向,填小写字母标号)
(3)试用平衡移动原理解释用饱和食盐水除去Cl2中混有的HCl的原因:_____________________。
Ⅱ.间氯苯甲醛的制备
反应原理:
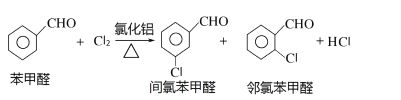
实验装置和流程如图所示:
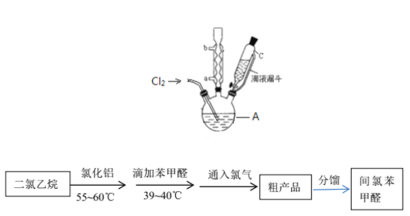
(4)图中仪器A的名称是_____________。
(5)间氯苯甲醛的制备过程中,二氯乙烷的作用是________________________;该实验要求无水操作,理由是____________________________________________;该实验有两次恒温过程,为控制反应温度仪器A处可采用________加热的方法。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com