
科目: 来源: 题型:
【题目】某研究小组同学为探究锌与硫酸反应生成SO2、H2的临界浓度(浓硫酸能与锌反应生成SO2的最低浓度)设计了如下实验。在大试管A中加入100mLl 8mol/L硫酸,向连接在塑料棒上的多孔塑料球内加入足量的锌粒(塑料棒可以上下移动),在试剂瓶D中加入足量的浓NaOH溶液(加热和夹持装置已省略)。

已知:锌与浓硫酸接触,开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。
(1)请写出锌与硫酸反应产生SO2的化学方程式______________。
(2)在组装仪器之后,加入试剂之前必须进行的操作是__________。
(3)长导管B的作用是______,如果没有这个设计,最终测定的临界浓度会_________。(填“偏高”、“偏低"或“无影响”)
(4)装置中干燥管C的作用是_______,请简述如何判断硫酸已达临界浓度________。
(5)反应结束后向D装置中加入足量的H2O2溶液和足量的BaCl2溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a克,则浓硫酸与锌反应的临界浓度为:_________mol/L。(用含a的计算式表示,忽略体积变化)
(6)某同学通过联系氧化还原反应的相关知识,认为也可以利用硫酸酸化的高锰酸钾溶液对D中的SO32-进行滴定,通过滴定出的SO32-的物质的量计算临界浓度,你认为他的这一想法是否可行?________(填“可行”或“不可行”),原因是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,10L密闭容器中加入5.0molSO2、4.5molO2,经10min后反应达到平衡,此时容器中气体的平均分子量为58。请计算(写出计算过程):
(1)10min内SO2的转化率;
(2)容器内反应前与平衡时的压强之比(最简整数比) ;
(3)该温度下的平衡常数。
查看答案和解析>>
科目: 来源: 题型:
【题目】阿比朵尔主要用于甲、乙型流感和其它呼吸道病毒感染症的防治,有专家认为其在新冠肺炎的治疗上也有一定的疗效。阿比朵尔的合成路线如图所示:
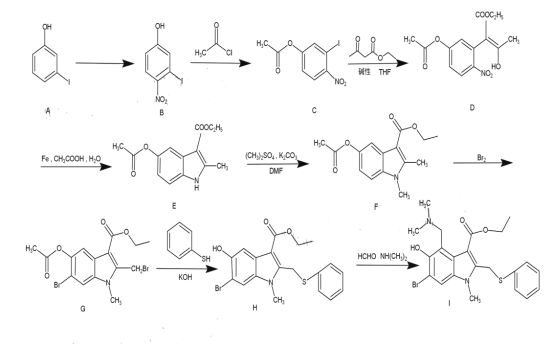
(1)图中I为阿比朵尔,其分子式为__________,
(2) A的名称是__________,G→H的反应类型为___________。
(3) C中所含的含氧官能团的名称为_____________。
(4) F→G的化学方程式为____________。
(5)C有多种同分异构体,写出能同时满足下列条件的芳香化合物的结构简式(不考虑立体异构)_________。
①能与NaHCO3溶液反应放出CO2;②核磁共振氢谱有三组峰,且峰面积的比是1:1:1。
(6)如图为合成阿比朵尔的另一种方法,请参照上述流程将下列流程图补充完整(试剂可从上题试剂中任选):______
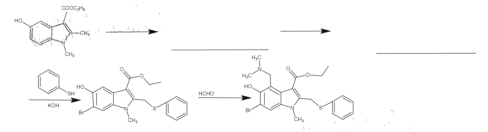
查看答案和解析>>
科目: 来源: 题型:
【题目】“绿色化学实验”进课堂,某化学教师为氯气与金属钠反应设计了如下装置与操作以替代相关的课本实验。实验操作:钠与氯气反应的装置作如下图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是( )
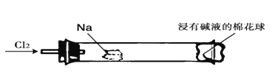
A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
C. 钠着火燃烧产生苍白色火焰
D. 若在棉球外沿滴一滴淀粉碘化钾溶液,据其颜色变化判断氯气是否被碱液完全吸收
查看答案和解析>>
科目: 来源: 题型:
【题目】将2.32gNa2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况) 关系如图所示,下列说法中错误的是( )
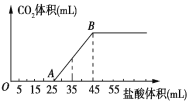
A.OA段发生反应的离子方程式为:H++OH-=H2O、CO32-+H+=HCO3-
B.A点溶液中的溶质为NaCl、NaHCO3
C.混合物中NaOH的质量0.60g
D.当加入35mL盐酸时,产生CO2的体积为224mL
查看答案和解析>>
科目: 来源: 题型:
【题目】2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
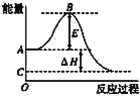
(1)图中A、C分别表示____,___,E的大小对该反应的反应热__(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点___(填“升高”或“降低”),ΔH___(填“变大”“变小”或“不变”)。
(2)图中ΔH=____kJ·mol-1。
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量H2(g)反应,生成NH3(g),放出92.2kJ热量:_____。
②1molCu(s)与适量O2(g)反应,生成CuO(s),放出157kJ热量:_____。
③在25℃、101kPa时,8 g CH4完全燃烧生成液态水时放出的热量是445.15kJ,则CH4燃烧的热化学方程式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的外围电子排布图为____,基态Fe2+中,核外电子占据最高能层的符号是____,Fe2+和Fe3+是铁的两种常见离子,Fe3+的稳定性强于Fe2+,原因是____。
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为_______,SCN—的几何构型为______,中心原子的杂化类型为_______。
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有_________(填写选项字母)
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为_____________。
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=__________g/cm3 (列出计算式),晶体中最近的两个铁离子间的距离为_______pm。
查看答案和解析>>
科目: 来源: 题型:
【题目】向Fe2(SO4)3、CuCl2混和溶液中投入足量的铁粉充分反应后,得到的固体经过滤、干燥、称重,若所得固体的质量与加入的铁粉的质量相等,则原溶液中c(SO42-)与c(Cl-)之比为
A.3︰14B.1︰7C.2︰7D.3︰2
查看答案和解析>>
科目: 来源: 题型:
【题目】GaN凭借其出色的功率性能、频率性能以及散热性能,在光电领域和高频微波器件应用等方面有广阔的前景。
(1) Johnson等人首次在1100℃下用镓与氨气制得氮化镓,该可逆反应每生成1 mol H2放出10.3 kJ热量。该反应的热化学方程式是_____。(己知金属镓的熔点是29.8℃,沸点是2403℃;氮化镓的熔点为1700℃)
(2)在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中NH3的体积分数与压强(p)、温度(T)的关系如图所示(已知图中T1和T2的温度均小于1700℃)。
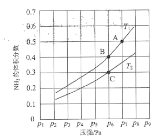
①下列说法正确的是________(填标号)。
a.相同条件下,Ga(OH)3 的碱性比Al(OH)3强
b.当c(NH3)=c(H2)时,一定达到了化学平衡状态
c. A点和C点化学平衡常数的关系是:KA< KC
d.温度一定时,达平衡后再充入氦气(氦气不参与反应),NH3的转化率增大.
②气相平衡中用组分的平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp),已知在T1℃时体系的压强初始压强为a Pa,则B点的Kp=____(用含a表示且保留2位有效数字)。
(3)电解精炼法提纯镓是工业上常用的方法。具体原理如图所示:
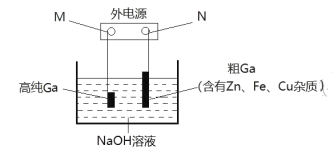
已知:金属的活动性Zn>Ga>Fe>Cu;镓化学性质与铝相似。
①M为电源的_______极,电解精炼镓时产生阳极泥的主要成分是________。
②电解过程中阳极产生的离子迁移到达阴极并在阴极析出高纯镓。请写出电解过程的阴极的电极反应__________。
③电解过程中需控制合适的电压,若电压太高时阴极会产生H2导致电解效率下降。若外电路通过0.2mole时,阴极得到3.5g的镓。则该电解装置的电解效率η=_________(η=生成目标产物消耗的电子数+转移的电子总数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20mL 0.05mol·L-1的某稀酸H2B溶液中滴入0.1mol·L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确的是

A.NaHB溶液可能为酸性,也可能为碱性
B.A、B、 C三点溶液的pH是逐渐减小,D、E、F三点溶液的pH是逐渐增大
C.B点溶液c(NH4+)=2c(B2-)
D.E溶液中离子浓度大小关系:c(NH4 +)> c(B2-)> c(H+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com