
科目: 来源: 题型:
【题目】室温下,用0.1000 mol·L-1 NaOH溶液分别滴定0.1000 mol·L-1 HA~HD酸的滴定曲线如图所示。下列说法不正确的是
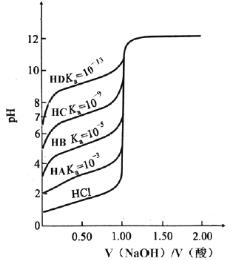
A.等物质的量浓度时,Ka越小滴定突变越不明显,滴定误差越大
B.滴定HC时,滴定终点的pH=7
C.滴定HB时,应该选择酚酞作为指示剂
D.由图像可知在计算HD滴定前溶液pH时不能忽略水的电离
查看答案和解析>>
科目: 来源: 题型:
【题目】主族元素R的最高价氧化物0.112g溶于水后,得到100g碱性溶液,其溶质的质量分数为0.148%,又知该原子核中有20个中子,试经过计算推求R是何元素。____
查看答案和解析>>
科目: 来源: 题型:
【题目】为了讲授“氯气的性质和用途”,一老师以二氧化锰和浓盐酸为主要原料制取氯气,并设计了如图所示装置(其中A是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行教学。
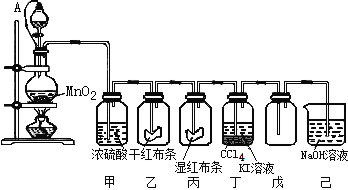
试回答下列问题:
(1)乙和丙中的现象分别是 ____________________、____________________;由上述现象可得出结论:_____________________(写化学式)具有漂白作用;
(2)分离丁中液体的方法是 _______;
(3)圆底烧瓶内发生反应的化学方程式为__________________________________;
(4)分液漏斗与烧瓶连接橡皮管的目的是 __________________________________;
(5)己烧杯中反应的离子方程式为:________________________________________;
(6)将产生的Cl2通入FeCl2溶液中得到含有FeCl2和FeCl3的混合物,实验测得混合物中n(Fe元素)∶n(Cl元素)=1:2.4,则该溶液中Fe2+和Fe3+的物质的量浓度之比约为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知甲酸的分解反应:HCOOHCO+H2O,△H。在H+催化作用下反应历程为:
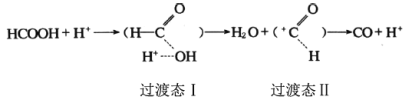
根据过渡态理论,其反应过程中的能量变化如图所示,E1、E2、E3均为大于0。
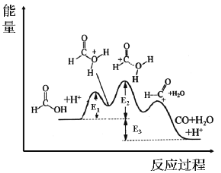
下列说法不正确的是
A.E2为正反应的最高活化能
B.该反应为放热反应,△H=E3
C.图像中第一个峰(过渡态)对应的物质结构为过渡态I
D.使用催化剂后,正逆反应速率同等程度改变,平衡不移动
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,将1 mol X和3 mol Y置于2 L的恒容密闭容器中,发生反应:X(g)+3Y(g)2Z(g),反应过程中部分数据如表所示:
t/min | 0 | 10 | 20 | 30 | 40 |
p/kPa | 32 | 28.8 | 27.2 | 26.88 | 26.88 |
下列说法正确的是
A.10min时,用Y表示的平均反应速率为0.03 mol·L-1·min-1
B.X和Y的转化率之比保持不变时,可判断反应达到平衡状态
C.平衡状态时,c(Z)=0.32 mol·L-1
D.用气体分压代替物质的量浓度计算该反应的平衡常数,数值不变
查看答案和解析>>
科目: 来源: 题型:
【题目】古代炼铜,主要矿物原料是孔雀石 [Cu2(OH)2CO3],燃料是木炭,涉及的反应有:
①Cu2(OH)2CO3 ![]() 2CuO+CO2↑+H2O②2CuO+C
2CuO+CO2↑+H2O②2CuO+C ![]() 2Cu+CO2↑
2Cu+CO2↑
③CuO+CO ![]() Cu+CO2 ④CO2+C
Cu+CO2 ④CO2+C ![]() 2CO
2CO
(1)从四种基本反应类型看:反应①、②、④分别属于:______、________、____________。
(2)在上述反应中,属于氧化还原反应的是 __________________(填序号)。其中这几个反应的氧化剂分别是:____________、___________、______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】学习了元素周期律后,同学们对第四周期过渡元素氧化物产生了浓厚的兴趣。是否只有二氧化锰能催化氯酸钾受热分解?氧化铁、氧化铜、氧化铬等对氯酸钾的受热分解有没有催化作用?对此他们进行了实验探究。请你根据要求完成下列部分实验报告。
(1)实验仪器及试剂:实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、___、___、___等;
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾;
(2)实验步骤:略;
(3)实验数据:
实验编号 | KClO3质量(g) | 氧化物化学式 | 氧化物质量(g) | 氧化物回收率 | 产生气体(mL)(已折算到标况) | 耗时(s) |
1 | 0.60 | 10 | 480 | |||
2 | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
3 | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
4 | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
5 | 0.60 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
(4)实验讨论:
a.在氧化物的回收过程中,要进行过滤操作,所用的玻璃仪器是玻璃棒、____;
b.实验编号3的实验中KClO3的分解率为____%(保留一位小数);
c.在用Cr2O3做研究实验时,发现有黄绿色刺激性气味的气体产生,同时绿色的混合物变成了橘黄色,该刺激性气体是___(填分子式),可用____试纸检验,上述异常现象产生的原因是____;
(5)实验结论:____。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏伽德罗常数的值。下列说法正确的是
A.2C+SiO2![]() 2CO↑十Si,则每生成4.48 L CO时转移电子0.4NA
2CO↑十Si,则每生成4.48 L CO时转移电子0.4NA
B.1 mol NH3完全溶于水,则n(NH3·H2O)+n(NH4+)=l mol
C.氯化铝在气态时以双聚分子存在,其球棍模型为![]() ,则1 mol双聚分子中含有电子数为128NA
,则1 mol双聚分子中含有电子数为128NA
D.2SO2(g)+O2(g)2SO3(l) △H=-a kJ·mol-1(a>0),则每生成2 mol SO3(l)时吸热a kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应3Cl2 + 6NaOH ![]() 5NaCl + NaClO3 + 3H2O,以下叙述正确的是( )
5NaCl + NaClO3 + 3H2O,以下叙述正确的是( )
A.Cl2是氧化剂,NaOH是还原剂
B.被氧化的Cl原子与被还原的Cl原子的个数比为1∶5
C.氧化产物与还原产物的物质的量的比为5∶1
D.每生成1mol的NaClO3转移6mol的电子
查看答案和解析>>
科目: 来源: 题型:
【题目】根据你所学习的元素周期律和周期表知识回答下列相关问题:
(1)现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 单质是一种淡黄色固体,是黑火药成分之一 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(i)元素Y的氢化物的电子式为____,其水溶液呈碱性的原因是(用电离方程式表示):____;
(ii)元素Z与元素T相比,非金属性较强的是___(填元素符号);
(iii)探寻物质的性质差异性是学习的重要方法之一,T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是___(填化学式)。
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质),把与下面元素有关的性质相符的曲线标号填入相应的空格中:
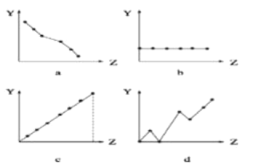
(i)IIA族元素的最外层电子数(填字母)____;
(ii)第三周期元素的最高化合价(填字母)____;
(iii)N3、O2、F、Na、Mg2、Al3的离子半径(填字母)___。
(3)周期表中某些元素化合物的易燃性、毒性变化有一定规律性,例如:
(i)氢化物的易燃性:第二周期___>__>H2O>HF,第三周期SiH4>PH3>___>___(填化学式);
(ii)化合物的毒性:PH3>NH3,H2S___H2O,CS2_CO2(选填“<”、“>”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com