
科目: 来源: 题型:
【题目】根据下图所示实验,回答问题:
(1)实验①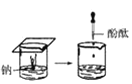 观察到的现象是________________________。实验②
观察到的现象是________________________。实验②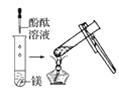 观察到的现象是________________________。
观察到的现象是________________________。
(2)实验③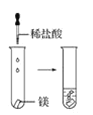 观察到的现象是________________________。实验④
观察到的现象是________________________。实验④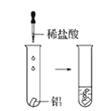 观察到的现象是________________________。
观察到的现象是________________________。
(3)由上述实验,你能得出的结论是________________________。
(4)请总结同周期元素金属性的变化规律__________,并用原子结构解释其原因_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学想通过实验探究硫和碳得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验。

(1)仪器a的名称是________,应盛放下列药品中的________(填字母)。
A.稀硫酸 B.亚硫酸C.氢硫酸 D.盐酸
(2)仪器b的名称是________,应盛放下列药品中的________(填字母)。
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
(3)仪器c中应盛放的试剂是________,如果看到的现象是____________________,证明b中反应产生了________,即可证明________比________酸性强,得电子能力________比________强,b中发生反应的离子方程式为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有①氯化钡、②金刚石、③氯化铵、④硫酸钠、⑤干冰、⑥碘片六种物质,按下列要求回答:
(1)熔化时不需要破坏化学键的是________,熔化时需要破坏共价键的是________,熔点最高的是________,熔点最低的是________。
(2)属于离子化合物的是________,只有离子键的物质是________,以分子间作用力结合的是________。
(3)①的电子式是____________,⑥的电子式是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)反应前A的物质的量浓度是________。
(3)10 s末,生成物D的浓度为________。
(4)A与B的平衡转化率之比为________。
(5)反应过程中容器内气体的平均相对分子质量变化是________(填“增大”、“减小”或“不变”,下同),气体的密度变化是________。
(6)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):①降低温度______;②增大A的浓度________;③恒容下充入氖气_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化铁和摩尔盐是铁的两种重要盐类,在净水和定量分析等方面具有重要作用。
(1) 用FeCl3溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉,对加入铁粉充分反应后的溶液分析合理的是____________。
a. 若无固体剩余,则溶液中一定有Fe3+ b. 若有固体存在,则溶液中一定有Fe2+
c. 若溶液中有Cu2+,则一定没有固体析出 d. 若溶液中有Fe2+,则一定有Cu析出
(2)工业上通过氧化酸性FeCl2废液得到含FeCl3的溶液。若酸性FeCl2废液中 ![]() ,
,![]() ,
,![]() ,则该溶液的
,则该溶液的![]() 约为______(不考虑水的电离和离子的水解)。
约为______(不考虑水的电离和离子的水解)。
(3)摩尔盐 [(NH4)2Fe(SO4)26H2O]在定量分析中常作为基准物质,用来标定重铬酸钾、高锰酸钾等溶液的浓度,在![]() 的该盐的溶液中,离子浓度由大到小的顺序是____________。
的该盐的溶液中,离子浓度由大到小的顺序是____________。
(4)摩尔盐与酸性高锰酸钾发生反应:![]()
a.配平上述离子方程式:(___________)Fe2++(____________)MnO4-+(___________)H+→(_________)Mn2++(__________)Fe3++(___________)H2O
b.已知摩尔盐相对分子质量为![]() ,取摩尔盐产品
,取摩尔盐产品![]() (杂质不与高锰酸钾反应),配成
(杂质不与高锰酸钾反应),配成![]() 溶液,取出
溶液,取出![]() 用
用![]() 溶液滴定,消耗
溶液滴定,消耗![]() 溶液
溶液![]() ,则产品中摩尔盐的质量分数为____________(用小数表示,保留四位小数)。
,则产品中摩尔盐的质量分数为____________(用小数表示,保留四位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)2C(g)。若经2 s时测得C的浓度为0.6 mol·L-1,填写下列空白:
(1)用物质A表示反应的平均速率为_________。
(2)用物质B表示反应的平均速率为_________。
(3)2 s时物质A的转化率为_________。
(4)2 s时物质B的体积分数为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L1·min1,则以物质B表示此反应的化学反应速率为________mol·L1·min1。
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为____________________________。
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) ![]() 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L1·s1,则在2 s时,容器中有______ mol A,此时C的物质的量浓度为________。
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L1·s1,则在2 s时,容器中有______ mol A,此时C的物质的量浓度为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】碱金属元素按原子序数增大,依次为:锂(![]() )、钠(
)、钠(![]() )、钾(
)、钾(![]() )、铷(
)、铷(![]() )、铯(
)、铯(![]() )、钫(
)、钫(![]() ,放射性元素)。请回答:
,放射性元素)。请回答:
(1) 钠钾合金许多特殊反应中有着非常重要的应用。取![]() 钠钾合金和一定量四氯化碳在一定条件下恰好完全反应,制造出
钠钾合金和一定量四氯化碳在一定条件下恰好完全反应,制造出![]() 纳米级金刚石粉末。则该钠钾合金中钠元素和钾元素的质量比为______。
纳米级金刚石粉末。则该钠钾合金中钠元素和钾元素的质量比为______。
(2)将一定量的铝和过氧化钠混合物投入一盛有![]() 蒸馏水的烧杯中,反应终止时得到一澄清溶液,所得溶液的质量比反应前上述三种物质总质量之和减少
蒸馏水的烧杯中,反应终止时得到一澄清溶液,所得溶液的质量比反应前上述三种物质总质量之和减少![]() ,再向所得溶液中滴加
,再向所得溶液中滴加![]() 盐酸直至产生的沉淀刚好溶解,消耗盐酸
盐酸直至产生的沉淀刚好溶解,消耗盐酸![]() 。求原混合物中
。求原混合物中![]() 和
和![]() 各多少克?____、____
各多少克?____、____
(3)一定条件下,![]() 铷与氧气和臭氧的混合气体
铷与氧气和臭氧的混合气体![]() (已折算为标况,且该混合气体对相同状况下氢气的相对密度为20.8)恰好完全反应,得到两种离子化合物
(已折算为标况,且该混合气体对相同状况下氢气的相对密度为20.8)恰好完全反应,得到两种离子化合物![]() 和
和![]() 的固体混合物。
的固体混合物。![]() 和
和![]() 中,阴阳离子个数比均为
中,阴阳离子个数比均为![]() 且均在两种微粒间作用力。已知
且均在两种微粒间作用力。已知![]() 的含氧量为0.3596。推断化合物
的含氧量为0.3596。推断化合物![]() 、
、![]() 的化学式分别为:____________、____________。
的化学式分别为:____________、____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】谷物中脂肪含量虽少,但却是其品质优劣的指标之一。黄玉米中粗脂肪(以亚油酸甘油酯为主)含量测定的实验流程如下:
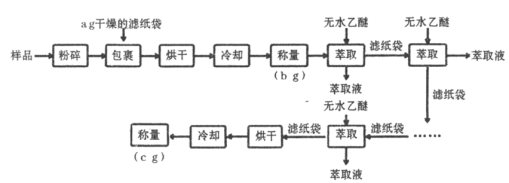
已知:亚油酸甘油酯沸点![]() ;乙醚熔点
;乙醚熔点![]() ,沸点
,沸点![]() ,易燃。
,易燃。
回答下列问题:
(1)实验中两次“冷却”均在干燥器中进行,其目的是____________________。
(2)上述实验中多次“萃取”均在下列____________仪器中进行(填字母标号)。
|
|
|
a | b | c |
(3)为了克服多次萃取实验操作繁琐,萃取剂消耗量过大的缺点, Franz von Soxhlet发明了索氏抽提筒。若将上述实验的多次萃取改为在下图装置中进行(约需10~12h):
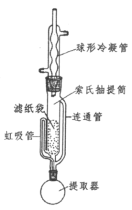
①为提高乙醚蒸气的冷凝效果,球形冷凝管可改用_____________(填仪器名称)。实验中常在冷凝管上口连接一个装有活性炭的球形干燥管,其目的是_______________。
②实验中需控制提取器(烧瓶)温度在60℃~70℃之间,应采取的加热方式是_____________________。
③索氏提取法原理:当无水乙醚加热沸腾后,蒸气通过____________(填字母标号,下同)上升,被冷凝为液体滴入抽提筒中,当液面超过________________________最高处时,萃取液即回流入提取器(烧瓶)中……如此往复。
a.冷凝管 b.虹吸管 c.连通管
④索氏提取法存在的明显缺点是__________________。
(4)数据处理:样品中纯脂肪百分含量_______________(填“<”、“>”或“=”)![]() ,原因是_______________________。
,原因是_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】按照下图所示的操作步骤,完成氢氧化钠与盐酸的反应的实验。

回答下列问题:
(1)反应后混合溶液的温度与反应前盐酸和氢氧化钠溶液的温度相比较其变化是___________________________________。
(2)你认为酸碱中和反应是放热反应还是吸热反应____________________________________。
(3)写出该反应的离子方程式:____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com