
科目: 来源: 题型:
【题目】某同学欲利用浓盐酸、MnO2、Fe等试剂制取无水氯化铁、收集一定量的氯气并验证其某些性质,实验装置如图所示(制气装置省略)。下列说法错误的是

A.④中a导管应向下延伸至接近瓶底
B.若撤去⑥,则⑤中可能有Fe2O3生成
C.当⑤中充满黄绿色气体时再点燃⑤处酒精灯
D.③中试纸若是湿润的,则根据产生的现象可证明氯气有酸性,漂白性
查看答案和解析>>
科目: 来源: 题型:
【题目】某混合气体由一种气态烷烃和一种气态烯烃(含一个双键)组成,在同温同压下,混合气体对氢气的相对密度13,在标准状况下,将56L混合气体通入足量的溴水中,溴水的质量增重35g。
(1)计算确定混合气体中烃的化学式_____。
(2)混合气体中两种烃的物质的量之比_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】李兰娟院士团队在救治感染新型冠状病毒患者过程中,发现达芦那韦对新冠病毒有一定的抑制作用。下列有关该物质的说法正确的是
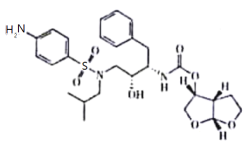
A.含有苯环,属于芳香烃
B.苯环上的一溴代物代物有5种同分异构体
C.1 mol该物质最多能与7 mol H2发生加成反应
D.不能溶于水、酸溶液、碱溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】为了测定乙醇的结构式,利用乙醇和钠的反应,设计如图1装置进行实验,在烧瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积。
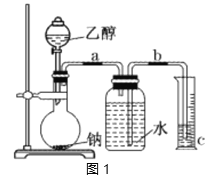
(1)实验前检验该装置的气密性的实验操作是__。
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为__(填“正确”或“不正确”)。
(3)若实验中所用乙醇含有少量水则实验结果将_(填“偏大”或“偏小”),若实验开始前b导管内未充满水则实验结果将__(填“偏大”或“偏小”)。
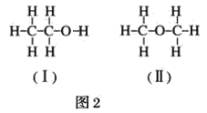
(4)若测得有1.15gC2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280mL,试结合计算和讨论,判断图2中(Ⅰ)和(Ⅱ)两式中,哪个正确__。
查看答案和解析>>
科目: 来源: 题型:
【题目】食品香精菠萝酯的生产路线(反应条件略去)如下:
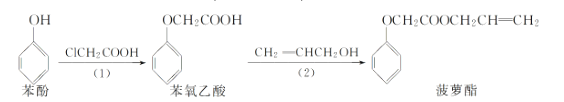
下列叙述错误的是( )
A.步骤(1)产物中残留的苯酚可用![]() 溶液检验
溶液检验
B.苯酚和菠萝酯均可与酸性![]() 溶液发生反应
溶液发生反应
C.苯氧乙酸和菠萝酯均可与![]() 溶液发生反应
溶液发生反应
D.步骤(2)产物中残留的烯丙醇可用溴水检验
查看答案和解析>>
科目: 来源: 题型:
【题目】设![]() 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是
A.![]() 与
与![]() 组成的混合物中,含有的电子数目为
组成的混合物中,含有的电子数目为![]()
B.![]() (标准状况)
(标准状况)![]() 与足量乙烷反应时,断裂的
与足量乙烷反应时,断裂的![]() 键数目为
键数目为![]()
C.![]() 浓度均为
浓度均为![]() 的
的![]() 、
、![]() 溶液中,
溶液中,![]() 数目前者比后者多
数目前者比后者多![]()
D.![]() [电离方程式:
[电离方程式:![]() ]消耗
]消耗![]() 数目最多为
数目最多为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸是一种重要的化工产品,实验室用硝酸氧化淀粉液水解制取草酸的装置如图所示(加热搅拌和仪器固定装置已略去)。
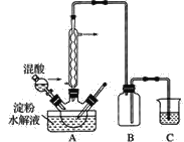
实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中;
②控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO2与98%H2SO4的质量比为2∶1.5)溶液;
③反应3h左右,冷却、抽滤后再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+2HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2↑+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2↑+2NO↑+4H2O
回答下列问题:
(1)检验淀粉是否水解完全所需用的试剂为__。
(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是_。
(3)装置C用于尾气吸收,当尾气中n(NO2)∶n(NO)=1∶1时,过量的NaOH溶液能将NO全部吸收,原因是__(用化学方程式表示)。
(4)与用NaOH溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是什么?__、__。
查看答案和解析>>
科目: 来源: 题型:
【题目】在石蜡油的分解实验中,产物可使酸性高锰酸钾溶液褪色,也可以使溴的四氯化碳溶液褪色。

请你根据实验过程及现象探讨下列问题:
(1)碎瓷片的作用是__。
(2)分解产物中的气体是否都是烷烃__,你的依据是__。
(3)证明石蜡油分解产物中含有碳、氢元素的方法是__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.实验室制备乙烯时,温度计水银球应该插入浓硫酸和无水乙醇的混合液液面以下
B.人体摄入的纤维素可以加快胃肠蠕动,并最终水解为葡萄糖而被吸收
C.![]() 分子中的所有原子有可能共平面
分子中的所有原子有可能共平面
D.溴水中加入苯,充分振荡、静置后,由于发生取代反应而水层几乎呈无色
查看答案和解析>>
科目: 来源: 题型:
【题目】锑(Sb)是第VA族元素,其单质主要用于制造合金、半导体。三氧化二锑俗称锑白,是白色粉末,不溶于水,是一种两性氧化物,主要用于白色颜料、油漆和塑料、石油化工等。某工厂用羽毛矿(主要成分为Pb4FeSb6S14)制取锑白的工艺流程如图所示:

(1)Pb4FeSb6S14中的锑元素只显一种化合价,则其化合价是______。X是一种固体单质,其成分是___(填化学式)。
(2)氯化浸出中,除铅与X外,被氧化的元素反应后均显高价,写出相应的化学方程式:______________。操作1为加水稀释,写出生成SbOCl的离子方程式:___________。
(3)试剂1通常选用氨水而不是NaOH溶液,最可能的原因是_______。操作2的内容是_________、干燥。
(4)在强碱性条件下电解Na3SbS3溶液(原理如图)可得到单质锑。

写出阴极的电极反应式:_______,B电极应接电源的______极,当有2 mol Sb生成时,通过阳离子交换膜的离子数为_________(设NA为阿伏加德罗常数的值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com