
科目: 来源: 题型:
【题目】如图为元素周期表中短周期的一部分,下列说法正确的是
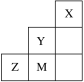
A.电负性:Y>Z>M
B.离子半径:M->Z2->Y-
C.Z和M的最高价含氧酸中非羟基氧原子数分别为2和3
D.Z元素基态原子的轨道表示式为:![]()
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】研究电解质在水溶液中的平衡能了解它的存在形式。
(1)已知部分弱酸的电离常数如下表:
化学式 | HF | H2CO3 | H2S |
电离平衡常数K(25℃) |
|
|
|
①写出H2S的Ka1的表达式:________________。
②常温下,pH相同的三种溶液NaF、Na2CO3、Na2S,物质的量浓度最小的是_______。
③将过量H2S通入Na2CO3溶液,反应的离子方程式是_______________。
(2)室温下,用0.100 mol·L-1 盐酸溶液滴定20.00 mL 0.100 mol·L-1 的氨水溶液,滴定曲线如图所示。(忽略溶液体积的变化,①②填“>”“<”或“=”)
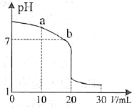
①a点所示的溶液中c(NH3·H2O)___________c(Cl-)。
②b点所示的溶液中c(Cl-)___________c(NH4+)。
③室温下pH=11的氨水与pH=5的NH4Cl溶液中,由水电离出的c(H+)之比为__________。
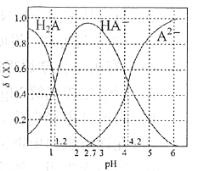
(3)二元弱酸H2A溶液中H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示。则H2A第二级电离平衡常数Ka2=___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于反应Cu+2H2SO4![]() CuSO4+SO2↑+2H2O说法正确的是( )
CuSO4+SO2↑+2H2O说法正确的是( )
A.H2SO4是还原剂B.Cu在反应中被氧化
C.H2SO4在反应中只表现氧化性D.1mol氧化剂在反应中得到1mol电子
查看答案和解析>>
科目: 来源: 题型:
【题目】CuCl为白色粉末,微溶于水,不溶于乙醇,潮湿的CuCl在空气中被氧化为Cu2(OH)3Cl。
(1)一种由海绵铜(Cu)为原料制备CuCl的工艺流程如下:

①“溶解”步骤发生反应的离子方程式为_________________________________;
②潮湿的CuCl在空气中被氧化的化学反应方程式为_________________________________;
③已知常温下Cu(OH)2溶度积常数Ksp=2×10-20要使c(Cu2+)=0.2 mol·L-1的硫酸铜溶液中的铜离子沉淀比较完全(使铜离子浓度变为原来的千分之一)则应调节溶液pH为___________以上。
(2)次磷酸(H3PO2)是一元中强酸,可用于作金属表面处理剂。
①向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,写出反应的化学方程式:_____________;
②H3PO2可将溶液中的Ag+还原为银,从而用于化学镀银,反应同时生成P元素最高价氧化物对应的水化物。在该过程中,氧化剂与还原剂的物质的量之比为:___________;
③NaH2PO2的水溶液呈弱碱性,用离子方程式说明原因:______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | Q | R |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
主要化合价 | +2 | +3 | +6,-2 | +5,-3 | +4,-4 | +1 |
(1)Z在元素周期表中的位置是_________________________。
(2)元素Q和R形成的化合物A是果实催熟剂,用A制备乙醇的化学方程式是_______________________。
(3)单质铜和元素M的最高价氧化物对应水化物的浓溶液发生反应的离子方程式为___________________。
(4)元素X的金属性比元素Y______(填“强”或“弱”)。
(5)元素Q、元素Z的含量影响钢铁性能,采用下图装置A在高温下将钢样中元素Q、元素Z转化为QO2、ZO2。

①气体a的成分是________________(填化学式)。
②若钢样中元素Z以FeZ的形式存在,在A中反应生成ZO2和稳定的黑色氧化物,则反应的化学方程式是_________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将64gCu与一定浓度的HNO3反应,Cu全部反应完后,收集到标准状况下NO和NO2混合气体22.4L。请回答下列问题:
(1)Cu与HNO3反应生成NO的离子方程式为____________________。该反应体现的HNO3的性质为______(填字母)。
A.强氧化性 B.酸性 C.不稳定性 D.易挥发性
(2)参加反应的Cu转移电子的数目为______。
(3)该反应中消耗HNO3的物质的量为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,T表示温度,n表示物质的量)。
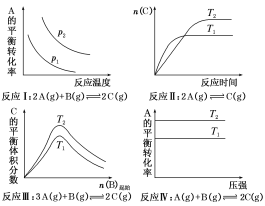
根据以上规律判断,下列结论正确的是( )
A.反应Ⅰ:ΔH>0,p2>p1B.反应Ⅱ:ΔH<0,T1<T2
C.反应Ⅲ:ΔH>0,T2>T1或ΔH<0,T2<T1D.反应Ⅳ:ΔH<0,T2>T1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.FeCl3溶液腐蚀铜线路板:Fe3++Cu=Fe2++Cu2+
B.氯气通入水中:Cl2+H2O=2H++ClO-+Cl-
C.金属铝加入到NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑
D.Na2O加入稀硫酸中:O2-+2H+=H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】工业甲醇的质量分数可以用下列方法测定:
①在稀H2SO4中甲醇被Cr2O72-氧化成CO2和H2O,反应式为:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72-可用Fe2+与之完全反应:___Cr2O72-+__Fe2++__H+—__Cr3++__Fe3++__H2O。现有0.12g工业甲醇,在H2SO4溶液中与25mL0.2mol·L-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1mol·L-1FeSO4与其反应,结果用去FeSO4溶液9.6mL。
(1)配平第②步的离子方程式___。
(2)计算工业甲醇的质量分数___。
(3)工业上通常利用SiO2和碳反应来制取硅,写出反应的化学方程式__。
工业上还可以利用镁制取硅,反应为2Mg+SiO2=2MgO+Si,同时会发生副反应:2Mg+Si=Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
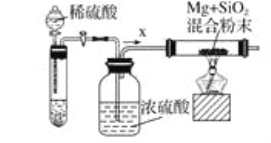
(4)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用__(填序号)。
A.石灰石 B.锌粒 C.纯碱
(5)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是__;当反应引发后,移走酒精灯,反应能继续进行,其原因是__。
(6)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①___,②___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com