
科目: 来源: 题型:
【题目】下列说法或表达正确的是( )
①活性炭、SO2和HClO都具有漂白作用,且漂白原理相同
②向100mL0.1mol/L 的溴化亚铁溶液中通入0.05mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2=2 Fe3++2Br2+6Cl-
③电解精炼铜时,以粗铜作阴极,纯铜作阳极
④钢铁的吸氧腐蚀负极电极反应式 :Fe-3e-=Fe3+
⑤碳酸氢根离子的电离方程式可表示为: HCO3- + H2O![]() H3O++ CO32-
H3O++ CO32-
⑥SiO2 虽是酸性氧化物,但其不溶于水,因此不能与NaOH溶液反应
⑦ CO、SO2、NO、NO2都是对大气产生污染的气体,他们在空气中都能稳定存在
⑧浓硫酸具有脱水性,所以可以做干燥剂
A.②④⑧ B.②⑤ C.③④⑥ D.④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
B.500℃、30M Pa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) ![]() 2NH3(g) ΔH = -38.6 kJ/mol
2NH3(g) ΔH = -38.6 kJ/mol
C.已知热化学方程式:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH = -Q kJ/mol ,若将一定量的SO2(g)和O2(g)置于密闭容器中充分反应后放出热量Q kJ,则此过程中有2 mol SO2(g)被氧化
2SO3(g) ΔH = -Q kJ/mol ,若将一定量的SO2(g)和O2(g)置于密闭容器中充分反应后放出热量Q kJ,则此过程中有2 mol SO2(g)被氧化
D.X(g)+Y(g)![]() Z(g) ΔH >0,恒温恒容条件下达到平衡后加入X,上述反应ΔH增大
Z(g) ΔH >0,恒温恒容条件下达到平衡后加入X,上述反应ΔH增大
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表短周期中六种元素的原子序数与主要化合价的关系如图:
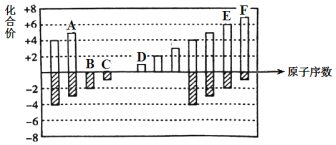
(1)E在元素周期表中的位置是_________。
(2)C、D、F原子半径由大到小的顺序是____________(填元素符号)。
(3)A、B、C的单质与氢气反应剧烈程度由强到弱的顺序____________.(用单质的化学 式表示)。
(4)应用元素周期律和元素周期表的知识,写出D和E形成的化合物的化学式_________、________(写2种)。
(5)判断F的单质和E的最简单氢化物之间能否发生反应,若能则写出反应的化学方程式,若不能则说明理由________
查看答案和解析>>
科目: 来源: 题型:
【题目】植物香料桂皮中含有肉桂醛。
Ⅰ、肉桂醛由C、H、O三种元素组成,质谱分析肉桂醛分子的相对分子质量为132,其分子中碳元素的质量分数为81.8%,肉桂醛的分子式是______,肉桂醛是苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的氢原子,其结构简式是_____(不考虑立体异构)。
Ⅱ、重外化学社某同学设计了如下合成线路图:
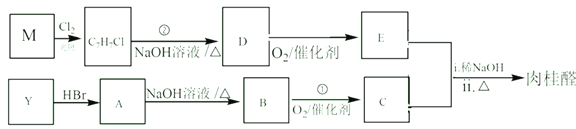
已知: 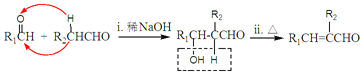
请回答下列问题:
(1)M的名称为 _______ ,D→E的反应类型为______。
(2)Y的结构简式为 _______。
(3)写出反应①的化学方程式____________。
(4)写出满足下列条件的肉桂醛的同分异构体的结构简式________。
① 与肉桂醛含有相同的官能团 ②苯环上的一氯代物有2种
(5)已知:RCH=CH2![]() RCH2CH2OH,请以丙烯和苯甲醛为原料,参照题干信息,合成
RCH2CH2OH,请以丙烯和苯甲醛为原料,参照题干信息,合成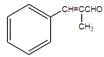 ,写出合成线路图。(合成线路图的表示方法:
,写出合成线路图。(合成线路图的表示方法:![]() )_____。
)_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】具有支链的芳香族化合物是重要的化工原料和合成中间体,以下是由丙烯为原料合成油墨材料DAP-A树脂的流程。
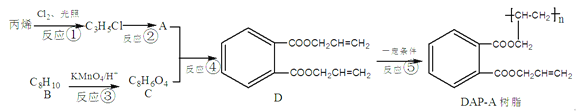
完成下列填空:
(1)D的分子式是____;反应④的条件是_____。
(2)写出结构简式A______;B__________。
(3)写出下列反应的化学方程式。
反应②:________________。
反应④:__________________________。
(4)符合下列条件的C的同分异构体共有___种。
①遇FeCl3溶液显紫色;②能发生银镜反应;③含有-COOH。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组为探究![]() 和
和![]() 的性质,将两种气体同时通入水中,实验装置如图:
的性质,将两种气体同时通入水中,实验装置如图:
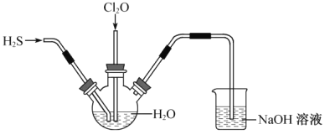
请回答:(1)三颈瓶中出现淡黄色沉淀,溶液呈强酸性,用一个化学方程式表示________。
(2)若通入水中的![]() 已过量,设计实验方案检验________。
已过量,设计实验方案检验________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂废料中含有一定量的单质银。该工厂设计回收单质银的工艺流程如下
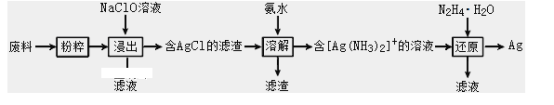
已知: i.NaClO在酸性条件下易分解,且NaClO氧化Ag的效果远强于NaClO3的ii.3NaClO![]() 2NaCl+NaClO3请回答下列问题
2NaCl+NaClO3请回答下列问题
(1)“粉碎”的目的为_____;
(2)“浸出”时,需加入适量NaCl并保持体系为碱性环境,其中需保持体系为碱性环境的原因为___,发生反应的离子方程式为______________;
(3)“浸出”时,所加 NaClO可用_____(填选项字母)代替,但此法的缺点是_______;
a.HNO3 b.NaCl c.Na2S
(4)“溶解”时,发生反应的离子方程式为______________。
(5)“还原”时,N2H4H2O对应的产物为N2.此反应中氧化剂与还原剂的物质的量之比为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)某小组设计了如下图所示的实验装置用于制备ClO2。
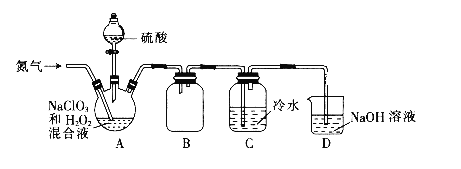
①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是__________。
②装置B的作用是_________。
③当看到装置C中导管液面上升时应进行的操作是________。
(2)用0.1000mol·L-1的Na2S2O3标准液测定装置C中ClO2溶液的浓度。原理:2ClO2+10I-+8H+=5I2+2Cl-+4H2O , I2+2S2O32- = 2I- +S4O62-
①配制0.1000molL-1的Na2S2O3标准溶液时所需仪器除在如图所示的仪器中进行选择外,还需用到的玻璃仪器是________(填仪器名称)
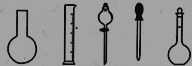
②在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度___0.1000molL-1(填“>”、“<”或“=”,下同);若Na2S2O3标准溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度___0.1000molL-1。
③取10mLC中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入___________作指示剂,测得标准液消耗的体积为20.00mL,通过计算可知C中ClO2溶液的浓度为________ mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如图反应。(图中有些反应的产物和反应条件没有标出)
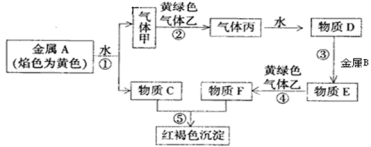
请回答下列问题:
(1)丙的化学式为____。
(2)A的一种氧化物为淡黄色固体,该物质的电子式为___。
(3)写出气体乙与C溶液反应的离子方程式:____。
(4)若将C溶液与E溶液混合,则可以观察到的现象是:____。
(5)配制F溶液时,要将F固体先溶于较浓的盐酸中,再加水稀释,其目的是___(用简单文字和离子方程式说明)。
(6)设计一种检验物质E溶液中金属阳离子实验方案:____(写出实验步骤,现象和结论)。
查看答案和解析>>
科目: 来源: 题型:
【题目】烃A是一种重要的化工原料,A的产量是衡量一个国家的石油化工水平的主要指标。B可发生银镜反应。F为有浓郁香味、不溶于水的油状液体。它们之间的转化关系如图。请回答:
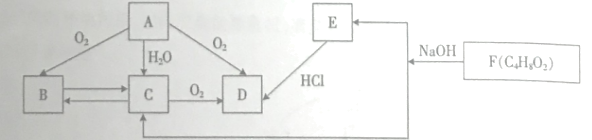
(1)C中含有的官能团名称是_________
(2)A与D也可在一定条件下生成F,该反应的反应类型为_________
(3)A在催化剂、加热条件下转化为B的化学方程式是_________
(4)下列说法正确的是_________
A F与NaOH溶液反应称为皂化反应
B 用新制碱性氢氧化铜悬独液可以区分B、C和D
C 给出氢离子的能力:D>C
D 实验室制备A和F时都需要使用浓硫酸,浓硫酸的作用完全相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com