
科目: 来源: 题型:
【题目】已知2FeSO4![]() Fe2O3+SO2↑+SO3↑。下列有关操作、装置、原理及对现象的表述正确的是
Fe2O3+SO2↑+SO3↑。下列有关操作、装置、原理及对现象的表述正确的是
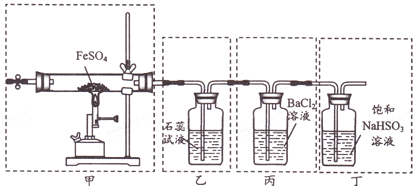
A. 用装置甲高温分解FeSO4,点燃酒精喷灯前应先向装置内通一段时间N2
B. 用装置乙可检验分解产生的SO2,现象是石蕊试液先变红后褪色
C. 用装置丙可检验分解产生的SO3,现象是产生白色沉淀
D. 用装置丁可吸收尾气,避免污染环境
查看答案和解析>>
科目: 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A.向澄清石灰水中通入少量SO2气体:Ca2++SO2=CaSO3↓
B.过量SO2气体通入氢氧化钠溶液中:SO2+OH-=![]()
C.SO2气体通入溴水中:SO2+Br2+H2O=2H++2Br-+![]()
D.向氢硫酸中通入氯气:S2-+Cl2=S↓+2Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的悬浊液中逐滴加入1 mol·L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:

(1)A点→B点反应的离子方程式为_______________________。
(2)原混合物中AlCl3的物质的量为______,NaOH的物质的量为_____。
(3)C点加入的HCl溶液体积为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在500 mL KNO3和Cu(NO3)2的混合溶液中,c(NO3-)=6 mol/L,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是
A. 电解得到的Cu的物质的量为0.5 mol
B. 向电解后的溶液中加入98 g的Cu(OH)2可恢复为原溶液
C. 原混合溶液中c(K+)=4 mol/L
D. 电解后溶液中c(H+)=2 mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】配制960 mL 0.3mol/L NaOH溶液。具体如下:
(1)需称取_________g NaOH。
(2)配制过程中除烧杯、托盘天平、玻璃棒,还需要用到主要玻璃仪器是__________。
(3)下列操作会使配制的溶液浓度偏低的是___________(填字母)。
A、配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体
B、配制氢氧化钠溶液时,容量瓶中有少量水
C、发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度线
D、定容时俯视容量瓶刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】某气态烃0.5mol能与0.5molCl2完全加成,加成产物又可被3molCl2完全取代,则此气态烃可能是
A.CH2=CH2B.CH3-CH=CH2
C.CH2=CHCH2CH3D.CH2=CH-CH=CH2
查看答案和解析>>
科目: 来源: 题型:
【题目】等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加入等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是
A. 甲、乙中都是铝过量 B. 甲中铝过量,乙中碱过量
C. 甲中酸过量,乙中铝过量 D. 甲中酸过量,乙中碱过量
查看答案和解析>>
科目: 来源: 题型:
【题目】透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶。制备它的一种配方中含有下列四种物质:
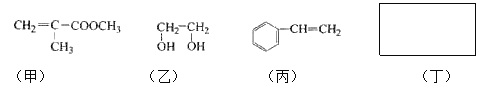
填写下列空白:
(1)甲中不含氧原子的官能团是____________;下列试剂能与甲反应而褪色的是___________(填标号)
a. Br2/CCl4溶液 b.石蕊溶液 c.酸性KMnO4溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:_______
(3)淀粉通过下列转化可以得到乙(其中A—D均为有机物):

A的分子式是___________,试剂X可以是___________。
(4)已知: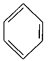 +RCl
+RCl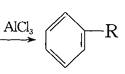 +HCl(-R为烃基)
+HCl(-R为烃基)
 +H2
+H2
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是 ______________ 。
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与FeCl3溶液作用现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为 ___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钛被称为继铁、铝之后的第三金属,请回答下列问题:
(1)金红石(TiO2)是钛的主要矿物之一,基态Ti原子价层电子的排布图为_________,基态O原子电子占据最高能级的电子云轮廓图为 __________形。
(2)以TiO2为原料可制得TiCl4,TiCl4的熔、沸点分别为205K、409K,均高于结构与其相似的CCl4,主要原因是 __________________。
(3)TiCl4可溶于浓盐酸得H2[TiCl6],向溶液中加入NH4Cl浓溶液可析出黄色的(NH4)2[TiCl6]晶体。该晶体中微观粒子之间的作用力有 ________。
A.离子键 B.共价键 C.分子间作用力 D.氢键 E.范德华力
(4)TiCl4可与CH3CH2OH、HCHO、CH3OCH3等有机小分子形成加合物。上述三种小分子中C原子的VSEPR模型不同于其他分子的是 _____,该分子中C的轨道杂化类型为________ 。
(5)TiO2与BaCO3一起熔融可制得钛酸钡。
①BaCO3中阴离子的立体构型为 ________。
②经X射线分析鉴定,钛酸钡的晶胞结构如下图所示(Ti4+、Ba2+均与O2-相接触),则钛酸钡的化学式为 _________。已知晶胞边长为a pm,O2-的半径为b pm,则Ti4+、Ba2+的半径分别为____________pm、___________pm。

查看答案和解析>>
科目: 来源: 题型:
【题目】在373K时,把0.5molN2O4气体通入体积为5L的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol/L。在60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法正确的是( )
A.前2s,以NO2浓度变化表示的平均反应速率为0.005mol·L-1·s-1
B.在2s时,体系内压强为反应前的1.1倍
C.平衡时,体系内含N2O4的物质的量为0.25mol
D.平衡时,若往容器内充入氮气,则可提高N2O4的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com