
科目: 来源: 题型:
【题目】下列反应不属于氧化还原反应的是 ( )
A.3Fe + 4H2O(g) ![]() Fe3O4 + 4H2
Fe3O4 + 4H2
B.3NO2 +H2O = 2HNO3+ NO
C.Ca(OH)2+SO2 = CaSO3 + H2 O
D.Cu+2H2SO4 (浓)![]() CuSO4+SO2↑+ 2H2O
CuSO4+SO2↑+ 2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】将 4molA气体和3molB气体在2L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)![]() 2C(g),若经 2s后测得C的浓度为 0.6molL-1,现有下列几种说法:
2C(g),若经 2s后测得C的浓度为 0.6molL-1,现有下列几种说法:
①用物质A 表示反应的平均速率为 0.3molL-1s-1
②物质 B的体积分数是40%
③2s 时物质 A 的转化率为30%
④2s 时物质 B 的浓度为 1.0molL-1
其中正确的是( )
A. ①④ B. ①③ C. ②③ D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应3A(g)![]() 3B(?)+C(?) △H>0达到化学平衡后,
3B(?)+C(?) △H>0达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
a.若B、C都是气体,气体的平均相对分子质量①___;
b.若B、C都不是气体,气体的平均相对分子质量②____;
c.若B是气体,C不是气体,气体的平均相对分子质量③___;
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是④___态,C是⑤___态。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,验证取代反应时,反应需用水浴加热的原因是_____;观察到________现象时,表明溴乙烷与NaOH溶液已完全反应。
(2)有机物A的分子式为C3H8O,它能氧化成B也能与浓硫酸共热生成C。若B不能发生银镜反应,C不能使溴水褪色。B含有的官能团名称为__________,C结构简式为:_____________。
(3)DAP是电器和仪表部件中常用的一种高分子材料,其结构如图:
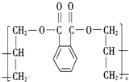
则合成它的单体是________(填序号)。
①邻苯二甲酸 ②丙烯 ③丙烯酸 ④邻苯二甲醇 ⑤丙烯醇
(4)![]() 的名称是(用系统命名法命名)_____________________。
的名称是(用系统命名法命名)_____________________。
(5)写出![]() 与足量溴水反应的化学方程式________。
与足量溴水反应的化学方程式________。
(6)写出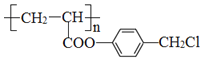 与足量NaOH溶液反应的化学方程式_____。
与足量NaOH溶液反应的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,水作为还原剂的是( )
A.2F2 + 2H2O = 4HF + O2B.Na2O + H2O = NaOH
C.Br2 + H2O ![]() HBr + HBrOD.2Na + 2H2O = 2NaOH + H2↑
HBr + HBrOD.2Na + 2H2O = 2NaOH + H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g)+Y(g)![]() 3Z(g)△H<0反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。
3Z(g)△H<0反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。

下列推断正确的是
A.升高温度,平衡常数增大
B.W点X的正反应速率等于M点X的正反应速率
C.Q点时,Y的转化率最大
D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
查看答案和解析>>
科目: 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)俗称保险粉,易被氧气氧化。利用如图装置,在锥形瓶中加入HCOONa、NaOH、CH3OH和水形成的混合液,通入SO2时发生反应生成保险粉和一种常见气体,下列说法错误的是
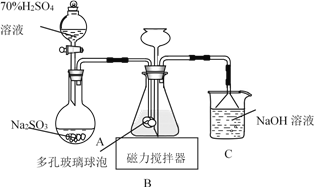
A. 制备保险粉的离子方程式为HCOO-+OH-+2SO2===S2O42-+CO2↑+H2O
B. NaOH溶液的主要作用是吸收逸出的CO2
C. 多孔玻璃球泡的作用是增大气体与溶液的接触面积,使SO2能被充分吸收
D. 为避免产生的Na2S2O4被O2氧化,使硫酸与亚硫酸钠先反应,产生的SO2排出装置中残留的O2
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下图所示:
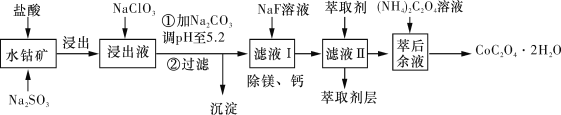
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)浸出过程中加入Na2SO3的主要目的是_______________________。
(2)向浸出液中加入NaClO3的离子反应方程式:_____________________。
(3)已知:常温下NH3·H2O![]() NH4++OH- Kb=1.8×10-5
NH4++OH- Kb=1.8×10-5
H2C2O4![]() H++HC2O4- Ka1=5.4×10-2
H++HC2O4- Ka1=5.4×10-2
HC2O4-![]() H++C2O42- Ka2=5.4×10-5
H++C2O42- Ka2=5.4×10-5
则该流程中所用(NH4)2C2O4溶液的pH____7 (填“>”或“<”或“=”)。
(4)加入(NH4)2C2O4溶液后析出晶体,再过滤、洗涤,洗涤时可选试剂_____(填字母代号)。
A.蒸馏水 B.自来水 C.饱和的(NH4)2C2O4溶液 D.稀盐酸
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,萃取剂的作用是除去锰离子,其使用的适宜pH范围是_________(填字母代号)。
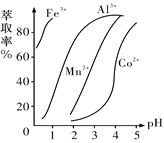
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
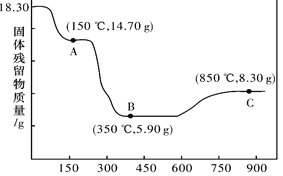
(6)CoC2O4·2H2O热分解质量变化过程如图所示。其中600℃以前是隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物;C点所示产物的化学式是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于各装置图的叙述不正确的是
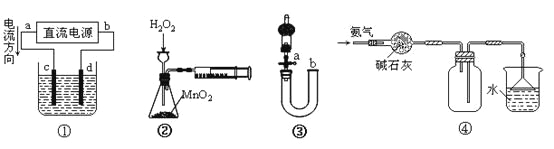
A.装置①中,c为阳极,d为阴极
B.装置②可定量测定H2O2的分解速率
C.关闭活塞a,从b处加水,可以检查装置③的气密性
D.装置④可用于收集并吸收多余的氨气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com