
科目: 来源: 题型:
【题目】在中和热测定的实验中,以下操作正确的是:( )
①只在大烧杯底部垫泡沫塑料,使放入的小烧杯杯口与大烧杯杯口相平,再盖上硬纸板
②温度计测量过盐酸的温度后,立即插入![]() 溶液中测量
溶液中测量![]() 溶液的温度
溶液的温度
③将量筒中的![]() 溶液慢慢加入到小烧杯的盐酸中,边加边搅拌
溶液慢慢加入到小烧杯的盐酸中,边加边搅拌
④读取混合溶液的最高温度和最低温度,以其平均值记为最终温度.
A.只有①正确B.只有②正确
C.只有①④正确D.都不正确
查看答案和解析>>
科目: 来源: 题型:
【题目】用下列实验装置完成对应的实验,能达到实验目的的是( )
A. 制取并收集乙炔
制取并收集乙炔
B.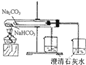 比较NaHCO3、Na2CO3的热稳定性
比较NaHCO3、Na2CO3的热稳定性
C.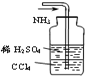 吸收多余的NH3
吸收多余的NH3
D.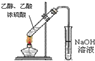 实验室中制取少量乙酸乙酯
实验室中制取少量乙酸乙酯
查看答案和解析>>
科目: 来源: 题型:
【题目】已知氨气可与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置(省略夹持装置及加热装置)可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是 ( )
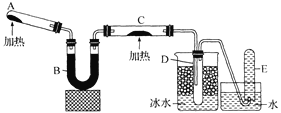
A.试管A中加入的试剂为NH4Cl固体
B.反应中氧化剂和还原剂的物质的量之比为2 : 3
C.装置B中加入的物质可以是碱石灰或无水氯化钙
D.装置D中液体可以使干燥的红色石蕊试纸变蓝
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是中学化学中常见物质间的转化关系,其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B为常见的能产生温室效应的气体;E是最简单的有机物,且标准状况下密度为0.714g·L-1。乙和丁为黑色固体,将它们混合后加热发现固体由黑变红。
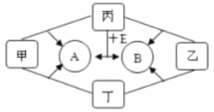
(1)写出化学式:乙___;丙___;
(2)丁的摩尔质量__;
(3)写出丙和E反应生成A和B的化学方程式___;
(4)有同学将乙和丁混合加热后收集到的标准状态下气体8.96L,测得该气体是氢气密度的16倍,若将气体通入足量澄清石灰水,得到白色沉淀物___g;
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.明矾溶于水产生Al(OH)3胶体,离子方程式可表示为:Al3++3H2O=Al(OH)3↓+3H+
B.![]() 和CO2反应生成可降解聚合物
和CO2反应生成可降解聚合物![]() ,该反应符合绿色化学的原则
,该反应符合绿色化学的原则
C.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度
D.聚氯乙烯塑料制品可用于食品的包装
查看答案和解析>>
科目: 来源: 题型:
【题目】通过以下反应可获得新型能源二甲醚(CH3OCH3)。下列说法不正确的是( )
①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=akJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=bkJ·mol-1
③CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH3=ckJ·mol-1
④2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH4=dkJ·mol-1
A.反应①、②为反应③提供原料气
B.反应③使用催化剂,ΔH3减小
C.反应CH3OH(g)=![]() CH3OCH3(g)+
CH3OCH3(g)+![]() H2O(l)的ΔH<
H2O(l)的ΔH<![]() kJ·mol-1
kJ·mol-1
D.反应2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g)的ΔH=(2b+2c+d)kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO2和3molH2。在500℃下发生发应,CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
CH3OH(g)+H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
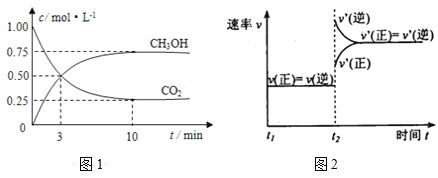
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=________。
(2)500℃该反应的平衡常数为_____(结果保留一位小数),图2是改变温度时化学反应速率随时间变化的示意图,若提高温度到800℃进行,达平衡时,K值_____(填“增大”“减小”或“不变”)。
(3)下列措施中不能使CO2的转化率增大的是_______。
A 在原容器中再充入1mol H2 B 在原容器中再充入1molCO2
C 缩小容器的容积 D 使用更有效的催化剂 E 将水蒸气从体系中分离出
(4)500℃条件下,测得某时刻,CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0.5mol/L,则此时v(正)____ v(逆)(填“>”“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】取某浓度的NaOH溶液10mL,向其中通入一定量的CO2,再向所得溶液中逐滴加入![]() 的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,请回答:
的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,请回答:
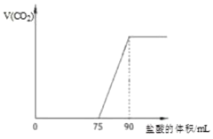
(1)原NaOH溶液的物质的量浓度为__mol·L-1;
(2)原NaOH溶液通入CO2后,所得溶液中的溶质为(写化学式)__;其物质的量之比为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:CH3CH2CH2CH2OH![]() CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
物质 | 沸点/℃ | 密度 / gcm-3 | 水中溶解性 |
|
正丁醇 | 117.2 | 0.8109 | 微溶 | |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是
A.为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B.当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
C.反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D.向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
查看答案和解析>>
科目: 来源: 题型:
【题目】在3个体积均为1 L的恒容密闭容器中发生反应:SO2(g)+2NO(g)![]() 2NO2(g)+S(s)。改变容器I的反应温度,平衡时c(NO2)与温度的关系如图所示。下列说法正确的是( )
2NO2(g)+S(s)。改变容器I的反应温度,平衡时c(NO2)与温度的关系如图所示。下列说法正确的是( )
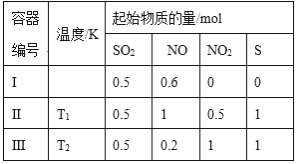
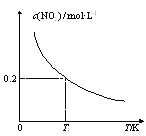
A.该反应的ΔH>0
B.T1时,该反应的平衡常数为![]()
C.容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比大于1:2
D.若T2<T1,达到平衡时,容器Ⅲ中NO的体积分数大于40%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com