
科目: 来源: 题型:
【题目】酸奶中含有乳酸,乳酸在常温常压下是一种黏度很大的液体。取9.0g乳酸与足量的Na反应,在标准状况下收集到2.24L气体;另取9.0g乳酸与足量的NaHCO3溶液反应,生成的CO2气体在标准状况下的体积为2.24L。已知乳酸分子中含有一个甲基,请回答:
(1)乳酸的相对分子质量为___________________。
(2)乳酸与NaHCO3溶液反应的化学方程式为___________________。
(3)在浓硫酸存在下,两分子乳酸相互反应生成环状酯类化合物,则环状酯的结构简式为_________
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由软锰矿浆(主要成分是MnO2)吸收含硫废渣产生的废气制备,工艺如下图所示。
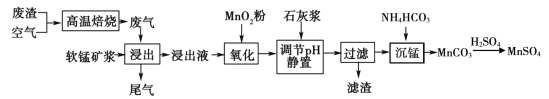
已知:浸出液的pH <2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。请回答下列问题:
(l)高温焙烧前需将矿石研成粉末,其目的是____。
(2)“氧化”中添加适量的MnO2的作用是____(用离子方程式表示);写出“沉锰”的离子方程式____。
(3)下列各组试剂中,能准确测定尾气中SO2含量的是____。(填编号)
a NaOH溶液、酚酞试液
b 稀H2SO4酸化的KMnO4溶液
c 碘水、淀粉溶液
d 氨水、酚酞试液
(4)滤渣的主要成分有____。
(5)若要从MnSO4溶液中得到高纯硫酸锰必须进行的实验操作顺序是____(用字母填空)。
a 过滤洗涤 b 蒸发浓缩 c 冷却结晶 d 干燥
(6)已知:![]() pH =7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10 -6mol/L),需调节溶液pH范围为____
pH =7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10 -6mol/L),需调节溶液pH范围为____
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2O=H++OH-,下列叙述正确的是( )
A.![]() 表示的粒子不会对水的电离平衡产生影响
表示的粒子不会对水的电离平衡产生影响
B.![]() 表示的物质加入水中,促进水的电离,c(H+)增大
表示的物质加入水中,促进水的电离,c(H+)增大
C.25℃时,CH3COO-加入水中,促进水的电离,Kw不变
D.水的电离程度只与温度有关,温度越高,电离程度越大
查看答案和解析>>
科目: 来源: 题型:
【题目】将![]() gNa和
gNa和![]() gAl同时加入到足量的水中充分反应,将反应后的溶液稀释、定容为
gAl同时加入到足量的水中充分反应,将反应后的溶液稀释、定容为![]() 下列说法正确的是
下列说法正确的是![]()
A.反应中放出的气体在标准状况下的体积为![]()
B.参加反应的水的质量与加入Al的质量相等
C.所得溶液中![]() 和
和![]() 的物质的量之比为2:1
的物质的量之比为2:1
D.所得溶液中阳离子和阴离子的物质的量之比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将一定量的氨基甲酸铵置于密闭真空容器中(固体体积忽略不计)发生反应:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是( )
2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是( )
A. 混合气体的平均相对分子质量不再变化时表明达到平衡状态
B. 达到新平衡时,△H为原来的2倍
C. 上述反应达到新平衡状态时x=2a
D. 上述反应体系中,压缩容器体积过程中n(H2NCOONH4)不变
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机物的说法错误的是( )
A.植物油分子结构中含有碳碳双键
B.现有乙烯、丙烯的混合气体共14 g,其原子数为3NA
C.同温同压下,等质量的乙炔和苯完全燃烧耗氧量相同
D.分子式为C5H10O2与碳酸氢钠溶液反应产生气体的有机物有3种
查看答案和解析>>
科目: 来源: 题型:
【题目】锗(![]() )在自然界中非常分散,几乎没有比较集中的锗矿,因此被人们称为“稀散金属”。砷(
)在自然界中非常分散,几乎没有比较集中的锗矿,因此被人们称为“稀散金属”。砷(![]() )是第四周期VA族元素,可以形成
)是第四周期VA族元素,可以形成![]() 、
、![]() 、
、![]() 等化合物,用途广泛。完成下列填空:
等化合物,用途广泛。完成下列填空:
(1)已知锗元素与碳位于同一主族,与钙位于同一周期。
写出锗在周期表中的位置:____________。
根据锗在元素周期表中的位置写出锗的一条用途____________。
(2)将![]() 溶于浓盐酸,可以得到
溶于浓盐酸,可以得到![]() ,其沸点为
,其沸点为![]() 。
。
推测![]() 的晶体类型为______。
的晶体类型为______。
已知![]() 沸点高于
沸点高于![]() ,请从结构角度解释原因:____________。
,请从结构角度解释原因:____________。
将![]() 与
与![]() 作用可以得到
作用可以得到![]() ,
,![]() 水溶液呈______性(填“酸”“碱”或“中”)。
水溶液呈______性(填“酸”“碱”或“中”)。
(3)锗金属对人类具有保健功能,适宜人体接触佩戴。锗金属非常脆,容易破碎,一种常用的方法是将锗制成颗粒镶嵌到其他金属上,但存在易脱落的缺点。请提出一种改进建议:____________。
(4)砷原子核外有______个电子层,最外层有______个电子;比较溴、砷最高价氧化物对应水化物酸性的强弱:____________强于____________(填物质的化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】设![]() 代表阿伏加德罗常数,下列说法正确的是
代表阿伏加德罗常数,下列说法正确的是 ![]()
![]()
A.![]() 中,生成
中,生成![]() 标准状况
标准状况![]() 转移电子数为
转移电子数为![]()
B.56gFe与一定量的稀硝酸反应,转移电子数可能为![]()
C.足量的![]() 与一定量的浓盐酸反应得到
与一定量的浓盐酸反应得到![]() ,若向反应后的溶液中加入足量的
,若向反应后的溶液中加入足量的![]() ,则生成AgCl的物质的量为2mol
,则生成AgCl的物质的量为2mol
D.标准状况下,![]() 和
和![]() 混合后,原子总数小于
混合后,原子总数小于![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
(实验目的)制取乙酸乙酯。
(实验原理)甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,浓硫酸的作用是_________、_________。
(装置设计)甲、乙、丙三位同学分别设计了下列三套实验装置:
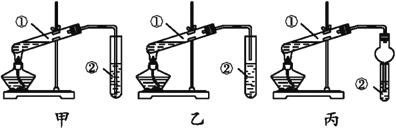
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是____(填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是_________。
(实验步骤)
(1)按选择的装置组装仪器,在试管中先加入3 mL乙醇和2 mL冰醋酸,并在摇动下缓缓加入2 mL的浓硫酸;
(2)将试管固定在铁架台上;
(3)在试管②中加入适量的饱和Na2CO3溶液;
(4)用酒精灯对试管①加热;
(5)当观察到试管②中有明显现象时停止实验。
(问题讨论)
a.按步骤(1)装好实验装置,加入样品前还应检查__________;
b.根据试管②中观察到的现象,可知乙酸乙酯的物理性质有_________;
c.试管②中饱和Na2CO3溶液的作用是________、________、________;
d.从试管②中分离出乙酸乙酯的实验操作是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】FeCl3(aq)与KSCN(aq)混合时存在下列平衡: Fe3+(aq)+SCN-(aq) Fe(SCN)2+(aq)。已知平衡时,c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是
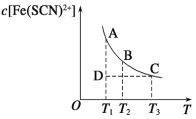
A.FeCl3(aq)与KSCN(aq)的反应是放热反应
B.T1、T2时反应的平衡常数分别为K1、K2,则K1<K2
C.反应处于D点时,一定有υ正<υ逆
D.恒温下加入KCl固体,平衡逆向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com