
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列判断正确的是( )
A.0.1mol H2和0.1mol I2在密闭容器中充分反应后,其分子总数为0.2NA
B.30g乙烷(C2H6)含有共价键总数为6NA
C.1L 1mol·L-1的(NH4)2SO4溶液中含有的NH4+数目为2NA
D.常温下,将2.7g铝片投入过量浓硝酸中充分反应转移电子数为0.3NA
查看答案和解析>>
科目: 来源: 题型:
【题目】用如图所示装置探究Cl2和NO2在NaOH溶液中的反应,若通入适当比例的Cl2和NO2,即发生反应Cl2+2NO2+4NaOH=2NaNO3+2NaCl+2H2O。
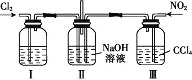
下列叙述正确的是
A. 实验室中用二氧化锰与3 mol·L-1的盐酸共热制备氯气
B. 装置Ⅰ中盛放的试剂是浓硫酸,作用是干燥氯气
C. 装置Ⅲ的作用是便于控制通入NO2的量
D. 若制备的NO2中含有NO,应将混合气体通入水中以除去NO
查看答案和解析>>
科目: 来源: 题型:
【题目】砷酸(H3AsO4)是三元弱酸,剧毒,可用于制备颜料、砷酸盐、杀虫剂等。常温下,其溶液中含砷的各微粒的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与pH的关系如图所示。在常温下,下列说法错误的是
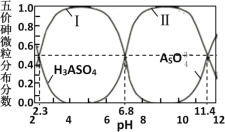
A.曲线Ⅱ代表HAsO![]() 的分布分数
的分布分数
B.该砷酸溶液:Ka2/Ka3=104.6
C.等物质的量浓度的H3AsO4溶液和NaOH溶液等体积混合后所得溶液:pH>7
D.0.1mol/L的Na2HAsO4溶液中: c(HAsO![]() )> c(H2AsO
)> c(H2AsO![]() )> c(AsO
)> c(AsO![]() )
)
查看答案和解析>>
科目: 来源: 题型:
【题目】乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计以下两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯(沸点77.2℃)。下列说法不正确的是
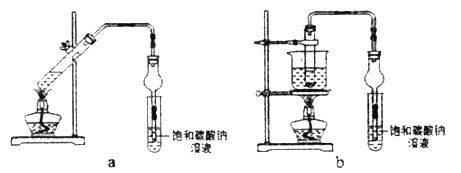
A. 浓硫酸能加快酯化反应速率 B. 不断蒸出酯,会降低其产率
C. 装置b比装置a原料损失的少 D. 可用分液的方法分离出乙酸乙酯
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积可变的密闭容器中充入2mol苯蒸气和4mol氢气,恒温T1和恒压P1条件下进行如下反应:![]() △H1= -208.8kJ· mol-1,达平衡时容器的体积为2L,苯的转化率为50%。下列有关说法正确的是( )
△H1= -208.8kJ· mol-1,达平衡时容器的体积为2L,苯的转化率为50%。下列有关说法正确的是( )
A.苯蒸气的体积分数不再变化时,说明该反应己达平衡状态
B.反应体系中气体总浓度保持不变,说明该反应己达平衡状态
C.在原平衡基础上,再向容器中充入3mol苯蒸气,平衡逆向移动
D.在原平衡基础上,升高温度,苯的转化率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电板上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是
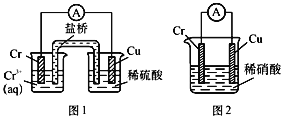
A. 图1为原电池装置,盐桥中的阴离子移向Cu电极的烧杯中
B. 由实验现象可知:金属活动性Cu>Cr
C. 图2装置中Cu电极上发生的电极反应式为:Cu-2e-=Cu2+
D. 两个装置中,电子均由Cr电极流向Cu电极
查看答案和解析>>
科目: 来源: 题型:
【题目】CPAE是蜂胶的主要活性成分,它可由咖啡酸合成,其合成过程如下。下列说法不正确的是
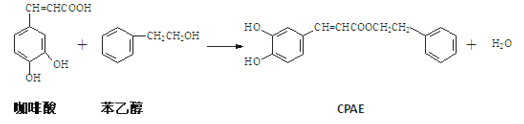
A. 咖啡酸的分子式为C9H8O4
B. 咖啡酸可发生加聚反应,并且所得聚合分子中含有3种官能团
C. 1 mol CPAE与足量的NaOH溶液反应,最多消耗3molNaOH
D. 1 mol CPAE与足量H2反应,最多消耗7 mol H2
查看答案和解析>>
科目: 来源: 题型:
【题目】锂-空气电池的装置示意图如下,以金属锂作电极,从空气中获得O2。下列说法正确的是( )
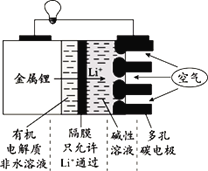
A.锂作负极,电极反应式为:Li-e-+OH-=LiOH
B.若隔膜被腐蚀,不会影响该电池正常使用
C.多孔碳电极上发生的电极反应为:O2+2H2O+4e-=4OH-
D.应用该电池电镀铜,若析出64g Cu,理论上消耗22.4L O2
查看答案和解析>>
科目: 来源: 题型:
【题目】同温同压下,三个等体积的干燥圆底烧瓶中分别充满①HCl;②NO2;③体积比为4:1的NO2和O2,进行喷泉实验。经充分反应后烧瓶内溶质的物质的量浓度之比为( )
A.1:1:1B.4:4:5C.5:5:4D.15:10:12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com