
科目: 来源: 题型:
【题目】不同条件下,用O2氧化a mol/L FeCl2溶液过程中所 测的实验数据如图所示。下列分析或推测合理的是
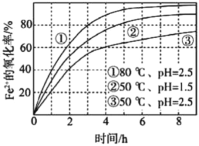
A.由①、②可知,pH越大,+2价铁越易被氧化
B.由②、③推测,若pH>7,+2价铁更难被还原
C.由①、③推测,FeCl2被O2氧化的反应为放热反应
D.60℃、pH=2.5时,4 h内Fe2+的平均消耗速率大于0.15a mol/(L·h)
查看答案和解析>>
科目: 来源: 题型:
【题目】现有单质A、B、C及化合物D、E、F、G、H,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。
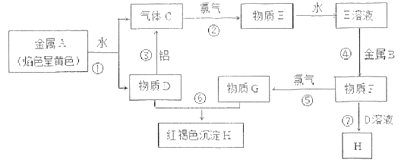
请根据以上信息回答下列问题:
(1)反应③是D物质的水溶液与金属铝反应,金属铝被氧化___(写化学式);
(2)步骤⑦中刚生成的白色沉淀颜色会迅速发生变化,最终生成红褐色沉淀H,请写出由白色沉淀变成H的化学方程式:___;
(3)检验G中所含的金属离子时,在G溶液中加入硫氰化钾溶液,离子方程式为:___;
(4)工业上将氯气通入D溶液中制取消毒液,反应的化学方程式为___,1mol氯气发生反应,转移电子___mol;消毒液中的有效成分是___(填名称);
(5)将0.1molA的碳酸盐溶液和0.15molE溶液混合,有如下两种方式:
A.将含A的碳酸盐溶液逐滴加入到E溶液中;
B.将E溶液逐滴加入到含A的碳酸盐溶液中;
理论上产生气体比较多的是___(填序号),多___mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】某固体中可能含有K+、NH4+、Mg2+、Fe3+、Ba2+、Cu2+、Cl-、SO42-、HCO3-中的几种,填写下列空白:
(1)将该固体溶于水后得无色澄清溶液,由此现象得出该固体中一定不存在的离子是___;
(2)将所得无色澄清溶液进行检测,实验步骤及现象如图:

图中实验中得到的两种气体分别是___、___;白色沉淀成分是___ (填化学式);加入足量盐酸生成气体的离子方程式为___;该固体中可能存在的离子是___;
(3)通过以上检测,下列说法正确的是___
A.该固体中可能含有(NH4)2SO4、KHCO3
B.该固体中可能含有K2SO4、NH4HCO3,一定不含KCl
C.该固体中可能含有(NH4)2SO4、KCl,一定不含KHCO3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列判断正确的是(NA表示阿伏加德罗常数)( )
A.常温c(OH-)/c(H+)=10-13的溶液中可能含有K+、Fe2+、NO3-、Cl-四种离子
B.1 L 0.1molL-1的CH3COONa溶液中CH3COO-和OH-的总数大于0.1NA
C.电子工业上用30%的氯化铁溶液腐蚀敷在印刷线路板上的铜箔:Fe3+ +Cu = Fe2++Cu2+
D.H2的燃烧热为a kJ·mol-1,H2燃烧热的热化学方程式为:O2(g) +2H2(g) = 2H2O(l) ΔH = -2a kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列属于酯化反应的是( )
A.CH4 + Cl2 ![]() CH3Cl + HCl
CH3Cl + HCl
B.CH2 = CH2 + Br2![]() CH2BrCH2Br
CH2BrCH2Br
C.nCH2 = CH2 ![]()
![]()
D.CH3CH2OH + CH3COOH ![]() CH3COOCH2CH3 + H2O
CH3COOCH2CH3 + H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列浓度关系正确的是
A.0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全:c (NH4+)>c (OH-)>c (SO42-)>c (H+)
B.0.1 mol/L的KOH溶液中通入标准状况下的CO2气体3.36 L,所得溶液中:c (K+)+c (H+)=c (CO32-)+c (HCO3-)+c (OH-)
C.0.1 mol/L的NaOH溶液与0.2 mol/L的HCN溶液等体积混合,所得溶液呈碱性:c (HCN)>c (Na+)>c (CN-)>c (OH-)>c (H+)
D.pH相同的NaOH溶液、CH3COONa溶液、Na2CO3溶液、NaHCO3溶液的浓度:c (NaOH)<c (CH3COONa)<c (NaHCO3)<c (Na2CO3)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
A.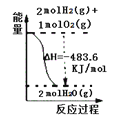 表示 H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ·mol-1
表示 H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ·mol-1
B.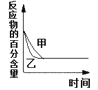 表示压强对可逆反应2A(g) + 2B(g)
表示压强对可逆反应2A(g) + 2B(g)![]() 3C(g) + D(s)的影响,乙的压强比甲的压强大
3C(g) + D(s)的影响,乙的压强比甲的压强大
C.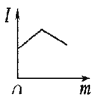 表示在一定温度下,向氢氧化钡溶液中滴入硫酸溶液至过量时,溶液的导电性即电流强度(I)随加入硫酸溶液的量(m)的变化曲线
表示在一定温度下,向氢氧化钡溶液中滴入硫酸溶液至过量时,溶液的导电性即电流强度(I)随加入硫酸溶液的量(m)的变化曲线
D. 表示某可逆反应的反应速率随时间的变化关系,t0时刻改变的条件可能是使用了催化剂
表示某可逆反应的反应速率随时间的变化关系,t0时刻改变的条件可能是使用了催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】相对分子质量不超过100的有机物A,既能与金属钠反应产生无色气体,又能与碳酸钠反应产生无色气体,还可以使溴的四氯化碳溶液褪色。 A完全燃烧只生成CO2和H2O。经分析其含氧元素的质量分数为37.21%。经核磁共振检测发现A的氢谱如下:

(1)A的分子式为___________________________________;
(2)A的结构简式为:___________________________________;
(3)A是否存在顺反异构?___________(填“是”或“否”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】合理应用和处理含氮的化合物,在生产、生活中有重要意义。回答下列问题:
(1)在紫外光照射的条件下,氯气与偏二甲肼[(CH3)2NNH2]可快速反应,偏二甲肼转化为CH3OH和N2,该反应的化学方程式为______________________________。
(2)连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。25℃时,连二次硝酸的电离常数Ka1=6.17×10-8,Ka2=2.88×10-12
①25℃时0.1molL-1NaHN2O2溶液中离子浓度由大到小的顺序为____________________________。
②25℃时向0.1 molL-1连二次硝酸溶液中逐滴滴入NaOH溶液,当溶液的pH=10时,C(N2O22-)/ C(H2N2O2)=________。
(3)亚硝酰氯可由NO与Cl2反应制得,反应原理为2NO(g)+ Cl2 (g)![]() 2C1NO(g)。按投料比n(NO):n(Cl2) =2:1把NO和Cl2充入一恒压的密闭容器中发生上述反应,NO的平衡转化率与温度T的关系如图所示:
2C1NO(g)。按投料比n(NO):n(Cl2) =2:1把NO和Cl2充入一恒压的密闭容器中发生上述反应,NO的平衡转化率与温度T的关系如图所示:
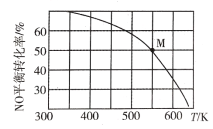
①该反应的△H_____(填“>”“<”或“=”)0。
②M点时容器内NO的体积分数为____。
③若反应一直保持在P压强条件下进行,则M点的平衡常数Kp=____________,(用含P的表达式表示)。
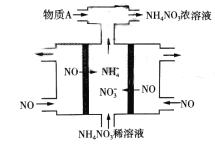
(4)工业上电解NO制备NH4NO3可以变废为宝,其工作原理如图所示、电解时阳极反应式为___________,为使电解产物全部转化为NH4NO3,需要补充物质A,物质A化学式为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上常用水蒸气蒸馏的方法(蒸馏装置如图)从植物组织中获取挥发性成分。这些挥发性成分的混合物统称精油,大都具有令人愉快的香味。从柠檬、橙子和柚子等水果的果皮中提取的精油90%以上是柠檬烯。提取柠檬烯的实验操作步骤如下:柠檬烯![]()
①将12个橙子皮剪成细碎的碎片,投人乙装置中,加入约30mL水,
②松开活塞K。加热水蒸气发生器至水沸腾,活塞K的支管口有大量水蒸气冒出时旋紧, 打开冷凝水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上有一层很薄的油层。下列说法不正确的是
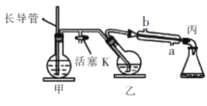
A.当馏出液无明显油珠,澄清透明时,说明蒸馏完成
B.为达到实验目的,应将甲中的长导管换成温度计
C.蒸馏结束后,先把乙中的导气管从溶液中移出,再停止加热
D.要得到纯精油,还需要用到以下分离提纯方法:分馏、蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com