
科目: 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置如图所示。下列说法中,错误的是( )。

A.燃料电池中通入氢气一端的多孔电极为负极
B.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4 OH-
C.该燃料电池的总反应式为:2H2+O2=2H2O
D.乙装置可实现将电能转化为化学能
查看答案和解析>>
科目: 来源: 题型:
【题目】芳香化合物A(C9H9O3Br)可以发生如图所示的转化,合成两种重要的高分子化合物G和H(其他产物和水已略去)。

已知A遇氯化铁溶液显紫色,请回答下列问题:
(1)B的结构简式为____________,其核磁共振氢谱图显示有______种不同环境的氢原子。
(2)D的名称是________________;C和E生成H的反应类型为 _______________
(3)1molA与足量NaOH 溶液充分反应,消耗NaOH的物质的量为____________
(4)C生成D的化学方程式为________________________
(5)W是B的同系物,比B多一个碳原子, 符合下列条件的W的同分异构体有______种。
①遇氯化铁溶液显紫色
②既能发生水解反应又能发生银镜反应
(6)参照上述合成路线,根据信息,以乙醇为原料(无机试剂任选)设计制备 的合成路线_______________
的合成路线_______________
ⅰ.![]()
![]()
![]() +H2O(R1、R2为烃基或氢)
+H2O(R1、R2为烃基或氢)
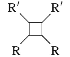
ⅱ.R-HC![]() CH-R'
CH-R'![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】根据反应:2Ag+ + Cu = Cu2+ + 2Ag,设计如图所示原电池,下列说法错误的是( )。

A.X可以是银或石墨
B.Y是硫酸铜溶液
C.电子从铜电极经外电路流向X电极
D.X极上的电极反应式为Ag+ + e-= Ag
查看答案和解析>>
科目: 来源: 题型:
【题目】砷化镓是继硅之后研究最深人、应用最广泛的半导体材料。回答下列问题:
(1)Ga基态原子核外电子排布式为________________,As基态原子核外有__________个未成对电子。
(2)Ga、As、Se的第一电离能由大到小的顺序是__________,Ga、As、Se的电负性由大到小的顺序是__________________。
(3)比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因:________,GaF的熔点超过1000℃,可能的原因是__________________________。
(4)二水合草酸镓的结构如图1所示,其中镓原子的配位数为__________,草酸根离子中碳原子的杂化轨道类型为__________。
(5)砷化镓的立方晶胞结构如图2所示,晶胞参数为a=0.565nm,砷化镓晶体的密度为__________g·cm-3(设NA为阿伏加德罗常数的值,列出计算式即可)。

查看答案和解析>>
科目: 来源: 题型:
【题目】碳、氮、硫的化合物在生产生活中广泛存在。请回答:
(1)以CO2与NH3为原料可合成化肥尿素[CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-l59.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) ΔH=-160.5 kJ·mol-1
③H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出CO2与NH3合成尿素和气态水的热化学反应方程式____________。
(2)T1温度时在容积为2L的恒容密闭容器中只充入1.00molNO2气体发生反应:2NO(g)+O2(g)![]() 2NO2(g) H<0。实验测得:v正=k正c2(NO)·c(O2),v逆=k逆c2(NO2),
2NO2(g) H<0。实验测得:v正=k正c2(NO)·c(O2),v逆=k逆c2(NO2),
k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO2)如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
①从0~2s该反应的平均速率v(NO2)=___________。
②T1温度时化学平衡常数K=___________mol-1·L。
③化学平衡常数K与速率常数k正、k逆的数学关系是K=___________。若将容器的温度改变为T2时其k正=k逆,则T1__________T2 (填“>”、“<”或“=”)。
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是____________________(写出主要反应的离子方程式),该溶液中,c(Na+)______2c(SO32-)+c(HSO3-)(填“>”“<”或“=”)。
②在某NaHSO3、Na2SO3混合溶液中HSO3-、SO32-物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO32-的第一步水解平衡常数=________。

查看答案和解析>>
科目: 来源: 题型:
【题目】下列用来表示物质变化的化学用语错误的是( )。
A.氢氧燃料电池在碱性介质中的正极反应式:O2 + 2H2O + 4e-= 4 OH-
B.用惰性电极电解饱和氯化钠溶液的离子方程式为:2C1一+ 2H2O = H2↑+ Cl2↑+ 2OH-
C.钢铁发生电化学腐蚀的负极反应式:Fe - 3e- = Fe3+
D.粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu2+ + 2e-= Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】关于如图所示的原电池,下列说法正确的是( )。

A.锌是电池负极,发生还原反应
B.电子从铜电极通过电流计流向锌电极
C.盐桥中的阳离子向硫酸铜溶液中迁移
D.实验过程中取出盐桥,原电池仍继续工作
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关常数表达式的正确的是( )。
A.NH3·H2O ![]() NH4+ + OH-Ka =
NH4+ + OH-Ka =
B.CH3CH2COO - + H2O![]() CH3CH2COOH +OH- Kh =
CH3CH2COOH +OH- Kh = 
C.AgCl(s) ![]() Ag+(aq)+Cl-(aq) Ksp = c(Ag+)c(Cl-)
Ag+(aq)+Cl-(aq) Ksp = c(Ag+)c(Cl-)
D.FeO(s)+CO(g) ![]() Fe(s)+CO2(g) K =
Fe(s)+CO2(g) K =![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:pOH=-lgc(OH-)。室温下,将稀盐酸滴加到某一元碱(BOH)溶液中,测得混合溶液的pOH 与微粒浓度的变化关系如图所示。 下列说法错误的是( )

A.若向0.1mol/L BOH溶液中加水稀释,则溶液中c(OH-)/c(BOH) 增大
B.室温下,BOH的电离平衡常数K = 1×10-4.8
C.P点所示的溶液中:c(Cl-) > c(B+)
D.N点所示的溶液中: c(H+) = c(Cl-) + c(OH-) - c(BOH)
查看答案和解析>>
科目: 来源: 题型:
【题目】图甲是一种利用微生物将废水中的尿素(CO(NH2)2)转化为环境友好物质的原电池装置示意图甲,利用该电池在图乙装置中的铁上镀铜。下列说法正确的是( )

A.图乙中Fe电极应与图甲中Y相连接
B.图甲中H+透过质子交换膜由右向左移动
C.图甲中M电极反应式:CO(NH2)2 +5H2O -14e = CO2+2NO2+14H+
D.当图甲中N电极消耗0.5 mol O2时,图乙中阴极增重64g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com