
科目: 来源: 题型:
【题目】不同元素的原子在分子内吸引电子的能力大小可用一数值x来表示,若x越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。下面是某些短周期元素的x值:

(1)通过分析x值的变化规律,确定N、Mg的x值范围: ____<x(N)<_____;_____<x(Mg)<_____。
(2)推测x值与原子半径的关系是_______________________________。
(3)某有机物结构式为C6H5SONH2,在S—N中,你认为共用电子对偏向谁?__________(写原子名称)。
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键的类型是____________。
(5)预测元素周期表中,x值最小的元素位置____________________(放射性元素除外)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。
(查阅资料)
物质 | BaSO4 | BaCO3 | AgI | AgCl |
溶解度/g(20℃) | 2.4×10-4 | 1.4×10-3 | 3.0×10-7 | 1.5×10-4 |
(实验探究)
(一)探究BaCO3和BaSO4之间的转化,实验操作如下所示:
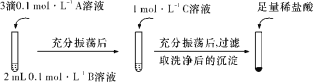
试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
实验Ⅰ | ||||
实验Ⅱ | BaCl2 | |||
Na2CO3 | Na2SO4 | …… | ||
Na2SO4 | 有少量气泡产生,沉淀部分溶解 |
(1)实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入稀盐酸后,__________。
(2)实验Ⅱ中加入稀盐酸后发生反应的离子方程式是_________。
(3)实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:___________。
(二)探究AgCl和AgI之间的转化。
(4)实验Ⅲ:证明AgCl转化为AgI。
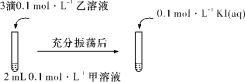
甲溶液可以是______(填字母代号)。
a AgNO3溶液 b NaCl溶液 c KI溶液
(5)实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
装置 | 步骤 | 电压表读数 |
| ||
ⅰ.按图连接装置并加入试剂,闭合K | a | |
ⅱ.向B中滴入AgNO3(aq),至沉淀完全 | b | |
ⅲ.再向B中投入一定量NaCl(s) | c | |
ⅳ.重复ⅰ,再向B中加入与ⅲ等量的NaCl(s) | a |
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
①查阅有关资料可知,Ag+可氧化I-,但AgNO3溶液与KI溶液混合总是得到AgI沉淀,原因是氧化还原反应速率__________(填“大于”或“小于”)沉淀反应速率。设计(-)石墨(s)[I-(aq)//Ag+(aq)]石墨(s)(+)原电池(使用盐桥阻断Ag+与I-的相互接触)如上图所示,则该原电池总反应的离子方程式为________。
②结合信息,解释实验Ⅳ中b<a的原因:__________。
③实验Ⅳ的现象能说明AgI转化为
(实验结论)溶解度小的沉淀容易转化为溶解度更小的沉淀,反之则不易;溶解度差别越大,由溶解度小的沉淀转化溶解度较大的沉淀越难实现。
查看答案和解析>>
科目: 来源: 题型:
【题目】世界能源消费的90%以上依靠化学技术。请回答下列问题:
(1)质子交换膜燃料电池中作为燃料的H2通常来自水煤气。
已知:C(s)+![]() O2(g)=CO(g)ΔH1=-110.35kJ·mol-1
O2(g)=CO(g)ΔH1=-110.35kJ·mol-1
2H2(g)+O2(g)=2H2O(l)ΔH2=-571.6kJ·mol-1
H2O(l)=H2O(g)ΔH3=+44.0kJ·mol-1
①则反应C(s)+H2O(g)![]() CO(g)+H2(g) ΔH4=__________。
CO(g)+H2(g) ΔH4=__________。
②某实验小组在实验室模拟反应C(s)+H2O(g)CO(g)+H2(g),其平衡常数表达式为K=_______。一定温度下,在2L盛有足量炭粉的恒容密闭容器(固体所占体积忽略不计)中通入0.8molH2O,6min时生成0.7gH2,则6min内以CO表示的平均反应速率为________(保留3位有效数字)。
(2)燃料气(流速为1800mL·min-1;体积分数为50%H2,0.98%CO,1.64%O2,47.38%N2)中的CO会使电极催化剂中毒,使用CuO/CeO2催化剂可使CO优先氧化而脱除。
①160℃、CuO/CeO2作催化剂时,CO优先氧化的化学方程式为__________。
②CeO2可由草酸铈[Ce2(C2O4)3]隔绝空气灼烧制得,同时生成两种气体,则发生反应的化学方程式为____________。
③在CuO/CeO2催化剂中加入不同的酸(HIO3或H3PO4),测得燃料气中CO优先氧化的转化率随温度的变化如下图所示。
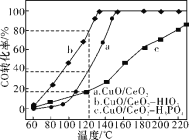
加入________(填酸的化学式)的CuO/CeO2催化剂催化性能最好。温度为120℃,催化剂为CuO/CeO2HIO3时,反应0.5h后CO的体积为______mL。
(3)LiOH是制备锂离子电池正极材料的重要原料,采用惰性电极电解制备LiOH的装置如下图所示。
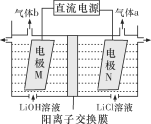
①通电后,Li+通过阳离子交换膜向________(填“M”或“N”)极区迁移。
②电极N产生的气体a通入淀粉-KI溶液,溶液变蓝,持续一段时间后,蓝色可逐渐褪去。据此写出电极N的电极反应式:___________;蓝色逐渐褪去是因为溶液中逐渐生成HIO3,写出此反应的化学方程式:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:

(1)已知在反应①、②中均生成相同的气体分子,该气体具有漂白性。请分别写出反应①、②的化学方程式是___________________、__________________。
(2)基态铜原子的核外电子排布式为________,硫、氧元素相比,第一电离能较大的是________。
(3)反应①和②生成的气体分子的中心原子的杂化类型是________,分子的空间构型是________。
(4)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体,请解释加入乙醇后析出晶体的原因_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法正确的是( )
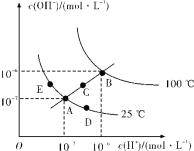
A.图中五点Kw间的关系:B>C>A=D=E
B.若从A点到D点,可采用在水中加入少量NaOH的方法
C.若从A点到C点,可采用温度不变时在水中加入适量H2SO4的方法
D.100℃时,将pH=2的硫酸溶液与pH=12的KOH溶液等体积混合后,溶液显中性
查看答案和解析>>
科目: 来源: 题型:
【题目】现有短周期主族元素X、Y、Z、R、T,R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T型化合物能破坏水的电离平衡,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是( )
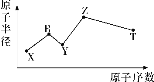
A.原子半径和离子半径均满足:Y<Z
B.简单氢化物的沸点和热稳定性均满足:Y>T
C.最高价氧化物对应的水化物的酸性:T<R
D.常温下,0.1mol·L-1由X、Y、Z、T四种元素组成的化合物的水溶液的pH一定大于1
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有_______(填序号,以下同),含有金属离子的物质是__,分子间可形成氢键的物质是________,属于离子晶体的是__,属于原子晶体的是__,①~⑤五种物质的熔点由高到低的顺序是__。
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__。
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.__;B.__;C.__D.____。
.
查看答案和解析>>
科目: 来源: 题型:
【题目】Z是一种常见的工业原料,实验室制备Z的化学方程式如下图所示。下列说法正确的是( )
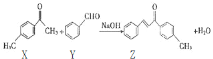
A.1molZ最多能与7molH2反应
B.Z分子中的所有原子一定共平面
C.可以用酸性KMnO4溶液鉴别X和Y
D.X的同分异构体中含有苯环和醛基的结构有14种(不考虑立体异构)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中,正确的是( )
A.一定条件下,将2gH2与足量的N2混合,充分反应后转移的电子数为2NA
B.1mol![]() 与足量水反应,最终水溶液中18O数为2NA(忽略气体的溶解)
与足量水反应,最终水溶液中18O数为2NA(忽略气体的溶解)
C.常温下,46gNO2和N2O4组成的混合气体中所含有的分子数为NA
D.100mL12mol·L-1的浓HNO3与过量Cu反应,转移的电子数大于0.6NA
查看答案和解析>>
科目: 来源: 题型:
【题目】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物:

下列说法正确的是( )
A.正四面体烷的分子式为C4H8B.正四面体烷二氯取代产物有1种
C.环辛四烯核磁共振氢谱有2组峰D.环辛四烯与苯互为同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com