
科目: 来源: 题型:
【题目】某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
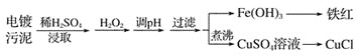
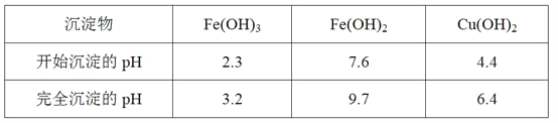
(1)酸浸后加入H2O2的目的是__,调pH的最适宜范围为__。
(2)调pH过程中加入的试剂最好是__。
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
(3)煮沸CuSO4溶液的原因是__。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式__。
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是__。
(5)称取所制备的CuCl样品0.2500g置于一定量的0.5mol﹒L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol﹒L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数___。
查看答案和解析>>
科目: 来源: 题型:
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药I(C31H34O6)的合成路线如图:
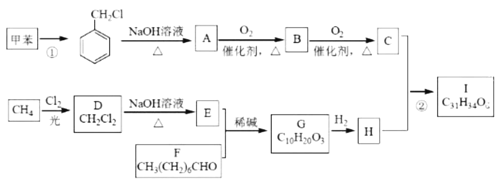
已知: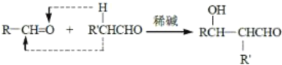 、
、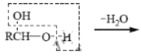 RCHO
RCHO
回答下列问题:
(1)②的反应类型是___。
(2)G的结构简式为___。
(3)①写出A→B的化学方程式为___。
②写出E和新制氢氧化铜溶液反应的化学方程式___。
③写出B与银氨溶液反应的离子方程式___。
(4)若某化合物W的相对分子质量比化合物C大14,且满足下列条件,则W的可能结构有___种。
①遇到FeCl3溶液显色 ②属于芳香族化合物 ③能发生银镜反应
查看答案和解析>>
科目: 来源: 题型:
【题目】烃是由C、H元素组成的有机物、不同有机物的结构不同。试回答下列问题:
(1)分子式为C6H12的某烯烃的所有的碳原子都在同一个平面上,则该烯烃的结构式___,系统命名为___。
(2)组成符合CnH2n-2的某种烃,分子结构中没有支链或侧链,它完全燃烧时所消耗的氧气的体积是相同状态下该烃蒸气体积的8.5倍。
(a)若该烃为链状烯烃,并且与等物质的量的Br2加成只能得到某单一产物,则该烃的结构简式为___。
(b)若该烃只能与含等物质的量的Br2四氯化碳溶液发生反应,则其结构简式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某大理石(含Fe2O3)转化为氯化钙水合物储热材料和高纯度的碳酸钙,无论从经济效益还是资源综合利用都具有重要意义。其工艺流程示意图如下。
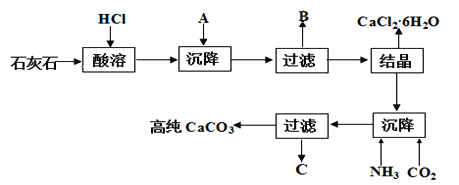
完成下列填空:
(1)上述流程中A是_________(填化学式,下同)、写出B中的成分___________。
(2)C可以作化肥,写出检验C中含有NH4+的方法:________。
(3)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是_____。
a 无毒
b 能导电
c 易溶于水
d 熔点较低(29℃熔化)
![]() CaCl2·6H2O
CaCl2·6H2O
(4)经过热重分析测得:CaCl2·6H2O在焙烧过程中,固体质量的减少值(纵坐标)随温度变化的曲线如图所示。则第一个相对稳定的物质的化学式是______。
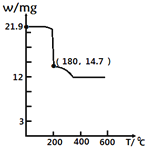
a CaCl2·4H2O
b CaCl2·2H2O
c CaCl2·H2O
d CaCl2
(5)工业还可以利用氨碱法的母液生产氯化钙。根据如图溶解度曲线,设计从含CaCl241%的饱和食盐水中,获得氯化钙水合物的流程______。
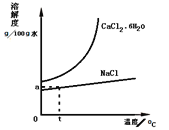
(流程示意:![]() )
)
查看答案和解析>>
科目: 来源: 题型:
【题目】海水是一种丰富的资源,工业生产可以从海水中提取许多有用的物质,这些物质广泛应用于生活、生产、科技等方面。下图是从含碘CCl4溶液得到碘的实验过程:
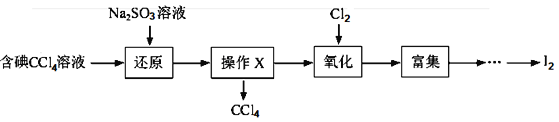
完成下列填空:
(1)向含碘溶液中加入稍过量的Na2SO3溶液,其离子方程式为_________;该操作将I2还原为I-的目的是__________。
(2)操作X的名称为_______,所用的主要仪器是_________。
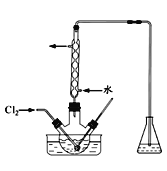
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在400C左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是_________;锥形瓶里盛放的溶液为________。
(4)已知:5SO32-+2IO3-+2H+ → I2+5SO42-+H2O某含碘溶液(pH约为8)中一定存在I2,可能存在I-、IO3—中的一种或两种。请补充完整检验含碘溶液中是否同时含有I-、IO3-的实验方案:_______。实验中可供选择的试剂:CCl4、稀盐酸、淀粉溶液
(5)浓海水提取镁的工艺流程如下图:
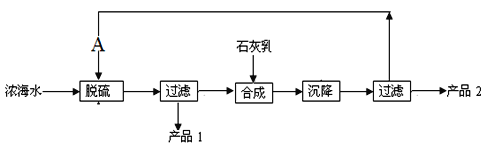
浓海水的主要成分如下:
离子 | Na+ | Mg2+ | Cl- | SO42- |
浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
该工艺过程中,脱硫阶段主要反应的离子方程式为________,产品2的化学式为__________。1L浓海水最多可得到产品2的质量为____g。
查看答案和解析>>
科目: 来源: 题型:
【题目】氨气常用作合成氯氨类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2C1、NHCl2和NCl3),副产物少于其它水消毒剂。
回答下列问题:
(1)工业上可利用反应Cl2(g)+NH3(g)=NH2Cl(l)+HCl(g)制备一氯胺,已知部分化学键的键能如下表所示(假设不同物质中同种化学键的键能相同),则该反应的△H=___kJ/mol。
化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
键能(kJ/mol) | 391.3 | 243.0 | 191.2 | 431.8 |
一氯胺是重要的水消毒剂,其原因是由于一氯胺在中性、酸性环境中会发生完全水解,生成具有强烈杀菌消毒作用的物质,该水解反应的化学方程式为___。
(2)用Cl2和NH3反应制备二氯胺的方程式为2Cl2(g)+NH3(g)![]() NHCl2(g)+2HCl(g)。在恒温条件下,3molCl2和1molNH3发生反应,测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示:
NHCl2(g)+2HCl(g)。在恒温条件下,3molCl2和1molNH3发生反应,测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示:
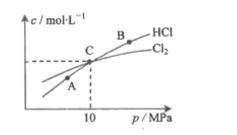
①A、B、C三点中Cl2转化率最高的是___点(填“A”“B”或“C")。
②计算C点时该反应的压强平衡常数Kp(C)=____(Kp是平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(3)我国研制出非贵金属镍钼基高效电催化剂,实现电解富尿素废水低能耗制H2(装置如图),总反应为:CO(NH2)2+H2O![]() 3H2↑+N2↑+CO2↑。
3H2↑+N2↑+CO2↑。
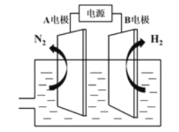
①A电极连接电源的___极(填"正”或“负”)。
②A电极的电极反应为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.中国科学家制得一种蓝色钨的氧化物(WOa ),其中钨的质量分数为 0.7985。
(1)a=______(保留2位小数)。
(2)WOa中存在五价和六价两种价态的钨。则蓝色钨的氧化物中这两种价态的钨原子数之比为________。
II.将铁锰的钨酸盐[(Fe,Mn)WO4]碱熔,发生如下反应(设空气中N2、O2的体积分数分别为0.8和0.2):
4FeWO4+4 Na2CO3+ O2![]() 4 Na2WO4+ 2Fe2O3+ 4CO2 ①
4 Na2WO4+ 2Fe2O3+ 4CO2 ①
2MnWO4+2Na2CO3+ O2![]() 2 Na2WO4+ 2MnO2+ 2CO2 ②
2 Na2WO4+ 2MnO2+ 2CO2 ②
(1)根据反应①,若反应前空气为100L,反应后气体为160L(气体体积在同温同压下测定),则反应后所得气体中CO2的体积分数为_________。
(2)某工厂投料550 mol Na2CO3制备Na2WO4,每反应1mol O2时,气体就增加1.5mol,则生成物中Fe2O3与MnO2的物质的量之比为_________;若反应后气体增加300 mol,制得Na2WO4_____mol。
III.由Na2WO4制备W的第一步反应为:Na2WO4+2HCl→H2WO4↓+2NaCl。往1L密度为1.190g /cm3的37%的浓盐酸加入6.030 mol Na2WO4,恰好完全反应。将产生的沉淀过滤后,溶液中溶质只有NaCl,求该溶液中NaCl的质量分数(25℃时NaCl的溶解度为36.0 g/100 g水)______________
查看答案和解析>>
科目: 来源: 题型:
【题目】聚酯纤维(涤纶)是重要的衣服面料,以下是一种合成路线(部分反应条件略去)。
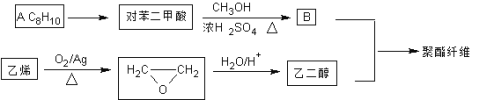
已知:酯与醇(或酚)可发生如下酯交换反应:![]()
(1)C8H10的系统命名为______________;它的同系物分子通式为________________。
(2)在其它催化剂作用下,乙烯与氧气反应的产物是____________(写结构简式)。
(3)若B过量,生成的聚酯纤维可表示为:![]() ,若乙二醇过量,则生成的聚酯纤维可表示为_______________________________。
,若乙二醇过量,则生成的聚酯纤维可表示为_______________________________。
(4)将废涤纶和甲醇在一定条件下反应,对聚合物进行降解,生成物是______________(填名称)。
(5)对苯二甲酸有多种芳香族同分异构体,写出一种满足以下条件的有机物的结构简式________。
①遇氯化铁溶液显紫色;②能发生银镜反应;③有三种不同化学环境的H原子。
(6)聚合物PC也由酯交换反应合成,其结构可表示为:![]() ,合成PC的2种单体中:醇(或酚)的结构简式为______________________,酯的名称为
,合成PC的2种单体中:醇(或酚)的结构简式为______________________,酯的名称为
_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】肉桂酸的一种合成路线如下:
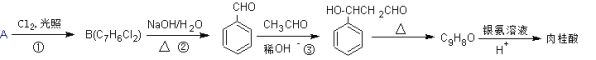
(1)烃A的名称为_________。反应①中B的产率偏低,其原因是________________________。
(2)反应②的化学方程式为_________________________________________________。
(3)反应③的反应类型是________________。
(4)肉桂酸的结构简式为__________________。
(5)反应③的产物同分异构体有多种,其中苯环上直接有一个甲基的酯类化合物有_____种。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)室温下,在0.5mol/L的纯碱溶液中加入少量水,由水电离出的c(H+)·(OH-)___(填“变大”、“变小”、“不变”)。
(2)已知Ksp(Ag2CrO4) =1.0×10-12,向0.2mol/L的AgNO3溶液中加入等体积的0.008mol/LK2CrO4溶液, 则溶液中的c(CrO42-)=___。
(3)室温下,0.1mol/LNaHCO3溶液的pH值___0.1mol/LNa2SO3溶液的pH值(填“>”、“<”、“=")。
H2CO3 | K1=4.3×10-7 | K2=5.6×10-11 |
H2SO3 | K1=1.54×10-2 | K2=1.02×10-7 |
已知:
(4)有一种可充电电池Na—Al/FeS,电池工作时Na+的物质的量保持不变,并且是用含Na+的导电固体作为电解质,已知该电池正极反应式为2Na++FeS+2e-=Na2S+Fe.则该电池在充电时,阳极发生反应的物质是___,放电时负极反应式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com