
科目: 来源: 题型:
【题目】一定条件下,CO2分子晶体可转化为具有类似SiO2结构的原子晶体.从理论上分析,下列说法正确的是( )
A.该转化过程是物理变化
B.1molCO2原子晶体中含2mol C﹣O键
C.CO2原子晶体的熔点高于SiO2
D.CO2的原子晶体和分子晶体互为同分异构体
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上CO2、CH4等含碳化合物有着重要的应用。
(1)科学家以CH4为原料来制备乙烯,同时得到氢气。已知相关物质的标准燃烧热如下表所示,写出甲烷制备乙烯的热化学方程式:__。
物质 | 标准燃烧热/kJ·mol-1 |
氢气 | -285.8 |
甲烷 | -890.3 |
乙烯 | -1411.0 |
(2)在400℃时,向初始体积为1L的恒容密闭反应器中充入1molCH4,发生上述反应,测得平衡混合气体中C2H4的体积分数为20.0%。
①该温度下,平衡常数K=__。
②若向该平衡体系中充入等物质的量的CH4和H2,则平衡将___(填“正向移动”或“逆向移动”或“不移动”成“无法确定”),理由是__。
(3)科学家用氮化镓材料与铜组装成如图所示的人工光合系统实现CO2的再利用。
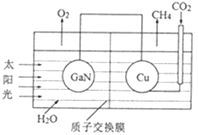
①该电化学装置属于__(填“原电池”或“电解池”)。
②该电池的Cu电极上发生反应的电极方程式为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图。字母代表元素,分析正确的是
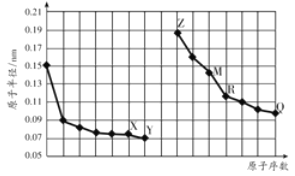
A. R在周期表的第15列
B. Y、Q两种元素的气态氢化物及其最高价氧化物的水化物均为强酸
C. 简单离子的半径:X>Z>M
D. Z的单质能从M与Q元素构成的盐溶液中置换出单质M
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室可用浓盐酸与浓硫酸混合快速制取HCl.下列解释合理的是( )
A.浓硫酸是高沸点的酸,通过它与浓盐酸反应制取低沸点的酸
B.通过改变温度和浓度等条件,利用平衡移动原理制取HCl
C.两种强酸混合,溶解度会相互影响,低溶解度的物质析出
D.浓硫酸的浓度远大于浓盐酸的浓度,高浓度的酸制取低浓度的酸
查看答案和解析>>
科目: 来源: 题型:
【题目】风靡全球的饮料果醋中含有苹果酸(MLA),其分子式为C4H6O5。0.1mol苹果酸与足量的NaHCO3溶液反应能产生4.48LCO2(标准状况),苹果酸脱水能生成使溴水褪色的产物。苹果酸经聚合生成聚苹果酸酯(PMLA)。
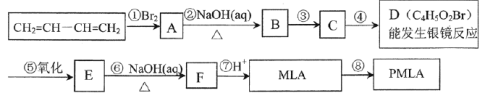
(1)写出物质的结构简式:A___,D___。
(2)指出合成路线中①、②的反应类型:①___;②___。
(3)写出所有与MLA具有相同官能团的同分异构体的结构简式:___。
(4)写出E→F转化的化学方程式___。
(5)上述转化关系中步骤③和④的顺序能否颠倒?___(填“能”或“不能”)。说明理由:___。
(6)请写出以丙烯为原料制备乳酸(2-羟基丙酸)的合成路线流程图(无机试剂任取)___。
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨是人工固氮最重要的途径,反应的热化学方程式如下:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ·mol-1。
2NH3(g) ΔH=-92.4kJ·mol-1。
(1)工业上有利于提高合成氨产率的条件有___。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)关于合成氨的说法,正确的是__。
A.合成氨反应的ΔH和ΔS都小于零
B.控制在773K下反应,目的是加快反应速率和提高平衡转化率
C.将NH3液化后移去,利于反应速率提高和平衡正向移动
D.原料气须经过净化处理,以防止催化剂中毒和事故发生
(3)若N2、H2的初始投入量分别为0.1mol、0.3mol,在恒容容器中反应,平衡后混合物中氨的体积分数(ψ)与温度、压强的关系如图所示。
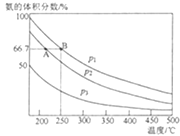
①比较p2、p3的大小:p2__p3(填“>”“<”或“=”),其原因是__。
②比较平衡时A、B点对应的化学反应速率:VA(N2)__VB(N2)(填“>”“<”或“=”)。
③若起始压强为1×108Pa,则平衡时B点的压强为___Pa。
(4)科学家发现,以H2O和N2为原料,熔融NaOH-KOH为电解质,纳米Fe2O3作催化剂,在250℃和常压下可实现电化学合成氨,阴极区发生的变化可按两步进行。已知第一步的反应为:Fe2O3+6e-+3H2O=2Fe+6OH-,则第二步的反应方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)![]() 2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示。已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法正确的是( )
2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示。已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法正确的是( )
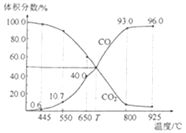
A.550℃时,若充入稀有气体,v正、v逆均减小,平衡不移动
B.T℃时,反应达平衡后CO2的转化率为50%
C.T℃时,若充入等体积的CO2和CO,平衡不移动
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.0p总
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在三个容积均为1.0L的恒容密闭容器中发生反应:
CH3OH(g)+CO(g) ![]() CH3COOH(g)△H<0。下列说法正确的是
CH3COOH(g)△H<0。下列说法正确的是
容器编号 | 温度/K | 物质的起始浓度/mol/L | 物质的平衡浓度/mol/L | ||
c(CH3OH) | c(CO) | c(CH3COOH) | c(CH3COOH) | ||
I | 530 | 0.50 | 0.50 | 0 | 0.40 |
II | 530 | 0.20 | 0.20 | 0.40 | |
III | 510 | 0 | 0 | 0.50 | |
A. 达平衡时,容器I与容器II中的总压强之比为3:4
B. 达平衡时,容器II中![]() 比容器I中的大
比容器I中的大
C. 达平衡时,容器Ⅲ中的正反应速率比容器I中的大
D. 达平衡时,容器I中CH3OH转化率与容器III中CH3COOH转化率之和小于1
查看答案和解析>>
科目: 来源: 题型:
【题目】为了测定实验室长期存放的Na2SO3固体的纯度,准确称取W g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案I:取25.00 mL上述溶液,加入过量的盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1g 。
方案Ⅱ:取25.00 mL上述溶液,加入过量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2g 。
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、胶头滴管、药匙和__________________、_________________。
(2)写出Na2SO3固体氧化变质的化学方程式__________________________________。
(3)方案I加入过量的盐酸酸化的BaCl2溶液,目的是_____________________________,在过滤前,需要检验是否沉淀完全,其操作是___________________________。
(4)方案I中,若滤液浑浊,将导致测定结果____________(选填“偏高”或“偏低”)。
(5)若操作正确,则m1_____ m2(选填“>”、“<”或“=”),原因是________________。
(6)取25.00 mL上述溶液,用滴定的方法测定Na2SO3的纯度。下列试剂可作为标准溶液进行滴定的是________。
a.酸性KMnO4溶液 b.H2O2溶液 c.Br2水 d.FeCl3溶液
Na2SO3固体的纯度可表示为:______________________________(注明你的表达式中所用的有关符号的含义和单位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮元素的化合物在工农业以及国防科技中用途广泛,但也会对环境造成污染,如地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题。
(1)神舟载人飞船的火箭推进器中常用肼(N2H4)作燃料。NH3与NaClO反应可得到肼(N2H4),该反应中被氧化与被还原的元素的原子个数之比为___。如果反应中有5mol电子发生转移,可得到___ g肼。
(2)常温下向25mL0.01mol/L稀盐酸中缓缓通入5.6mLNH3(标准状况,溶液体积变化忽略不计),反应后溶液中离子浓度由大到小的顺序是___。在通入NH3的过程中溶液的导电能力___(填写“变大”、“变小”或“几乎不变”)。
(3)向上述溶液中继续通入NH3,该过程中离子浓度大小关系可能正确的是___(选填编号)。
a.[Cl-]=[NH4+]>[H+]=[OH-] b.[Cl-]>[NH4+]=[H+]>[OH-
c.[NH4+]>[OH-]>[Cl-]>[H+] d.[OH-]>[NH4+]>[H+]>[Cl-]
(4)常温下向25mL含HCl0.01mol的溶液中滴加氨水至过量,该过程中水的电离平衡(填写电离平衡移动情况)___。当滴加氨水到25mL时,测得溶液中水的电离度最大,则氨水的浓度为___mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com