
科目: 来源: 题型:
【题目】贝诺酯是一种解热镇痛药,在酶的作用下可以释放出阿司匹林和扑热息痛,其结构为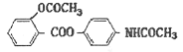 ,其合成途径如下:
,其合成途径如下:
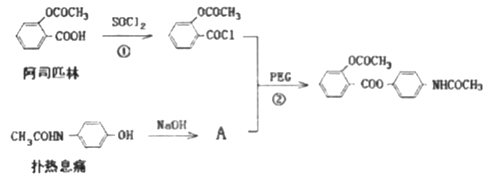
完成下列填空:
(1)反应①的反应类型为________________,有机物A与扑热息痛的式量相差______________
(2)贝诺酯所含的含氧官能团是__________
(3)写出反应②的化学方程式_____________
(4)关于阿司匹林性质叙述正确的是(填选项编号)____________
A.能与氯化铁溶液发生显色反应 B.能与氢氧化铜悬浊液反应
C.能发生消去反应 D.能发生酯化反应
(5)符合下列条件的扑热息痛的同系物共有_________种,写出其中一种的结构简式___________。
①碳原子数比扑热息痛多2个 ②苯环上只有2个对位的支链 ③含有2个甲基
(6)若已知:
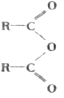 +R'OH
+R'OH![]() RCOOH +RCOOR'
RCOOH +RCOOR'
现以苯酚和乙酸酐(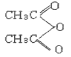 )为有机原料,合成阿司匹林,请设计完成下列合成途径______(合成路线常用的表示方法为:A
)为有机原料,合成阿司匹林,请设计完成下列合成途径______(合成路线常用的表示方法为:A![]() B……
B……![]() 目标产物)
目标产物)
查看答案和解析>>
科目: 来源: 题型:
【题目】将一包铝热剂(铝粉和氧化铁的混合物),进行如下实验,①向一份铝热剂中加入800ml 2mol/L的氢氧化钠溶液,使其充分反应后,收集到的气体体积为20.16L(S.T.P.)②另一份等质量的铝热剂在高温下充分反应后,向反应后固体中加入2L 2.5mol/L的盐酸溶液,使固体完全溶解,反应后溶液PH=0(假设过程中溶液体积不变),取少量反应后溶液,滴加硫氰化钾,没有出现血红色.完成下列计算:
(1)计算该铝热剂中铝与氧化铁物质的量之比?_______________
(2)实验②产生的气体的体积是多少?(S.T.P.)______________
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表中大多数元素是金属元素,金属及其化合物在生活生产中有着重要应用,根据试题信息,完成下列计算:
(1)某常见二价金属12.6g与足量稀硫酸反应,生成氢气5.04L(S.T.P),该元素原子的摩尔质量为__g/mol.
(2)39.32g某金属混合物,由12.32g镁和0.25mol另一种比镁不活泼的金属元素A组成,该混合物与一定量盐酸反应,产生氢气4.928L(S.T.P),则参加反应的HCl为__mol,金属A的相对原子质量为__.
(3)由NaCl、NaHCO3、Na2CO310H2O组成的混合物157.8g,充分加热后,产生的气体(气体温度150℃)依次通过无水CaCl2和碱石灰,两种吸收剂分别增重59.4g和13.2g,则混合物中NaHCO3的质量分数为___,若等质量的该混合物与足量盐酸反应,产生二氧化碳(S.T.P)__L.
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是制备二氧化硫制取和吸收装置(加热装置已省略)分液漏斗中是液体反应试剂A,烧瓶中盛反应试剂B。完成下列填空:
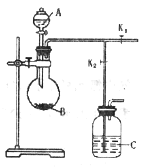
(1)实验室制备二氧化硫的试剂是_____________和________________。
(2)检验该气体发生装置气密性的方法是____________。
(3)装置C是吸收多余二氧化硫的装置,其中盛放的吸收剂为__________,实验结束进行尾气吸收时,对活塞开关K1、K2的控制是_____________________。
(4)如果用该套装置制备盐酸,此时C瓶所加试剂为_____________,此时C中液体可能会发生倒吸,如果不改变现有的装置,要克服这一安全隐患,可以在C瓶中再加入有机试剂封住长导管管口,该有机试剂可以为___________,吸收后,将 C瓶中的液体经过_____操作获得盐酸。
(5)甲同学用该装置测定一定质量小苏打样品(含少量NaCl)中碳酸氢钠的纯度,可以在C中加入氢氧化钠溶液吸收二氧化碳,通过C瓶增重得到二氧化碳质量,计算出碳酸氢钠的含量,实验结果小苏打含量偏低,你认为实验结果偏低的原因是_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁元素、氮元素有多种可变价态,在氧化还原反应中常以不同价态出现,根据题中信息,完成下列填空:
(1)金属与硝酸反应通常还会生成NO和NO2,当n(NO): n(NO2)<1时,产生的气体可以完全被氢氧化钠溶液吸收,写出除去这两种气体的方法,以化学方程式表示_________、_______
(2)室温下,0.1mol/L的亚硝酸、次氯酸钠的电离常数HNO2:Ki =7.1× 10-4, HClO: Ki =2.98× 10-8,将0.1mol/L的亚硝酸稀释100倍,c(H+)=将(填“不变”、“增大”、“减小”)_______;Ki值将(填“不变”、“增大”、“减小”)_______。写出HNO2、HClO、NaNO2、NaClO四种物质,可能相互之间发生的离子互换反应的离子方程式_________。
(3)亚硝酸钠与氯酸钠都是白色粉末,且都有咸味,但亚硝酸盐都有毒性,通常它们可以通过加入热的白醋鉴别,亚硝酸钠遇到白醋会产生红棕色刺激性气味气体,该气体为______;实验室鉴别氯化钠和亚硝酸钠的方法之一是测定等浓度NaNO2、NaClO的pH,其鉴别的理由是______________。
(4)现有11.2g铁单质恰好与稀硝酸反应,生成无污染的单质气体,该单质气体为________,在反应后的溶液中加入铜粉,铜粉可以继续溶解,且无气体生成,铁与稀硝酸的反应产物中一定含有的金属阳离子是______,若反应后的溶液最多可溶解铜粉6.4g,写出上述过程中铁与稀硝酸反应的化学方程式___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氨的催化氧化是工业制硝酸的重要反应,500°C,其反应方程式为:4NH3(g) +5O2(g)4NO(g)+6H2O(g)+Q,完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是___________________
a.减压 b.增加NH3的浓度 c.升温 d.将水液化移走
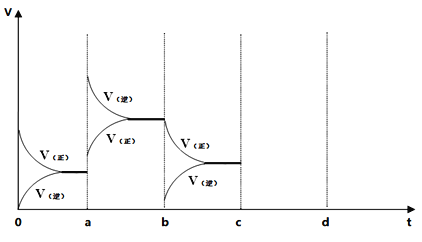
(2)在500℃时,在2L密闭容器中加入10mol NH3、10mol O2,上述可逆反应达到平衡,过程如图所示,在a时刻改变反应条件,重新达到平衡,该改变的条件可能是____________,比较b时刻与c时刻反应氨的转化率大小(填“>”或“<”)b____c。其它条件不变,c时刻加压后,若平衡正向移动,其原因可能是____________,若在d时刻重新达到平衡,请在图中画出c到d的相关变化图像________。
(3)工业上以氨和空气为原料生产硝酸,请画出硝酸工业的物质流程图________
(4)氨中氮元素原子最外层电子排布的轨道表达式是______________,短周期元素原子所形成的与N3-电子排布相同的离子所对应的原子的半径从大到小的排列顺序为 _______________。其中非金属元素形成的氢化物的稳定性由强到弱为的顺序为(用化学式表示)_____________。
(5)已知NH3与N2H4都是氮的氢化物,N2H4的电子式是 __________________。NH3与N2H4都具有还原性,可以与其它强氧化剂反应,例如在一定条件下,氨可以被双氧水氧化为游离态氮,写出该反应的化学方程式 ______________
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列溶液中一定大量共存的离子组是( )
A.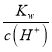 =0.1 mol L1 的溶液:Na+、K+、CO32-、NO3-
=0.1 mol L1 的溶液:Na+、K+、CO32-、NO3-
B.含有大量 S2-的溶液中:K+、Fe3+、ClO-、SO42-
C.能使 Al3+生成沉淀的溶液中:NH4+、Na+、SiO32-、HCO3-
D.水电离产生的 c(OH-)=1×10-10 mol/L 的溶液中:Fe2+、SO42-、NO3-、Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应mA(s)+nB(g)eC(g)+fD(g),反应过程中,当其它条件不变时C 的百分含量与温度 (T)和压强(P)关系如图所示,下面叙述正确的是( )
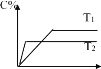
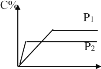
A.使用催化剂,C 的百分含量增大
B.升温,化学平衡向正反应方向移动
C.化学方程式的化学计量数关系 n<e+f
D.其他条件不变,增入 A 物质,提高 B 的转化率
查看答案和解析>>
科目: 来源: 题型:
【题目】洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图。下列关于A的相关叙述正确的是
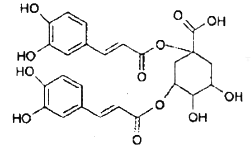
A.A在酸性条件下可以发生水解反应
B.1mol A和足量NaOH溶液反应,最多消耗9mol NaOH
C.A能和浓溴水发生加成和取代反应
D.A含4种官能团
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不属于盐类水解应用的是( )
A.明矾、氯化铁晶体常用于净水
B.实验室通常在HCl气氛中加热MgCl2·6H2O制MgCl2
C.实验室配制FeCl3溶液时加入少量稀盐酸
D.实验室制氢气时加入CuSO4可加快反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com