
科目: 来源: 题型:
【题目】海洋是一个巨大的化学资源宝库,海水资源综合利用的部分流程图。
![]()
(1)由海水提取的粗盐中常含有![]() 等,可以加入_______________(填化学式)除去,反应的离子方程式为__________________。
等,可以加入_______________(填化学式)除去,反应的离子方程式为__________________。
(2)步骤①反应的离子方程式为__________________。
(3)步骤②中溴单质被SO2还原为![]() ,硫元素被氧化为
,硫元素被氧化为![]() ,从该反应原理中不能得出溴的非金属性强于硫,其原因是__________________。当有0.25 mol SO2被氧化,转移的电子的物质的量为__________mol。
,从该反应原理中不能得出溴的非金属性强于硫,其原因是__________________。当有0.25 mol SO2被氧化,转移的电子的物质的量为__________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应mA(g)+nB(g)=eC(g)+fD(s) △H。若按反应物的化学计量数比投料,在一定条件下进行反应,该反应达到平衡时C的气体体积分数与温度、压强的关系如图所示。下列叙述正确的是
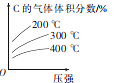
A.该反应的△H >0
B.该化学方程式中m+n>e+f
C.加入催化剂可加快正反应速率,逆反应速率不变
D.往平衡后的恒压容器中再充入一定量C,达到新平衡时,C的浓度与原平衡时的相同
查看答案和解析>>
科目: 来源: 题型:
【题目】利用原电池原理,在室温下从含低浓度铜的酸性废水中回收铜的实验装置如图所示,下列说法错误的是
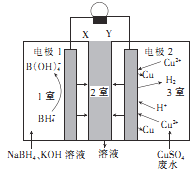
A.电极1为负极
B.Y为阳离子选择性交换膜
C.电极2上只有Cu析出
D.负极的电极反应式: ![]() +8
+8![]() 8
8![]() B
B![]() +4
+4![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学称取9.00g淀粉溶于水,测定淀粉的水解百分率.其程序如下:
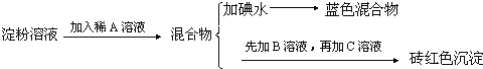
试回答下列问题:
(1)各步加入的试剂为:A_________,B_________,C_________;
(2)加入A溶液而不加入B溶液是否可以_________,其理由是_________;
(3)写出淀粉水解的方程式_________;
(4)当析出1.44g砖红色沉淀时,淀粉水解率是_________;[已知葡萄糖与Cu(OH)2反应的化学方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2![]() CH2OH(CHOH)4COOH+Cu2O↓+2H2O]。
CH2OH(CHOH)4COOH+Cu2O↓+2H2O]。
查看答案和解析>>
科目: 来源: 题型:
【题目】有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是( )
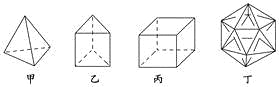
A. 1 mol甲分子内含有10 mol共价键
B. 由乙分子构成的物质不能发生氧化反应
C. 丙分子的二氯取代产物只有三种
D. 分子丁是不可能合成的
查看答案和解析>>
科目: 来源: 题型:
【题目】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
化学性质 | ①300℃以上完全分解; ②S2Cl2+Cl2 ③遇高热或与明火接触,有引起燃烧的危险; ④受热或遇水分解放热,放出腐蚀性烟气; | ||||
Ⅰ.制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品。
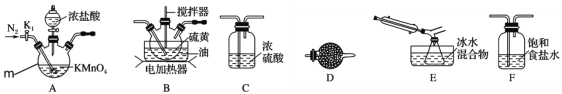
(1)仪器m的名称为___,装置A中发生反应的离子方程式为 ______________。
(2)装置连接顺序:A→___→___→___→E→D。______________
(3)为了提高S2Cl2的纯度,实验的关键是控制好温度和__________________。
(4)若D中所装试剂为碱石灰,则该装置的作用为______________。
II.测定产品中SO2Cl2的含量,实验步骤如下:
①取1.8g产品加入足量Ba(OH)2溶液,充分振荡、过滤、洗涤,将所得溶液均放入锥形瓶中;
②向锥形瓶中加入硝酸酸化,再加入0.2000mol·L-1的AgNO3溶液l00.00mL;
③向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
④加入NH4Fe(SO4)2指示剂,用0.1000mol·L-1NH4SCN溶液滴定过量Ag+,终点所用体积为10.00mL。
已知:Ksp(AgCl)=3.2×10-10 ;Ksp(AgSCN)=2×10-12
(5)滴定终点的现象为_____________________________。
(6)产品中SO2Cl2的质量分数为__________,若步骤③不加入硝基苯则所测SO2Cl2含量将________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式(![]() )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目: 来源: 题型:
【题目】莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是( )
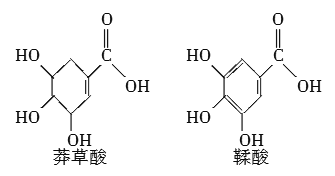
A.两种酸都能与溴水发生加成反应
B.两种酸与三氯化铁溶液都能发生显色反应
C.鞣酸分子与莽草酸分子相比多了两个碳碳双键
D.等物质的量的两种酸与足量的金属钠反应产生氢气的量相同
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物J是一种防止血管中血栓形成与发展的药物,其合成路线如图所示 (部分反应条件略去)。
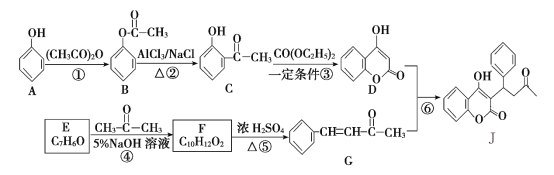
回答下列问题:
(1)反应①的反应类型是________,反应⑥的反应类型是________。
(2)J的分子式是________。F的结构简式是________。
(3)反应③的化学方程式为___________________________________。
(4)写出同时满足下列条件的F的所有同分异构体的结构简式________。
①苯环上只有两个处于对位的取代基;
②1 mol该有机物能与含2 mol NaOH的溶液恰好完全反应。
(5)参照J的合成路线,设计一种以![]() 为原料制备
为原料制备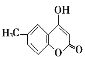 的合成路线________。
的合成路线________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com