
题目列表(包括答案和解析)
7. 下列除去杂质的方法正确的是
A. 除去FeCl2溶液中的少量FeCl3: 加入足量铁屑,充分反应后过滤
B. 除去CO2中的少量HCl: 通入Na2CO3溶液,收集气体
C. 除去N2中的少量O2: 通过灼热的CuO粉末,收集气体
D. 除去KCl溶液中的少量MgCl2: 加入适量NaOH溶液,过滤
6. 下列各组顺序不正确的是:
A.粒子半径:S2->Cl ->F ->Na+>Mg2+ B.热稳定性:SiH4<PH3<NH3<H2O<HF
C.熔点: SiO2>NaCl>干冰>碘>臭氧 D.还原性:HF<HCl<HBr<HI<H2S
5. 已知C3N4晶体具有比金刚石还大的硬度,且每个原子的最外层均满足8电子结构。下列关于C3N4晶体的说法正确的是:
A. C3N4晶体可能是分子晶体,晶体中微粒间通过共价键相结合
B. C3N4晶体中每个碳原子连接4个氮原子,每个氮原子连接3个碳原子
C. C3N4晶体中,C-N键的键长比金刚石中C-C键的键长要长
D. C3N4晶体中每个氮原子上还有2对未共用电子
4. 下列说法或表示方法中正确的是:
A. 等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多
B. 氢气的燃烧热为285.8kJ · mol-1,则氢气燃烧的热化学方程式为
2H2(g) + O2(g) = 2H2O(l);△H=-285.8 kJ· mol-1
C. Ba(OH)2 · 8H2O(s) + 2NH4Cl(s) = BaCl2(s) + 2NH3(g) + 10H2O(l);△H<0
D. 已知中和热为57.3 kJ · mol-1,若将含0.5mol H2SO4的浓溶液与含1mol NaOH的溶液混合,放出的热量要大于57.3 kJ
3.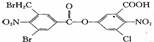 已知卤代烃在碱性条件下易水解。某有机物的结构简式如下;lmol 该有机物与足量的NaOH 溶液混合共热,充分反应最多可消耗amolNaOH,将所得溶液蒸干后再与足量的碱石灰共热,又消耗bmol NaOH。则a与b的值分别是
已知卤代烃在碱性条件下易水解。某有机物的结构简式如下;lmol 该有机物与足量的NaOH 溶液混合共热,充分反应最多可消耗amolNaOH,将所得溶液蒸干后再与足量的碱石灰共热,又消耗bmol NaOH。则a与b的值分别是
A. 5mol,10mo1 B.6mol,2mol
C.8mol,4mol D.8mol,2mol
2.下列分子中,所有原子不可能共处在同一平面上的是
A.C2H2 B.CS2 C.NH3 D.C6H6
1.我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料。下列相关叙述中错误的是
A. 使用乙醇汽油能能减少有害气体的排放 B. 乙醇汽油是一种新型化合物
C.乙醇可以通过粮食发酵或化工合成等方法制得 D.甲醇、乙醇都属于可再生能源
27.(12分)有下列实验:将过量Mg粉溶于100mL 1.5mol·L-1的稀H2SO4中,反应结束后, 滤去多余Mg粉,滤液在保持t℃的恒温下蒸发水分,当滤液质量为63 g时开始析出 MgSO4·xH2O晶体,当析出晶体13.47g时,剩下滤液40g。请计算下列各小题:
(1)生成标准状况下的气体体积。
(2)开始析出MgSO4·xH2O晶体时溶液的质量分数。
(3)t℃时MgSO4的溶解度。
(4)MgSO4·xH2O中x的值。
26.(8分)NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:Na2CO3
+nH2O==Na2CO3·nH2O(n为平均值,n≤10)。取没有妥善保管的NaHCO3样品9.16g,溶于水制成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表。(溶于水的CO2不计)
|
盐酸的体积(mL) |
4 |
8 |
15 |
20 |
50 |
120 |
150 |
|
生成CO2的体积(mL) |
0 |
0 |
112 |
224 |
896 |
2240 |
2240 |
求:
(1)稀盐酸的物质的量浓度。
(2)样品中的成分及成分的物质的量。
25.(10分)利用芳香烃X和链烃Y可以合成紫外线吸收剂BAD,已知G不能发生银镜反应,BAD的结构简式如下:
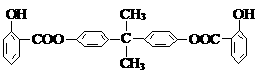
BAD的合成路线如下图所示:
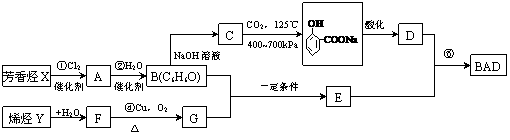 试回答下列问题:
试回答下列问题:
(1)写出结构简式:X ,Y 。
(2)在反应①-⑤中,属于取代反应的有 (填数字序号)。
(3)写出下列反应的化学方程式:
反应④: ;
B+G→E: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com