
题目列表(包括答案和解析)
25、混合物的计算(近10年来的化学高考命题中的呈现率:90%)
[点题]密闭容器中有CO和空气的混合气体14L,用电火花引燃,经充分反应后总体积为VL(假设所有体积均在同温、同压下测定,且空气中O2的体积分数以0.20计算。计算结果保留两位小数)
(1)若CO和O2恰好反应,计算原混合气体中CO的体积分数(请写出必要过程)。
(2)若反应后总体积V=13时,则原混合气体可能的组成为(可不填满,也可补充)。
第一种情况:V(CO):V(O2)=_______________;
第二种情况:V(CO):V(O2)=_______________;
第三种情况:V(CO):V(O2)=_______________。
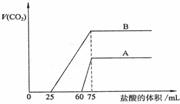
(3)反应后总体积数V的取值范围是_______________。
[点晴] (1)设原混合气体中CO的体积为x,O2的体积为y。
据题意得关系式:
 列二元一次方程组:
列二元一次方程组: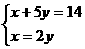 解得:
解得: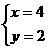
 则原混合气体中CO的体积分数=0.29 (2)9:1 (CO剩余)
1:1.2
(原空气中O2剩余) (3)
则原混合气体中CO的体积分数=0.29 (2)9:1 (CO剩余)
1:1.2
(原空气中O2剩余) (3)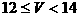
[点题]取等物质的量浓度的NaOH溶液两份A和B,每份50mL,向其中各通入一定量的CO2,然后各取溶液10mL,分别将其稀释为100mL,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸体积之间的关系如右图所示,试回答下列问题:
(1)曲线A表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式) ,两种溶质的物质的量之比为 ;加盐酸后产生CO2体积的最大值为 mL。
(2)曲线B表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式) ,两种溶质物质的量之比为 ;加盐酸后产生CO2体积最大值 mL。
(3)通过计算求出原NaOH溶液的物质的量浓度。
[点晴](1) NaOH、Na2CO3 3∶1 33.6 (2)Na2CO3、NaHCO3 1∶1 112
(3)解:图示表明,向溶液中滴加0.1mol/L的盐酸至不再放出CO2气体时,消耗盐酸的体积为75mL。所以原NaOH溶液的物质的量浓度为:
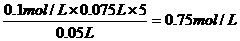 (其它合理解法可得分)
(其它合理解法可得分)
[点题]有机物A是烃或烃的含氧衍生物,分子中碳原子数不超过6。当0.1 mol A 在0.5 mol O2中充分燃烧后,A无剩余。将生成的气体(1.01×105 Pa,110 ℃下)依次通过足量的无水氯化钙和足量的碱石灰,固体增重质量之比为9∶11,剩余气体的体积折算成标准状况为6.72 L。试通过计算、讨论确定A可能的化学式。
[点晴] (1)若剩余氧气,则由二氧化碳与水的物质的量之比,可知有机物中C、H原子个数比为1:4。可假设有机物化学式为(CH4)mOn,列式讨论,得该有机物为CH4。(2)若剩余气体为CO,则由有机物、氧气、一氧化碳的物质的量分别为0.1mol、0.5mol、0.3mol,可知反应中化学计量数之比。假设该有机物化学式为CXHYOZ。
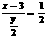
 CXHYOZ+5O2 3CO+(x-3)CO2+Y/2
H2O
CXHYOZ+5O2 3CO+(x-3)CO2+Y/2
H2O
由CO2与H2O物质的量之比为1﹕2得: ①
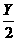
由氧原子守恒得:Z+10=3+(2X-6)+ ②
综合①②得:Z=4X-19
讨论知:X=5时,Z=1,有机物化学式为:C5H8O
X=6时,Z=5,有机物化学式为:C6H12O5
用最少的悔恨面对过去
用最少的浪费面对现在
用最多的梦想面对未来
 每天告诉自己一次,『我真的很不错』
每天告诉自己一次,『我真的很不错』
浙江省武义第一中学 刘卫捐 321200
24、有机物的燃烧规律(近10年来的化学高考命题中的呈现率:60%)
[点题]某类有机物CnHxOy完全燃烧需要O2的物质的量为该有机物的n倍,生成CO2
和H2O的物质的量之比为1:1
(1)该类有机物的分子通式为(CnHxOy中的x、y均以n表示) 。
(2)若n=3,写出符合下列条件的物质的结构简式(各一种):
①呈酸性,且能发生缩聚反应: 。
②呈中性,且能发生水解反应: 。
(3)有一种符合此通式的有机物,可以在一定条件下用农作物的秸秆制取,写出反应的化学方程式(该有机物用结构简式表示): 。
[点晴]
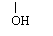 (1) CnH2nOn (2) ①HOCH2-CH2-COOH(或CH3-CH-COOH)
(1) CnH2nOn (2) ①HOCH2-CH2-COOH(或CH3-CH-COOH)
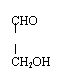 ②H-C-O-CH2-CH2OH(或HO-CH2-C-O-CH3)
②H-C-O-CH2-CH2OH(或HO-CH2-C-O-CH3)

(3) (C6H10O5)n+ n H2O n(CHOH)4
23、有机物的合成(近10年来的化学高考命题中的呈现率:100%)
[点题]去年9月底,国家质检总局查处了在食品中使用“雕白块”七大案例。“雕白块”的化学名称为甲醛次硫酸氢钠,违法者往食品中添加“雕白块”是为了漂白增色、防腐、增加米面制品的韧性及口感。但人食用“雕白块”后会刺激肠道,引起过敏和食物中毒,容易致癌。已知“雕白块”是甲醛和次硫酸氢钠(可表示成Na+[OSOH]-)反应制得:
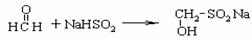
回答下列问题:
(1)“雕白块”_______________(填“易”或“微”或“难”)溶于水。“雕白块”具有________(填“强还原性”或“强氧化性”),写出“雕白块”溶液中滴加足量碘水所发生反应的化学方程式_____________________________________。
(2)写出次硫酸氢根的电子式___________________________。
(3)写出水溶液中次硫酸氢钠和氢氧化钾反应的离子方程式____________________。
(4)甲醛能使__________变性凝固,所以可用其浓溶液保存动物标本。
(5)甲醛是非常重要的合成原料。纯净的甲醛在[F3B←O(CH2CH3)2]配位化合物的催化下,生成聚甲醛(是一种优良的工程塑料),聚甲醛的结构简式为_____________;俄国化学家布特列洛夫在1861年首次发现在弱碱作用下,6个甲醛分子加合得到己糖,此己糖的分子式为___________。
[点晴](1)易。强还原性。NaHSO2·CH2O+2I2+2H2O?4HI+NaHSO4+CH2O。(2)
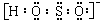 。(3)HSO2-+OH-=H2O+SO22-。(4)蛋白质。(5)聚甲醛。 C6H12O6。
。(3)HSO2-+OH-=H2O+SO22-。(4)蛋白质。(5)聚甲醛。 C6H12O6。
[点题]已知二氯烯丹是一种播前除草剂, 其合成路线如下:
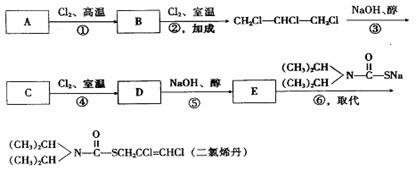
D在反应⑤中所生成的E, 其结构只有一种可能.
(1)写出下列反应类型: 反应①是_____________, 反应③是________________.
(2)写出下列物质的结构简式:
A________________, C_______________,D__________________, E_______________。
[点晴] 此题主要是考查卤代烃的化学性质,卤代烃的化学性质就两个,一是与氢氧化钠水溶液发生取代反应生成醇,二是与氢氧化钠醇溶液发生消去反应生成烯烃。有机框图推断题一般考查:同分异构体、同系物,有机化学反应类型,有机化学方程式书写,有机物结构简式书写等。同学们只要掌握好典型官能团的性质,抓住有机化学的知识主线:烯烃 卤代烃
卤代烃 醇
醇 醛
醛 酸
酸 酯。有机框图题就会迎刃而解。有机框图推断题一般有三种解法:顺推、逆推、顺逆结合推。此题突破口在B与氯气加成得到CH2Cl-CHCl-CH2Cl,从面倒推出B 为CH2Cl-CH=CH2和A为CH3-CH=CH2。CH2Cl-CHCl-CH2Cl与氢氧化钠醇溶液发生消去反应可得出C为CH2Cl-CCl=CH2,C再与氯气加成变成D:CH2Cl-CCl2-CH2Cl。D再与氢氧化钠醇溶液发生消去反应可得出E为CH2Cl-CCl=CHCl。
酯。有机框图题就会迎刃而解。有机框图推断题一般有三种解法:顺推、逆推、顺逆结合推。此题突破口在B与氯气加成得到CH2Cl-CHCl-CH2Cl,从面倒推出B 为CH2Cl-CH=CH2和A为CH3-CH=CH2。CH2Cl-CHCl-CH2Cl与氢氧化钠醇溶液发生消去反应可得出C为CH2Cl-CCl=CH2,C再与氯气加成变成D:CH2Cl-CCl2-CH2Cl。D再与氢氧化钠醇溶液发生消去反应可得出E为CH2Cl-CCl=CHCl。
故(1)取代反应 消去反应(2)CH3-CH=CH2,CH2Cl-CCl=CH2 , CH2Cl-CCl2-CH2Cl ,CH2Cl-CCl=CHCl。(特别注意官能团保护题,其中有有机合成中的防官能团还原的保护与恢复和防官能团受氧化影响的保护与恢复。)
22、有机物的聚合及单体的推断(近10年来的化学高考命题中的呈现率:70%)
[点题] 非典型肺炎(SARS)病毒是一种RNA病毒,是三万多个碱基组成,分子直径达100nm,目前治疗该病尚无特效药,目前用于治疗的抗菌指定药物之一是阿昔洛韦[化学名称:9-(2-羟乙氧甲基)鸟嘌呤],已知这种药物的结构式如下:
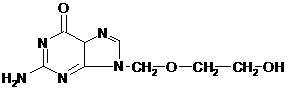
关说法不正确的是 ( )
A.阿昔洛韦的分子式为:C8H10N5O3 B.该物质一定条件下可发生消去反应
C.该物质一定条件可发生取代反应 D.五个氮原子一定在同一平面内
[点晴] 本题为一题化学学科内综合题,通过看图可得分子式为:C8H11N5O3,当然也可根据分子中N、H原子的奇偶性一致的原则,判断出A是错误的。由于分子中有羟基,所以能发生取代、消去反应,B、C正确。根据不同化学键在空间可能伸展方向,D是错误的。故选A、D。
[点题]新兴的大脑营养学研究发现,大脑的生长发育与不饱和脂肪酸有密切关系,被称为脑黄金的DHA就是一种不饱和程度很高的脂肪酸,它的分子中有6个C=C键,学名二十六碳六烯酸,它的分子组成是
A.C25H50COOH B.C25H39COOH C.C26H41COOH D.C26H47COOH
[点晴] B
[点题]中草药秦皮中含有的七叶树内酯 (碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
(碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
A.3mol Br2;2mol NaOH B.3mol Br2;4mol NaOH
C.2mol Br2;3mol NaOH D.4mol Br2;4mol NaOH
[点晴] 有机物中结构决定性质。不同类型的有机物有其不同的官能团与结构,在学习中一定要注意反应时化学键断裂部位,是学好有机物的关键所在!本题要求学生在理解酚和酯的结构及其性质的基础上,将获取的有关规律迁移到题 目所指定的有机物中。由于学生在课本中学习的是一元酚和普通酯,而题设物质却是一种既 可以看成二元酚,又可看成酯(内酯)且含有双键的复杂有机物,所以本题在考查相关知识点 的同时,也在一定程度上考查学生思维的灵活性、广阔性和创造性。仔细观察该有机物的结构简式并结合已有知识,不难得知:1mol七叶树内酯可与3mol Br2 相作用,其中2mol Br2 用于酚羟基的邻位氢的取代(注:对位无氢可取代),1mol用于酯环上双键的加成,其反应原理为:
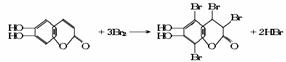
当1mol七叶树内酯与NaOH反应时,需4mol NaOH,其中3mol NaOH与酚羟基(包括水解后生成 的)作用,1mol NaOH与水解后产生的羧基发生中和反应,其反应原理为:
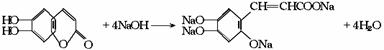
故选B。
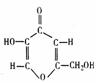 [点题]从米曲霉中分离出的曲酸是-种新型添加剂,其分子结构如下图。曲酸具有抗氧化性(保护其它物质不被空气氧化),在化妆、医药、食品、农业等方面具有广泛的应用前景。下列关于曲酸的说法正确的是
[点题]从米曲霉中分离出的曲酸是-种新型添加剂,其分子结构如下图。曲酸具有抗氧化性(保护其它物质不被空气氧化),在化妆、医药、食品、农业等方面具有广泛的应用前景。下列关于曲酸的说法正确的是
A. 曲酸是一种芳香族化合物 B.曲酸是一种羧酸,难溶于水
C. 曲酸分子中的所有原子不可能都在同一平面上
D. 曲酸被空气中的O2氧化时,反应发生在环上的羟基部位
[点晴] BC
21、同分异构体(近10年来的化学高考命题中的呈现率:100%)
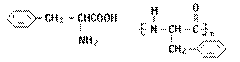 [点题]化合物A与化合物是同分异构体。A是天然蛋白质的水解产物,分子中不存在甲基。A的结构简式是_________________,A的分子间互相结合而形成的高分子化合物的结构简式是___________________________。
[点题]化合物A与化合物是同分异构体。A是天然蛋白质的水解产物,分子中不存在甲基。A的结构简式是_________________,A的分子间互相结合而形成的高分子化合物的结构简式是___________________________。
[点晴]
20、完成有机反应的化学方程式(近10年来的化学高考命题中的呈现率:90%)
[点题]2003年8月4日在齐齐哈尔市发生了侵华日军遗留的芥子气毒气罐泄漏伤人事件。芥子气,学名二氯二乙硫醚,是微黄色或无色的油状液体,具有芥子末气味或大葱、蒜臭味。芥子气的分子式为(ClCH2CH2)2S。
(1)芥子气可用两种方法制备。其一是ClCH2CH2OH和Na2S反应,反应产物之一接着与氯化氢反应;其二是CH2=CH2与S2Cl2反应,反应物的物质的量比为2∶1。写出化学方程式________________________________;_____________________________________。
(2)碱液可以解毒。写出化学方程式________________________________________。
(3)根据上述二氯二乙硫醚性质,你能设计一种最简单且实用快速的预防方法吗?
____________________________________________________________________________。
(4)对局部中毒如皮肤上之毒液,可立即采取什么措施进行简单的处理
A.用可溶解芥子气的溶剂如煤油、酒精 B.用漂白粉、双氧水浸润棉球吸去毒液
C.用浓氢氧化钠溶液浸润的棉球擦洗 D.将中毒局部皮肤割除
[点晴] (1)2ClCH2CH2OH + Na2S→(HOCH2CH2)2S + 2NaCl
(HOCH2CH2)2S + 2HCl→(ClCH2CH2)2S + 2H2O 2CH2 = CH2 + S2Cl2 →(ClCH2CH2)2S + S
(2)(ClCH2CH2)2S + 2OH- →(HOCH2CH2)2S + 2Cl-
(3)可用纱布、棉花浸润Na2CO3溶液或碱性洗衣粉作解毒溶液制成简单面具。(4)A B
[点题]类似于卤素X2与苯的同系物的反应,卤代烃亦可进行类似反应,如均三甲苯与氟乙烷的反应。它们的反应经历了中间体(Ⅰ)这一步,中间体(Ⅰ)为橙色固体,熔点-15℃,它是由负离子BF4-与一个六元环的正离子组成的,正离子中正电荷平均分配在除划*号碳原子以外的另五个成环的碳原子上,见下图(Ⅰ)虚线。
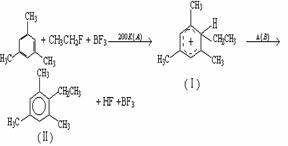
(1) 从反应类型看,反应A属于 ,反应B属于 ,全过程属于 。
(2)中间体(Ⅰ)中画*号的碳原子的立体构型与下列化合物中画*号碳原子接近的是( )
A *CH≡CH B CH3*CH2CH3 C 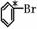 D
D 
(3)模仿上题,完成下列反应(不必写中间体,不考虑反应条件,但要求配平)。
① 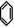 +
+ 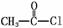 --→
--→
② 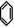 (过量)+ CHCl3 --→
(过量)+ CHCl3 --→
③  + --→
+ --→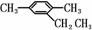 +
HBr
+
HBr
[点晴] (1)加成,消去,取代 (2)B
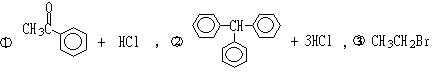 (3)
(3)
19、实验及实验与基本概念原理、元素化合物知识、有机化合物知识、化学计算等方面的综合(近10年来的化学高考命题中的呈现率:100%)
做过银镜反应实验的试管,可以用铁盐溶液洗涤,这是因为 与Ag发生可逆反应:
与Ag发生可逆反应: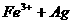
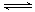
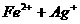 (1)若使该平衡向右移动,应采取的措施是:__________________________________________________________________________,(2)c(
(1)若使该平衡向右移动,应采取的措施是:__________________________________________________________________________,(2)c( )相同的
)相同的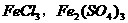 两种溶液,洗涤效果最好的___________,原因是:_______________________________________________________ ,
两种溶液,洗涤效果最好的___________,原因是:_______________________________________________________ ,
(3)有人认为 溶液也可以做洗涤剂,因为发生反应:
溶液也可以做洗涤剂,因为发生反应: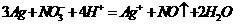 你认为
你认为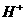 是由什么反应提供的(用离子方程式表示):
。
是由什么反应提供的(用离子方程式表示):
。
[点晴] (1)增大c( )或降低
)或降低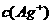 (2)
(2)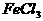 ;因为AgCl难溶,
;因为AgCl难溶,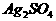 微溶。因此在
微溶。因此在 将Ag氧化为
将Ag氧化为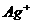 后,
后,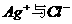 反应产生AgCl沉淀,
反应产生AgCl沉淀,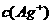 被降低的程度大,更有利于使平衡向右移动。(3)
被降低的程度大,更有利于使平衡向右移动。(3)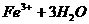
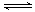
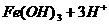
本题涉及平衡移动原理的考察。(1)若使该平衡向右移动,要么是增大反应物的浓度,要么是减少生成物的浓度,所以可以回答增大c( )或降低
)或降低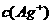 (2)两种溶液谁优谁劣,就要比较两种溶液的不同,氯化铁溶液中是氯离子,硫酸铁溶液中是硫酸根离子,进而想到AgCl难溶,
(2)两种溶液谁优谁劣,就要比较两种溶液的不同,氯化铁溶液中是氯离子,硫酸铁溶液中是硫酸根离子,进而想到AgCl难溶,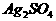 微溶。再根据平衡移动原理选用氯化铁溶液。(3)
微溶。再根据平衡移动原理选用氯化铁溶液。(3) 溶液水解显酸性。要擅于把平衡移动原理和化学事实联系起来,比如平衡移动原理可用于电离平衡、水解平衡,溶解平衡等可逆反应。
溶液水解显酸性。要擅于把平衡移动原理和化学事实联系起来,比如平衡移动原理可用于电离平衡、水解平衡,溶解平衡等可逆反应。
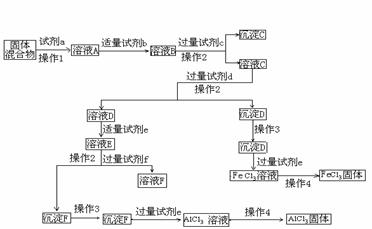
[点题] 固体AlCl3和FeCl3混合物中含有少量FeCl2和Al2(SO4)3。某同学设计如下实验进行分离,以分别得到纯净的AlCl3和FeCl3固体。回答下列问题:
(1) 写出下列试剂的名称:试剂c___________, 试剂d__________,试剂f ,
(2) 操作3是 ,具体操作是 ;
操作4是 ,操作时应注意的问题是_______ ;
(3) 加入试剂b的目的是_________________________________________ ,判断试剂b适量的方法是____________________________________________________________。
(4) 由溶液D转变成溶液E的操作中,判断加入的试剂e适量的依据是____________________________________________________________________。
(5) 溶液E中的溶质有:_________________________________。其中杂质是否要另加试剂除去__________(填“是”或“否”),原因是_______________________________;
(6) 有同学认为上述实验中最后得到AlCl3和FeCl3固体的步骤不科学,他的理由是:____________________________________________________________________。
[点晴]
(1) 氯化钡溶液 氢氧化钠溶液 氨水
(2) 洗涤沉淀 向过滤器中注入蒸馏水至浸没沉淀,用玻璃棒轻轻搅拌,至水流尽.重复数次 蒸发溶液 边加热边搅拌,至出现较多的晶体时停止加热.
(3) 使Fe2+氧化为Fe3+ 取少量溶液B,向其中滴加溴水溶液,看是否褪色,若不褪色,则说明已适量
(4) 生成的沉淀刚好溶解
(5) AlCl3 BaCl2 NaCl 否 在E中加入氨水后过滤,杂质自然分离
(6)
 未在酸性氛围中蒸发AlCl3、 FeCl3会部分水解而得不到纯净的AlCl3
、FeCl3固体
未在酸性氛围中蒸发AlCl3、 FeCl3会部分水解而得不到纯净的AlCl3
、FeCl3固体
[点题] “化学多米诺实验”即利用反应中气体产生的压力和虹吸作用原理,使若干化学实验依次发生,整个过程只须控制第一个反应,就好像多米诺骨牌游戏一样.右图就是一个“化学多米诺实验”.
各装置中试剂或物质是:A.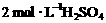 B.Zn C.
B.Zn C.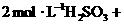
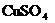 D.Zn E.
D.Zn E.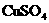 溶液 F.
溶液 F.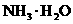 G.
G.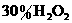 H.
H.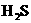 溶液 I.NaOH溶液已知:
溶液 I.NaOH溶液已知: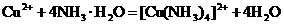 该反应产物可作为
该反应产物可作为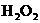 分解的催化剂.请回答下列问题:
分解的催化剂.请回答下列问题:
(1)进行实验前必须进行的操作________________________________________.
(2)B与D两容器中反应速率比较B______D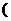 填>、<、=
填>、<、=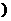 原因是____________.
原因是____________.
(3)H中的现象是_________________________________________________________.
(4)I的作用是(用化学方程式表示)___________________________________.
(5)A和B之间导管a的作用是_________________________________________.
(6)在该实验中不涉及的反应类型是(填序号)______.①分解反应②化合反应③置换反应④复分解反应
[点晴] (1)检查装置气密性
(2)<;D中Zn与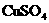 发生反应覆盖在Zn表面形成原电池,从而使反应速率加快
发生反应覆盖在Zn表面形成原电池,从而使反应速率加快
(3)有气泡并有乳白色(或浅黄色)浑浊.
(4)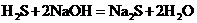
(5)平衡烧瓶(B)和漏斗(A)的气压,使液体易于流下 (6)B
[点题]现有分子式均为C3H6O2的四种有机物A、B、C、D,且分子中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
|
|
NaOH溶液 |
银氨溶液 |
新制Cu(OH)2 |
金属钠 |
|
A |
中和反应 |
-- |
溶 解 |
产生氢气 |
|
B |
-- |
有银镜 |
加热后有红色沉淀 |
产生氢气 |
|
C |
水解反应 |
有银镜 |
加热后有红色沉淀 |
-- |
|
D |
水解反应 |
-- |
-- |
-- |
则A、B、C、D的结构简式分别为:
A ,B ,C ,D 。
[点晴] A.CH3CH2COOH B.CH3CHOHCHO C.HCOOCH2CH3 D.CH3COOCH3
这题是考查常见官能团的性质,A 与NaOH溶液发生中和反应,会使新制Cu(OH)2溶解,与金属钠产生氢气可以说明A为羧酸,B与银氨溶液有银镜产生,与金属钠产生氢气说明有醛基和羟基,可能写出B为CH3CHOHCHO,C与NaOH溶液发生水解反应,与银氨溶液有银镜产生,说明C为酯类而且是甲酸酯,所以C为HCOOCH2CH3。D只能与NaOH溶液发生水解反应,说明D为酯类写出D为CH3COOCH3。此题说明学有机化学一定要抓住官能团的性质。羟基、醛基、羧基、酯基等官能团有什么特殊的性质一定要记住,而且要会区分醇羟基、酚羟基、羧羟基。
18、Cl、S、N、C、P、Na、Mg、Al、Fe等元素的单质及化合物(近10年来的化学高考命题中的呈现率:100%)
 [点题](1)Na投入到NH4Cl 溶液中放出的气体是__________________________。
[点题](1)Na投入到NH4Cl 溶液中放出的气体是__________________________。
(2)今有A、B、C、D四种钠盐。当其物质的量浓度相等时,溶液的pH值依次增大,已知:
又知F气体对空气的相对密度为1.517,请填写下列物质的化学式(E、F也分别是两种物质的代号) A_____________,B_____________,C_____________,D_____________。
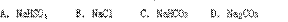 [点晴] (1)H2、NH3 (2)
[点晴] (1)H2、NH3 (2)
 [点题]甲、乙、丙、丁分别是NaAlO2、NaOH、HCl、 -ONa 四种溶液中的一种.若将甲溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加甲溶液则沉淀逐渐增多,而后又逐渐溶解,甲溶液滴入丁溶液时,无明显现象发生,据此可推断丙物质是
[点题]甲、乙、丙、丁分别是NaAlO2、NaOH、HCl、 -ONa 四种溶液中的一种.若将甲溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加甲溶液则沉淀逐渐增多,而后又逐渐溶解,甲溶液滴入丁溶液时,无明显现象发生,据此可推断丙物质是
 A.NaAlO2 B.NaOH
C.HCl D. -ONa
A.NaAlO2 B.NaOH
C.HCl D. -ONa
[点晴] D 。
[点题]A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,甲、乙、丙为常见化合物。它们之间有如下转化关系:
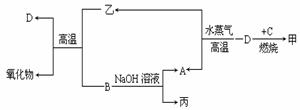
回答下列问题:
(1)A的电子式_________________________。
(2)D与甲溶液反应的化学方程式______________________________________。
(3)丙的水溶液显____________性(填酸或碱),原因是(用离子方程式表示)________(4)一定条件下,2 mol B与3 mol D的氧化物W恰好反应,则W的化学式________。

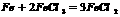 [点晴] (1)H:H(2)
(3)碱; (4)FeO
[点晴] (1)H:H(2)
(3)碱; (4)FeO
2.在钛酸钡晶体中一个钛(Ti)原子紧邻的氧原子有多少个?
[点晴]化学式为BaTiO3;Ti原子处于立方体的顶点上,为8个晶格共用,与之紧邻的O原子正处于经过Ti原子的6个晶胞的6条棱上,因此一个Ti原子紧邻的氧原子有6个。
1. 钛酸钡的化学式。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com