
题目列表(包括答案和解析)
6、下列能正确表示反应的离子方程式的是( )
A、FeCl3溶液的水解:Fe3+ + 3H2O = Fe(OH)3↓+ 3H+
B、氯化钡溶液与碳酸钠溶液反应:Ba2++CO32- =BaCO3
C、硫化亚铁与盐酸反应:FeS+2H+=Fe2+ +H2S
D、氯气通入碘化钾溶液中:Cl2 + 2I- =I2 + 2Cl-
5、下列能正确表示反应的离子方程式的是( )
A、铜与浓硫酸反应放出SO2:Cu + 4H++SO42-=Cu2++SO2↑+2H2O
B、浓硫酸与食盐共热制HCl写成:Cl- + H+ = HCl↑
C、浓盐酸与二氧化锰反应制氯气:MnO2 + 4H+ +2Cl- = Mn2+ + 2H2O + Cl2↑
D、加热NH4Cl和氢氧化钠固体混合物:NH4+ + OH- = NH3↑ + H2O
4、下列反应的离子方程式书写正确的是( )
A、CuSO4溶液加入过量氢氧化钡溶液:Ba2+ + SO42- = BaSO4↓
B、碳酸氢铵溶液与过量氢氧化钠溶液混合:HCO3- + OH- = CO32- + H2O
C、稀硫酸中滴加氢氧化钡溶液:H++OH- =H2O
D、硫酸氢钠溶液中加入碳酸氢钠溶液:H+ + HCO3- = CO2↑+H2O
3、下列反应的离子方程式错误的是( )
A、澄清石灰水跟稀硝酸反应:H++OH- = H2O
B、磷酸与氢氧化钾溶液反应:H++OH- = H2O
C、醋酸铵和盐酸反应:CH3COO- + H+ = CH3COOH
D、碳酸钙溶于硝酸中:CaCO3 + 2H+ = Ca2+ + H2O + CO2↑
2、下列反应的离子方程式书写正确的是( )
A、苛性钾溶液中加入稀醋酸:H++OH- = H2O
B、碳酸钠加入稀盐酸:Na2CO3+2H+ = 2Na+ +CO2↑+H2O
C、氧化钠溶于盐酸中: Na2O+2H+ = 2Na++H2O
D、氯气通入冷水中: Cl2+H2O = 2H++Cl- + ClO-
1、 下列反应的离子方程式书写正确的是( )
A、 铁和稀硫酸反应:2Fe+6H+ = 2Fe3++3H2↑
B、氯化亚铁溶中通入氯气:Fe2++Cl2=Fe3++Cl-
C、往水中投入一小块金属钠:Na+2H2O=Na++2OH-+H2个
D、铝粉溶于NaOH溶液中:2Al +2OH-+2H2O=2AlO2-+3H2↑
26.(10分)某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为两者反应生成只有CuCO3一种沉淀;
乙同学认为这两者相互促进水解反应,生成Cu(OH)2一种沉淀;
丙同学认为生成CuCO3和Cu(OH)2两种沉淀。(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.按照乙同学得理解Na2CO3溶液和CuSO4溶液反应的化学反应方程式为 ;
在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为①过滤②洗涤③干燥。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。
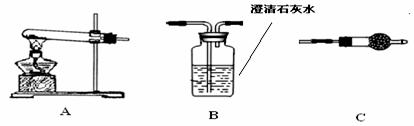

 (1)各装置连接顺序为
。
(1)各装置连接顺序为
。
(2)装置C中装有试剂的名称是 。
(3)能证明生成物中有CuCO3的实验现象是 。
Ⅲ.若CuCO3和Cu(OH)2两者都有,可通过下列所示装置进行定量分析来测定其组成。
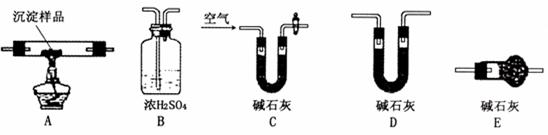
(1)装置C中碱石灰的作用是 ,实验开始时和实验结束时都要通入过量的空气其作用分别是 (2)若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为- 。
25. (8分)已知A、B、C、D分别代表中学化学常见物质(或微粒),其中A、B均为两种元素组的化合物(或微粒),相互转化关系如下(有关反应条件已略去)。
 请根据题目要求回答有关问题:
请根据题目要求回答有关问题:
(1)若A、B两化合物相互反应得到气体单质C和化合
物D,则化学方程式为(只写一个):
;
(2)若A、B两化合物相互反应生成非金属固体单质C和化合物D,且A的相对分子质量大于B,则A、B的化学式为:A 、B ;
(3)若A为5个原子构成的微粒,且A、B均为10电子微粒,含适量A、B微粒的溶液在加热条件下反应生成气体C和化合物D,含A、B微粒的溶液转化为C、D的离子方程式为: 。
24.(12分)粗盐提纯的研究。[有关资料]
|
化学式 |
CaCO3 |
CaSO3 |
CaC2O4 |
Mg(OH)2 |
|
Ksp |
4.96×10-9 |
4.96×10-9 |
2.34×10-9 |
5.61×10-12 |
某研究性学习小组对粗盐的提纯和检验进行研究,并提出一些新的方案。已知该粗盐样品中主要含有不溶性杂质、Mg2+、Ca2+等(忽略SO42-的存在),该小组设计流程如下:
 [设计除杂过程]
[设计除杂过程]
(1)操作①中需要使用的玻璃仪器有 、 。操作②的名称为 。
(2)混合液A的主要成分是 。(填化学式)
[检验除杂效果]
(3)为检验溶液B中Mg2+、Ca2+是否除尽,通常分别取少量溶液B于两支试管中,进行如下实验:步骤一:检验Mg2+是否除尽。向其中一支试管中加入 溶液(填化学式),看是否有沉淀生成。步骤二:检验Ca2+是否除尽。向另一支试管中加入某溶液,看是否有沉淀生成。效果最好的是 (填字母)。A.Na2CO3 B.Na2SO3 C.Na2C2O4
[获取纯净食盐]
(4)对溶液B加热并不断滴加6 mol·L-1的盐酸溶液,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C,该操作的目的是 。
(5)将溶液C倒入 (填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到 时(填现象),停止加热。
[问题讨论]
(6)在除杂过程中,向粗盐悬浊液中加混合液A,该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在 以下。
23.(6分)2009年3月底至4月中旬,墨西哥、美国等多国接连暴发甲型H1N1 型流感疫情,防控专家表示,含氯消毒剂和过氧化物消毒剂可防甲型H1N1流感。
(1)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3 和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳 酸钠只发生了还原反应的是 ;A.MnO2 B.KMnO4 溶液 C.稀盐酸D.Na2SO3 溶液
(2)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3 在H2SO4存在下与Na2SO3 反应制得。请写出反应的离子方程式(不必配平): ;
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2 → ClO2↑+ H+ +Cl-+H2O(未配平)。当1 mol HClO2 发生分解反应时,转移的电子个数是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com