
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
6. A”¢B”¢CŹĒ³£¼ūµ„ÖŹ£¬X”¢Y”¢ZŹĒŃõ»ÆĪļ£¬ĖüĆĒÖ®¼äÓŠČēĶ¼ĖłŹ¾×Ŗ»Æ¹ŲĻµ£ŗ
A”¢B”¢CŹĒ³£¼ūµ„ÖŹ£¬X”¢Y”¢ZŹĒŃõ»ÆĪļ£¬ĖüĆĒÖ®¼äÓŠČēĶ¼ĖłŹ¾×Ŗ»Æ¹ŲĻµ£ŗ
ĒėŠ“³ö·ūŗĻĻĀĮŠŅŖĒóµÄ»Æѧ·½³ĢŹ½£ŗ
””(1)ČōXĪŖCO2£¬BĪŖŗģÉ«¹ĢĢ壬Ōņ£ŗ
”””” ·“Ó¦¢Ł____________________”£ ·“Ó¦¢Ś_________________”£
(2)ČōXĪŖFe3O4£¬AĪŖŅų°×É«¹ĢĢ壬Ōņ£ŗ
”””” ·“Ó¦¢Ł____________________”£ ·“Ó¦¢Ś_________________________”£
5. Ķ¼ÖŠA-LĖł“ś±ķµÄø÷ĪļÖŹŹĒ֊ѧ»ÆѧĄļ³£¼ūµÄĪļÖŹ£¬ŅŃÖŖB”¢JŹĒµ„ÖŹ”£AŹĒ»ÆŗĻĪļ£»EµÄČÜŅŗøś±½·ÓČÜŅŗ»ģŗĻ£¬ČÜŅŗ³Ź×ĻÉ«”£A-Lø÷ĪļÖŹÖ®¼äĻą»„·“Ó¦×Ŗ»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾(Ī“×¢Ć÷±ŲŅŖµÄ·“Ó¦Ģõ¼ž)
Ķ¼ÖŠA-LĖł“ś±ķµÄø÷ĪļÖŹŹĒ֊ѧ»ÆѧĄļ³£¼ūµÄĪļÖŹ£¬ŅŃÖŖB”¢JŹĒµ„ÖŹ”£AŹĒ»ÆŗĻĪļ£»EµÄČÜŅŗøś±½·ÓČÜŅŗ»ģŗĻ£¬ČÜŅŗ³Ź×ĻÉ«”£A-Lø÷ĪļÖŹÖ®¼äĻą»„·“Ó¦×Ŗ»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾(Ī“×¢Ć÷±ŲŅŖµÄ·“Ó¦Ģõ¼ž)
Ēė»Ų“š£ŗ
(1)BŌŚAµÄÅØČÜŅŗÖŠ·“Ó¦¶ųČܽāµÄĢõ¼žŹĒ_______________£¬
¶ų³£ĪĀĻĀBŌŚAµÄÅØČÜŅŗÖŠÄŃŅŌ·“Ó¦µÄŌŅņŹĒ_______________”£
(2)Š“³öĻĀĮŠ»Æѧ·½³ĢŹ½£ŗ
F”śG+A__________£»”””””” G”śF______________£»E”śIµÄĄė×Ó·½³ĢŹ½_________________”£
(3)L×Ŗ»Æ³ÉIµÄĻÖĻóŹĒ______________”£
4. ČēĶ¼ĖłŹ¾µÄĪļÖŹµÄ×Ŗ»Æ¹ŲĻµÖŠ£¬AŹĒŅ»ÖÖ¹ĢĢåµ„ÖŹ£¬EŹĒŅ»ÖÖ°×É«³Įµķ”£¾ŻĶ¼ĢīŠ“”£
ČēĶ¼ĖłŹ¾µÄĪļÖŹµÄ×Ŗ»Æ¹ŲĻµÖŠ£¬AŹĒŅ»ÖÖ¹ĢĢåµ„ÖŹ£¬EŹĒŅ»ÖÖ°×É«³Įµķ”£¾ŻĶ¼ĢīŠ“”£
””(1)BµÄ»ÆѧŹ½ŹĒ________£¬ÄæĒ°BŅѱ»ÓĆ×÷________µÄÖ÷ŅŖŌĮĻ”£
(2)BŗĶaČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ________________________________________”£
(3)AŗĶaČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ________________________________________”£
(4)CŗĶ¹żĮæŃĪĖį·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ______________________________________”£
3. Ķ¼ÖŠĆæøö·½æņ±ķŹ¾ÓŠ¹ŲµÄŅ»ÖÖ·“Ó¦Īļ»ņÉś³ÉĪļ£¬·½æņÖŠ×ÖÄøŹĒĪļÖŹ“śŗÅ£¬ŅŃÖŖB”¢D”¢E”¢F”¢X¾łĪŖµ„ÖŹ£¬ÅŠ¶Ļ²¢»Ų“šĻĀĮŠĪŹĢā£ŗ
Ķ¼ÖŠĆæøö·½æņ±ķŹ¾ÓŠ¹ŲµÄŅ»ÖÖ·“Ó¦Īļ»ņÉś³ÉĪļ£¬·½æņÖŠ×ÖÄøŹĒĪļÖŹ“śŗÅ£¬ŅŃÖŖB”¢D”¢E”¢F”¢X¾łĪŖµ„ÖŹ£¬ÅŠ¶Ļ²¢»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Š“³öA”¢BµÄ»ÆѧŹ½£ŗA ________£»B ________”£
(2)Š“³öIŗĶJ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ________________”£
(3)Š“³öCČÜŅŗŗĶD»ņX·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ ________________________________________”£
2. “ÓijĪļÖŹAµÄĖ®ČÜŅŗ³ö·¢ÓŠČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ
“ÓijĪļÖŹAµÄĖ®ČÜŅŗ³ö·¢ÓŠČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Š“³öC”¢D”¢EµÄ»ÆѧŹ½£ŗC_________________£¬D________________£¬E________________”£
(2)¼ģŃéBČÜŅŗÖŠŅõĄė×ӵďµŃé²Ł×÷ŗĶŹµŃéĻÖĻóŹĒ___________________________________”£
(3)Š“³öĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½¢ŁAÓė×ćĮæNaOHČÜŅŗ(¼ÓČČ)______________________”£
¢ŚC”¢D°“Ģå»ż±Č1:1ĶØČĖĖ®ÖŠ£ŗ_____________”£¢ŪA+H2O2£ŗ_______________________”£
1.¶ĢÖÜĘŚµÄČżÖÖŌŖĖŲX”¢Y”¢Z£¬Ō×ÓŠņŹżŅĄ“Ī±äŠ”£¬Ō×ÓŗĖĶāµē×Ó²ćŹżÖ®ŗĶŹĒ5”£XŌŖĖŲŌ×Ó×īĶā²ćÉĻµÄµē×ÓŹżŹĒYŗĶZĮ½ŌŖĖŲŌ×Ó×īĶā²ćÉĻµÄµē×ÓŹżµÄ×ÜŗĶ£»YŌŖĖŲŌ×ÓµÄ×īĶāµē×Ó²ćÉĻµÄµē×ÓŹżŹĒĖüµÄµē×Ó²ćŹżµÄ2±¶£¬XŗĶZæÉŅŌŠĪ³ÉXZ3µÄ»ÆŗĻĪļ”£Ēė»Ų“š£ŗ
”””” (1)XŌŖĖŲµÄĆū³ĘŹĒ________£¬YŌŖĖŲµÄĆū³ĘŹĒ________£»ZŌŖĖŲµÄĆū³ĘŹĒ________”£
”””” (2)XZ3»ÆŗĻĪļµÄ·Ö×ÓŹ½ŹĒ________________£¬µē×ÓŹ½ŹĒ________________”£
(3)·Ö±šŠ“³öX”¢YµÄŗ¬ŃõĖįµÄ·Ö×ÓŹ½________________”¢________________”£
””[Ąż1]A”¢B”¢C”¢D”¢E”¢FĪŖŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄÖ÷×åŌŖĖŲ£¬ŅŃÖŖA”¢C”¢FČżŌ×ÓµÄ×īĶā²ć¹²ÓŠ11øöµē×Ó£¬ĒŅÕāČżÖÖŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖ®¼äĮ½Į½½ŌÄÜ·“Ó¦£¬¾łÄÜÉś³ÉŃĪŗĶĖ®£¬DŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ӱȓĪĶā²ćµē×ÓŹżÉŁ4£¬EŌŖĖŲŌ×Ó“ĪĶā²ćµē×ÓŹż±Č×īĶā²ćµē×ÓŹż¶ą3”£Ēė»Ų“š£ŗ
””¢ŁŠ“³öĻĀĮŠŌŖĖŲµÄ·ūŗÅ£ŗA________£¬D________£¬E________”£
¢ŚÓƵē×ÓŹ½±ķŹ¾B”¢FŠĪ³É»ÆŗĻĪļµÄ¹ż³Ģ____________________________________________”£
””¢ŪA”¢CĮ½ÖÖŌŖĖŲ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ___________________________”£
””¢ÜDµÄ¹ĢĢ¬Ńõ»ÆĪļŹĒ________¾§Ģ壬ŗ¬n mol DµÄŃõ»ÆĪļµÄ¾§ĢåÖŠŗ¬D-O¹²¼Ū¼üĪŖ________mol”£
 [Ąż2]X”¢Y”¢ZĪŖ³£¼ūµÄČżÖÖµ„ÖŹ”£³£ĪĀĻĀXŹĒ¹ĢĢ壬YŹĒŅŗĢ壬ZŹĒĪŽÉ«ĘųĢ唣Ęä·“Ó¦¹ŲĻµČēĶ¼12-1ĖłŹ¾£®ĘäÖŠBµÄČÜŅŗĻŌĒæĖįŠŌ”£
[Ąż2]X”¢Y”¢ZĪŖ³£¼ūµÄČżÖÖµ„ÖŹ”£³£ĪĀĻĀXŹĒ¹ĢĢ壬YŹĒŅŗĢ壬ZŹĒĪŽÉ«ĘųĢ唣Ęä·“Ó¦¹ŲĻµČēĶ¼12-1ĖłŹ¾£®ĘäÖŠBµÄČÜŅŗĻŌĒæĖįŠŌ”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)øł¾ŻÉĻŹö¹ŲĻµ£¬Č·¶ØX”¢Y”¢ZµÄ»ÆѧŹ½£ŗX________£¬Y________£¬Z________”£
(2)YŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ________”£
(3)Š“³öAČÜÓŚĖ®ŗó¼ÓČėXµÄĄė×Ó·½³Ģ___________________________________________”£
(4)Š“³öCµÄČÜŅŗÖŠĶØČė¹żĮæĀČĘųµÄĄė×Ó·½³Ģ____________________________________”£
[Ąż3]X”¢Y”¢ZĪŖČżøö²»Ķ¬¶ĢÖÜĘŚ·Ē½šŹōŌŖĖŲµÄµ„ÖŹ”£
ŌŚŅ»¶ØĢõ¼žĻĀÓŠČēĻĀ·“Ó¦£ŗY+X”śA(Ęų)£¬Y+Z”śB(Ęų)”£ĒėÕė¶ŌŅŌĻĀĮ½ÖÖ²»Ķ¬Ēéæö»Ų“š£ŗ
(1)Čō³£ĪĀĻĀX”¢Y”¢Z¾łĪŖĘųĢ壬ĒŅAŗĶB»ÆŗĻÉś³É¹ĢĢåCŹ±ÓŠ°×ŃĢ²śÉś£¬Ōņ£ŗ
¢ŁYµÄ»ÆѧŹ½ŹĒ____________£»
¢ŚÉś³É¹ĢĢåCµÄ»Æѧ·½³ĢŹ½ŹĒ_________________________”£
(2)Čō³£ĪĀĻĀ£¬YĪŖ¹ĢĢ壬X”¢ZĪŖĘųĢ壬AŌŚæÕĘųÖŠ³ä·ÖČ¼ÉÕæÉÉś³ÉB£¬Ōņ£ŗ
¢ŁBµÄ»ÆѧŹ½ŹĒ________________£ŗ
¢ŚĻņæĮŠŌÄĘČÜŅŗÖŠĶØČė¹żĮæµÄA£¬Ėł·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗ________________________”£
¢Ū½«YÓė(1)֊ijµ„ÖŹµÄĖ®ČÜŅŗ³ä·Ö·“Ó¦æÉÉś³ÉĮ½ÖÖĒæĖį£¬
øĆ·“Ó¦µÄ»Æѧ·½³Ģ__________________________________________________________”£
[Ąż4]A”¢B”¢C”¢DŹĒĖÄÖÖæÉČܵĻÆŗĻĪļ£¬·Ö±šÓÉŃōĄė×ÓK+”¢Ba2+”¢A13+”¢Fe3+ŗĶŅõĄė×ÓOH-”¢CO23-”¢NO3-”¢SO42-Į½Į½×éŗĻ¶ų³É£¬ĖüĆĒµÄČÜŅŗ·¢ÉśČēĻĀ·“Ó¦£ŗ
AÓėB·“Ӧɜ³É°×É«³Įµķ£¬ŌŁ¼Ó¹żĮæA£¬³ĮµķĮæ¼õÉŁ£¬µ«²»»įĶźČ«ĻūŹ§£»
CÓėD·“Ӧɜ³ÉÓŠÉ«³Įµķ£ŗ”””””” BÓėC·“Ӧɜ³É°×É«³Įµķ”£
Š“³öĖüĆĒµÄ»ÆѧŹ½£ŗA£ŗ__________”” B£ŗ__________C£ŗ__________”” D£ŗ__________
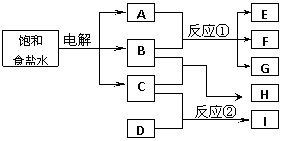 [Ąż5]ĻĀĶ¼ĆæŅ»·½æņÖŠµÄ×ÖÄø“ś±ķŅ»ÖÖ·“Ó¦Īļ»ņÉś³ÉĪļ£ŗ
[Ąż5]ĻĀĶ¼ĆæŅ»·½æņÖŠµÄ×ÖÄø“ś±ķŅ»ÖÖ·“Ó¦Īļ»ņÉś³ÉĪļ£ŗ
|
”” |
C |
D |
I |
|
ĘšŹ¼×é³É£Æmol |
6 |
4 |
0 |
|
ijŹ±æĢ×é³É£Æmol |
3 |
3 |
2 |
ĪļÖŹAøśB·“Ӧɜ³ÉĪļÖŹE”¢FŗĶG£»ĪļÖŹCøśD·“Ӧɜ³ÉĪļÖŹI£¬Ä³ĪĀ¶ČĻĀøĆ·“ӦʚŹ¼ŗĶijŹ±æĢµÄ·“Ó¦»ģŗĻĪļ×é³ÉČēÓŅÉĻ±ķøńĖłŹ¾”£ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ
¢ŁĪļÖŹHµÄ»ÆѧŹ½ŹĒ________________________________£»
¢Ś·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½ŹĒ_______________________________________________________£»
¢Ū·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½(Šė×¢Ć÷·“Ó¦Ģõ¼ž)ŹĒ________________________________________”£
3”¢½āĢāĖ¼Ā·Óė·½·Ø

ĪŽ»śĶʶĻĢāµÄ»ł±¾¶ØĪ»ŹĒ£ŗ“ś±ķŌŖĖŲ”°8+4”±£¬¼“֊ѧ»ÆѧѧĻ°µÄŌŖĖŲ“ś±ķ£ŗ
8ÖÖ·Ē½šŹō(H”¢C”¢Si”¢N”¢P”¢O”¢S”¢Cl)ŗĶ4ÖÖ½šŹō(Na”¢Mg”¢AlŗĶFe)”£
¶ŌÕāŠ©ŌŖĖŲµÄ”°Ī»”¢¹¹”¢ŠŌ”±¼°ĖüĆĒµÄµ„ÖŹ”¢»ÆŗĻĪļµÄ”°ŠŌ”¢ÓĆ”¢ÖĘ”±ŅŖøųÓčø߶ȵÄÖŲŹÓ”£
”°Ķ»ĘĘæŚ”±µÄÖŲŅŖŅĄ¾ŻŹĒ£ŗ
¢ŁĢŲŹāµÄŃÕÉ«(°üĄØ»šŃęµÄŃÕÉ«ŗĶĪļÖŹµÄŃÕÉ«)£»
¢ŚĪØŅ»µÄĻÖĻó(ČēNH3Ź¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£¬NOŌŚæÕĘųÖŠ±äŗģ×ŲÉ«£¬H2SµÄ³ō¼¦µ°ĘųĪ¶)£»
¢ŪĢŲŹāµÄŹµŃé(ČēNH3ÓėHCl»ņHNO3²śÉś°×ŃĢŅŌ¼°ø÷ÖÖĢŲŹāµÄĻŌÉ«·“Ó¦µČµČ)£»
¢ÜĪØŅ»µÄŠŌÖŹ(ČēFĪŽÕż¼Ū£¬Ēā·śĖįæÉŅŌµńæĢ²£Į§£¬³£ĪĀĻĀĪŖŅŗĢ¬µÄ·Ē½šŹōµ„ÖŹŹĒäåµČ)”£
””ŌŚ½āĢāŹ±ŅŖ×¢Ņā£ŗ
””¢ŁÉóĆ÷ĢāŅā£¬Ć÷Č··¶Ī§£¬×¢ŅāĢāÖŠŹĒ·ńøų³öĮĖĻŽÖĘĢõ¼ž£»
””¢Ś½ōæŪĻÖĻó£¬ÕżČ·ÅŠ¶Ļ£¬ĢŲ±šŹĒÓŠĻŽÖĘĢõ¼žµÄĢāÄæµ±µĆ³ö½įĀŪŹ±£¬ŅŖ¼ģŃéŹĒ·ńÓŠŅņ²»Äܹ²“ę¶ųÓ¦ÓčŅŌ·ń¶ØµÄ½įĀŪ£»
¢ŪŅŖ×¢ŅāĢāÉčĖłøųµÄŹż¾Ż¶ŌĶʶĻ½įĀŪµÄÓ°Ļģ£¬²¢Äܹ»ÉĘÓŚŌĖÓĆĖłøųŹż¾Ż½ųŠŠøØÖśĶʶĻ”£
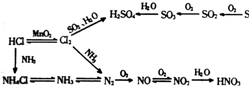
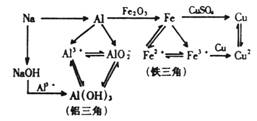
1”¢ÖŲŅŖµÄ·Ē½šŹōµ„ÖŹ¼°Ęä»ÆŗĻĪļÖ®¼äµÄ¹ŲĻµ”” 2”¢ÖŲŅŖµÄ½šŹōµ„ÖŹ¼°Ęä»ÆŗĻĪļÖ®¼äµÄ¹ŲĻµ
 ””””
”””” 
11”¢²¬µē¼«µē½ā1LCu(NO3)2ŗĶKNO3»ģŗĻČÜŅŗ,ĶصēŅ»¶ĪŹ±¼ä,Į½¼«¾ł²śÉś11.2L(S.T.P)ĘųĢå.Ēóµē½āŗóČÜŅŗµÄpH”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com