
题目列表(包括答案和解析)
4、关于非金属元素N、O、Cl、P的叙述,正确的是( )
A.在通常情况下其单质均为气体 B.其单质均由双原子分子构成
C.都属于主族元素 D.每种元素仅生成一种氢化物
3、下列广告用语在科学上没有错误的是………… ( )
A.这种饮料中不含任何化学物质
B.这种蒸馏水绝对纯净,其中不含任何离子
C.这种口服液含有丰富的氮、磷、锌等微量元素
D.没有水就没有生命
2、已知自然界中氧的同位素有16O、17O、18O,氧的同位素
有H、D,从水分子的组成来看,自然界的水一共有………………( )
A.3种 B.6种
C.9种 D.12种
18.现在一定条件下进行下列可逆反应的实验A(g)+2B(g) 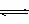 3C(g);△H<O平行三组实验的有关条件如表:
3C(g);△H<O平行三组实验的有关条件如表:
|
反应条件 |
温度(O℃) |
容器体积 |
起始n(A) |
起始n(B) |
其他条件 |
|
I |
500 |
1 L |
1 mol |
2 mol |
无 |
|
Ⅱ |
500 |
1 L |
2 mol |
4 mol |
无 |
|
Ⅲ |
500 |
1 L |
1 mol |
2 mol |
有 |
已知I组实验过程中,C气体的体积分数Vc%随时间t的变化曲线如图:
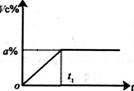
(1)试在图中画出Ⅱ组实验过程中C气体体积分数随时间t的变化曲线。
(2)若Ⅲ组实验过程中,C气体体积分数随时间t的变化曲线与Ⅱ组相当,则它所具备的“其他条件”可能是 。
(3)在I组实验中B气体的转化率是 ,若将实验温度变为800℃,则达到平衡所需时间 t1,(小于、大于、等于),平衡时Vc% a%(小于、大于、等于)。
17.在一定温度下,对于反应2A(g)+B(g)  2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图所示,从t1时间开始对反应体系升高温度,n(C)的变化如图所示。试回答下列问题:
2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图所示,从t1时间开始对反应体系升高温度,n(C)的变化如图所示。试回答下列问题:
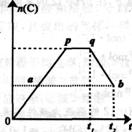
(1)p点反应的V正 V逆(填“<”“>”或“=”);
(2)此反应的正反应为 热反应(填“放”或“吸”);
(3)a、b两点的正反应速率;Va Vb(填“>”“<”或“=”)。
16.化学工业在江苏国民经济中占有极其重要的地位.我省是国内最早的硫酸生产基地之一。
(1)硫酸生产中,根据化学平衡原理来确定的条件或措施有 (填序号)。
A. 矿石加入沸腾炉之前先粉碎
B.使用V2O5作催化剂
C.接触室中不使用很高的温度
D.净化后炉气中要有过量的空气
E.接触氧化在常压下进行
F.吸收塔中用98.3%的浓硫酸吸收S03
(2)若实验在537℃、1.01x105 Pa和催化剂存在条件下,向某密闭容器中充入1 mol SO2和0.5 molO2,此时体积为100 L,在温度和压强不变条件下反应达到平衡,SO3体积分数为0.91。若保持温度和压强不变,充入1 mol SO3则平衡时SO2体积分数为 ;若保持温度和压强不变,充入a mol S02和b molO2,且a:b=2:1.反应达平衡时SO3体积分数仍为0.91,则a= 。
(3)硫酸工业的尾气中含有少量的SO2,常用氨水吸收后再加硫酸,回收S02同时得到化肥硫酸铵,硫酸铵溶液中各离子物质的量浓度由大到小的顺序为
15.已知某温度下的氟化氢气体中存在如下平衡关系:2H3F3 3H2F2;△H>O,H2 F2
3H2F2;△H>O,H2 F2 2HF;△H>0,则下面叙述正确的是 ( )
2HF;△H>0,则下面叙述正确的是 ( )
A.若气体平均相对分子质量为42,则H3F3的体积分数小于10%
B.若气体平均摩尔质量为40 g/mol,则H3F3的体积分数为10%
C.定温定容下再充入少量HF,则H3F3与HF的浓度比值增大
D.定温定容下再充入少量H3F3,则H3F3与HF的浓度比值减小
14.在423 K,体积相等的三个密闭容器A,B,C中分别加入amol HI,b mol HI,c mol 1:1的H2与I2(g)的混合气体,若a>b=c,分别达到平衡时,下列说法正确的是 ( )
A.从反应开始达到平衡所需的时间tA>tB
B.平衡时,I2的百分含量:A%=B%=C%
C.平衡时,c(I2)A=c(I2)B=c(I2)C
D.平衡时,各容器内的压强:PA>PB=PC
13.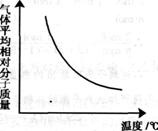 可逆反应2A+B
可逆反应2A+B 2C(g);△H<O。随温度变化气体平均相对分子质量如下图所示。则下列叙述正确的是 ( )
2C(g);△H<O。随温度变化气体平均相对分子质量如下图所示。则下列叙述正确的是 ( )
A.A和B可能都是固体
B. A和B一定都是气体
C.若B为固体则A一定为气体
D A和B可能都是气体 .
12.氙和氟按一定比例混合,在一定条件下反应,达到以下平衡:Xe(g)+2F2(g)  XeF4(g);△H>O。采取下列措施既能加快反应速率,又能使平衡向正反应方向移动的是 ( )
XeF4(g);△H>O。采取下列措施既能加快反应速率,又能使平衡向正反应方向移动的是 ( )
A.升温 B.加压 C.减压 D.适当降温
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com