
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
1ЁЂЁЁ ЮяжЪЕФСП(n)ЁЂФІЖћ
(1)ЮяжЪЕФСПгыФІЖћЕФЙиЯЕЃКЁАЮяжЪЕФСПЁБЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁАФІЖћЁБЪЧЁЁЁЁЁЁЁЁЁЁ ШчЙћдквЛЖЈСПЕФСЃзгЕФМЏЬхжаЫљКЌЕФСЃзгЪ§ФПгы0.012kg12CжаЫљКЌЕФЁЁЁЁЁЁЁЁ Ъ§ЯрЭЌЃЌдђИУМЏЬхЕФетИіСПжЕЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃФІЖћЕФСПЖШЖдЯѓЪЧЙЙГЩЮяжЪЕФЛљБОЮЂСЃ(ШчЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЕШ)ЛђЫќУЧЕФЬиЖЈзщКЯЁЃШч1molCaCl2,ПЩвдЫЕКЌ1molЁЁЁЁЁЁЁЁ ЃЌ2molЁЁЁЁЁЁ ЛђЁЁЁЁ molвѕЁЂбєРызгЃЌЛђКЌЁЁЁЁЁЁ molЕчзгЕШЁЃ
(2)зЂвтЃКдкЪЙгУФІЖћБэЪОЮяжЪЕФСПЪБЃЌгІИУгУЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ жИУїСЃзгЕФжжРрЃЌЖјВЛЪЙгУИУСЃзгЕФжаЮФУћГЦЃЌР§ШчЁА1molбѕЁБЪЧжИЁА1molбѕдзгЛЙЪЧ1molбѕЗжзгЃЌКЌвхВЛУїШЗЃЛгжШчЁА1molЬМдзгЁБЃЌЪЧжИ1mol12C,ЛЙЪЧ1mol13CЃЌКЌвхвВВЛУїШЗЁЃ
2.(04ФъНЫеИпПМЬт)ФГНсОЇЫЎКЯЮяКЌгаСНжжбєРызгКЭвЛжжвѕРызгЁЃГЦШЁСНЗнжЪСПОљЮЊ1.96gЕФИУНсОЇЫЎКЯЮяЃЌЗжБ№жЦГЩШмвКЁЃвЛЗнМгШызуСПBa(OH)2ШмвКЃЌЩњГЩАзЩЋГСЕэЃЌЫцМДГСЕэБфЮЊЛвТЬЩЋЃЌзюКѓДјгаКьКжЩЋЃЛМгШШИУЛьКЯЮяЃЌвнГіФмЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЕФЦјЬхЃЛгУЯЁбЮЫсДІРэГСЕэЮяЃЌОЯДЕгКЭИЩдяЃЌЕУЕНАзЩЋЙЬЬх2.33 gЁЃСэвЛЗнМгШыКЌ0.001 molKMnO4ЕФЫсадШмвКЃЌMnO4-ЧЁКУЭъШЋБЛЛЙдЮЊMn2+ЁЃ
ЁЁЁЁ ЧыЛиД№вдЯТЮЪЬтЃК
(1)ИУНсОЇЫЎКЯЮяжаКЌгаЕФСНжжбєРызгЪЧЁЁЁЁЁЁЁЁ КЭЁЁЁЁЁЁЁЁЁЁ ЃЌвѕРызгЪЧЁЁЁЁЁЁЁЁ ЁЃ
(2)ЪдЭЈЙ§МЦЫуШЗЖЈИУНсОЇЫЎКЯЮяЕФЛЏбЇЪНЁЃ
ЫМЮЌЗНЗЈ:ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁЮяжЪЕФСПКЭЦјЬхЕФФІЖћЬхЛ§ЛљДЁжЊЪЖ
1.(04ФъЩЯКЃИпПМЬт)ЩшNAЮЊАЂЗ№МгЕТТоГЃЪ§ЃЌЯТСаа№Ъіжае§ШЗЕФЪЧ
A.46 g NO2 КЭ N2O4ЛьКЯЦјЬхжаКЌгадзгЪ§ЮЊ3NA
B.БъзМзДПіЯТ22.4 L H2 жаКЌжазгЪ§ЮЊ2NA
C.1L 1mol/LДзЫсШмвКжаРызгзмЪ§ЮЊ2NA
D.1molMgгызуСПO2ЛђN2ЗДгІЩњГЩMgOЛђMg3N2ОљЪЇШЅ2NAИіЕчзгЁЁЁЁ
ЫМЮЌЗНЗЈ:ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
3.ЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЕФгаЙиМЦЫу
(1)ЛљБОМЦЫуЙиЯЕЃК M 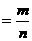
(2)БфЛЛМЦЫуЙиЯЕЃК
ЂйM =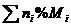
ЂкM =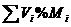
[Р§ЬтНтЮі]
ЁЁ[Р§1]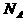 ДњБэАЂЗќМгЕТТоГЃЪ§ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
ДњБэАЂЗќМгЕТТоГЃЪ§ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
ЁЁЁЁ A. КЌ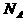 ИіHдзгЕФ
ИіHдзгЕФ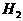 ЕФЮяжЪЕФСПЮЊ1mol
ЕФЮяжЪЕФСПЮЊ1mol
ЁЁ
ЁЁB. 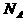 ИіCOЗжзгКЭ
ИіCOЗжзгКЭ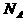 Иі
Иі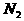 ЗжзгжЪСПОљЮЊ28g
ЗжзгжЪСПОљЮЊ28g
ЁЁ
ЁЁC. 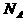 Иі
Иі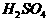 ЗжзгКЭ
ЗжзгКЭ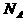 Иі
Иі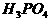 ЗжзгжаЫљКЌЧтдзгЕФИіЪ§БШЮЊ1:1
ЗжзгжаЫљКЌЧтдзгЕФИіЪ§БШЮЊ1:1
ЁЁ
ЁЁD. 5.6gбЧЬњРызгЕУЕН0.2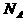 ИіЕчзгПЩБфГЩЬњдзг
ИіЕчзгПЩБфГЩЬњдзг
НтЬтЫМТЗ:ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
взДэЕу:ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
[Р§2]БъПіЯТЃЌmgЦјЬхAКЭngЦјЬхBЕФЗжзгЪ§ЯрЕШЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
ЁЁA.ЭЌЬхЛ§ЕФЦјЬхAКЭЦјЬхBЕФжЪСПБШЮЊm:n
ЁЁB.25ЁцЪБЃЌ1kgЦјЬхAКЭ1kgЦјЬхBЕФЗжзгЪ§БШЮЊm:n
ЁЁC.ЭЌЮТЭЌбЙЪБЦјЬхAКЭЦјЬхBЕФУмЖШБШЮЊn:m
ЁЁD.БъПіЪБЃЌЕШжЪСПЕФAКЭBЦјЬхЕФЬхЛ§БШЮЊn:m
НтЬтЫМТЗ:ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
взДэЕу:ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
[ПМЬтдйЯж]
2.VЁЂnЁЂNжЎМфЕФМЦЫуЙиЯЕ
(1)МЦЫуЙиЯЕЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(2)ЪЙгУЗЖЮЇЃК
ЂйЪЪгУгкЫљгаЕФЦјЬхЃЌЮоТлЪЧДПОЛЦјЬхЛЙЪЧЛьКЯЦјЬхЁЃ
ЂкЕБЦјЬхФІЖћЬхЛ§гУ22.4LЁЄmol-1ЪББиаыЪЧБъзМзДПіЁЃ
1. mЁЂnЁЂNжЎМфЕФМЦЫуЙиЯЕЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(1)МЦЫуЙиЯЕЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)ЪЙгУЗЖЮЇЃКжЛвЊЮяжЪЕФзщГЩВЛБфЃЌЮоТлЪЧКЮзДЬЌЖМПЩвдЪЙгУЁЃ
5.ЦјЬхФІЖћЬхЛ§
(1)ИХФюЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(2)ЗћКХЃКЁЁЁЁЁЁЁЁЁЁ (3)ЕЅЮЛЃКЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЃ
(4)БъзМзДПіЯТЕФЦјЬхФІЖћЬхЛ§
ЂйБъзМзДПіЪЧжИЃК ЮТЖШЁЁЁЁЁЁ ЁцЃЌбЙЧПЁЁЁЁЁЁЁЁ ЁЁPaЁЃ
ЂкБъзМзДПіЯТЕФЦјЬхФІЖћЬхЛ§ЪЧЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(5)гАЯьЮяжЪЬхЛ§ДѓаЁЕФвђЫиЃК
Ђй ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
Ђк ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
Ђл ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
4.ФІЖћжЪСП
(1)ИХФюЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(2)ЗћКХЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ(3)ЕЅЮЛЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(4)зЂвтЕуЃКгыЯрЖдЗжзгжЪСПЁЂЪНСПКЭ1molЮяжЪЕФжЪСПЕФвьЭЌЃККЌвхЩЯЁЁ ЁЁЭЌЃЌЪ§жЕЩЯЁЁ ЁЁЭЌЁЃ
3.АЂЗќМгЕТТоГЃЪ§
(1)КЌвхЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(2)ЗћКХЃКЁЁЁЁЁЁ (3)ЕЅЮЛЃК ЁЁЁЁЁЁЁЁЁЁЁЃ
(4)зЂвтЕуЃК
ЂйАЂЗќМгЕТТоГЃЪ§ЕФЛљзМЪЧ12gЁЁЁЁЁЁЁЁ жаЕФдзгИіЪ§ЁЃ
ЂкЯжНзЖЮГЃШЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЮЊАЂЗќМгЕТТоГЃЪ§ЕФНќЫЦжЕЁЃ
2.ФІЖћ
(1)ИХФюЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(2)ЗћКХЃКЁЁЁЁ
(3)ЛљзМ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(4)зЂвтЕуЃК
ЂйЕБУшЪіЮяжЪЕФЮяжЪЕФСП(ЪЙгУФІЖћ)ЪБЃЌБиаыжИУїЮяжЪЮЂСЃЕФЁЁЁЁЁЁ ЁЁЁЃ
ЂкГЃМћЕФЮЂЙлСЃзггаЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЛђЫќУЧЬиЖЈЕФзщКЯЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com