
题目列表(包括答案和解析)


 混凝 沉降过滤 活性碳吸附池除味 杀菌消毒
混凝 沉降过滤 活性碳吸附池除味 杀菌消毒
明矾---目的:净水 原理:Al3++3H2O Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
Al(OH)3(胶体)有吸附性吸附水中杂质 沉降
活性碳目的:去除异味。原理:吸附性
液氯目的:杀菌消毒Cl2+H2O HCl+HClO(强氧化性)
HCl+HClO(强氧化性)
(二)、大气主要污染物及其危害
1、温室效应
(1)原因:①全球化石燃料用量猛增排放出大量的CO2;②乱砍乱伐导致森林面积急剧减少,吸收CO2能力下降。
2、主要危害:(1)冰川熔化,使海平面上升(2)地球上的病虫害增加(3)气候反常,海洋风暴增多(4)土地干旱,沙漠化面积增大。
3、控制温室效应的措施
(1)逐步调整能源结构,开发利用太阳能、风能、核能、地热能、潮汐能等,减少化石燃料的燃烧;(2)进一步植树造林、护林、转化空气中的CO2
2、酸雨
(1)原因:酸性氧化物(SO2、NO2)SO2+H2O H2SO3 2H2SO3+O2==2H2SO4
H2SO3 2H2SO3+O2==2H2SO4
(2)防止方法:①开发新能源(太阳能、风能、核能等)②减少化石燃料中S的含量
钙基脱硫 CaCO3==CaO+CO2 CaO+SO2==CaSO3 2CaSO3+O2==2CaSO4
③吸收空气中的SO2 ④加强环保教育
3、机动车尾气污染:尾气净化装置 2NO+2CO  N2+2CO2
N2+2CO2
4、CO 能和人体的血红蛋白结合 使能中毒
5、可吸入颗粒物:静电出尘
6、居室空气污染物:甲醛、苯及其苯的同系物、氡等
危害:甲醛对人体健康的影响(肝功能异常等)
7、白色污染的危害:①破坏土壤结构②降低土壤肥效③污染地下水④危及海洋生物的生存
第二单元 水资源的合理利用
(一)、空气质量评价包括:二氧化硫(SO2)、二氧化氮(NO2)、可吸入颗粒物
空气污染指数:根据空气中二氧化硫(SO2)、二氧化氮(NO2)、可吸入颗粒物等污染物的浓度计算出来的数值。首要污染指数即位该地区的空气污染指数
2、如果用溴水检验乙烯,此时还有必要将气体先通入水中吗?
不需要,因为乙醇不干扰乙烯的检验。
[疑难解析]
 说明:
说明:
 说明:
说明:
(1)氟氯代烷是含有氟和氯的烷烃衍生物(商品名为氟得昂),它们性质稳定、无毒,具有不燃烧,易挥发、易液化等特点。
(2)氯、溴的氟代烷可对臭氧层产生破坏作用,形成臭氧空洞。
例1. 下列化合物在一定的条件下,既能发生消去反应又能发生水解反应的是:
A、①② B、②③④ C、② D、①②③④
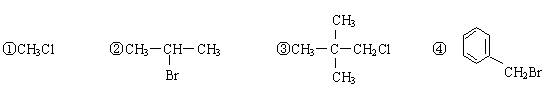
解析:卤代烃在发生消去反应时,有两种共价键断裂(C-X、C-H),并且断裂发生在碳卤键中相邻的两个碳原子上,由此可知,卤代烃发生消去反应对分子结构的要求:必须是与卤原子相连碳原子的相邻碳原子上连有氢原子的卤代烃才能发生消去反应,而不是所有的卤代烃都能发生消去反应。本题①③④卤代烃的相邻碳原子上没有连接氢原子,不能发生消去反应。而卤代烃的水解反应只断裂一种化学键,对分子结构没有什么特别要求。只要是卤代烃都可以发生水解反应,是所有卤代烃的通性。
答案:C
例2. 卤代烃在氢氧化钠的水溶液中水解,这是一个典型的取代反应,其实质是带负电荷的原子团取代了卤代烃中的卤原子。试写出下列反应的化学方程式。
(1)CH3CH2Br跟NaHS的反应 。
(2)CH3CH2I跟CH3COONa的反应 。
(3)CH3CH2I跟NaCN的反应 。
解析:由卤代烃在碱性条件下的水解反应的实质可知:⑴HS-取代溴生成CH3CH2SH;⑵CH3COO-取代I生成CH3CH2OOCCH3;⑶CN-取代I生成CH3CH2CN。
答案:(1)CH3CH2Br+NaHS→CH3CH2SH+NaBr
(2)CH3CH2I+CH3COONa→CH3CH2OOCCH3+NaI
(3)CH3CH2I+NaCN→CH3CH2CN+NaI
例3. 请以溴乙烷为原料合成1,2-二溴乙烷,写出设计方案及涉及到的化学方程式。
解析:简单有机物的合成,可用例推法求解。现要合成1,2-二溴乙烷,先要制得乙烯,而乙烯可由题中所给的溴乙烷在醇溶液中消去得到
答案:设计方案:由卤代烃发生消去反应制得烯,再通过烯的加成获得二卤代物:
CH3CH2Br+NaOH→CH2=CH2+H2O+NaBr
CH2=CH2+Br2→CH2Br-CH2Br
例4. 某液态卤代烷RX(R是烷基,X是某种卤素原子)的密度是a g/cm3。该RX可以与稀碱溶液发生水解反应生成ROH(能与水互溶)和HX。为了测定RX的相对分子量,拟定的实验步骤如下:
①准确量取该卤代烷b mL,放入锥形瓶中。
②在锥形瓶中加入过量稀氢氧化钠溶液,塞上带有长玻璃管的塞子,加热,发生反应。
③反应完成后,冷却溶液,加稀硝酸酸化,滴加过量硝酸银溶液得到白色沉淀。
④过滤、洗涤、干燥后称量,得到固体c 克。
回答下列问题:
(1)装置中长玻璃管的作用是: ;
(2)步骤④中,洗涤的目的是为了除去沉淀上吸附的 离子;
(3)该卤代烷中所含卤素的名称是 ,判断的依据是 ;
(4)该卤代烷的相对分子质量是 (列出算式);
(5)如果在步骤②中,加硝酸的量不足,没有将溶液酸化,则步骤④中测得的c值(填下列选项代码) 。
A、偏大 B、偏小 C、不变 D、大小不定
解析:本题的实验原理是:卤代烃在碱性条件下的水解和卤离子的检验。
(1)因RX(属有机物卤代烃)熔沸点低,加热时易挥发,所以装置中长玻璃导管的作用是防止卤代烃挥发或冷凝回流
(2)醇ROH虽然能与水互溶,但不能电离,所以沉淀AgX吸附的离子只能是Na+、NO3-和过量的Ag+
(3)因为所得AgX是白色沉淀,所以该卤化烃中所含卤素的名称是氯
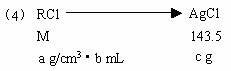
M=143.5ab/c
(5)若加硝酸的量不足,未将溶液酸化,则沉淀中还有AgOH转化为Ag2O沉淀,故测得的c值将增大。
答案:(1)防止卤代烃挥发或冷凝回流;
(2)Na+、NO3-和过量的Ag+
(3)名称是氯,依据是AgX是白色沉淀
(4)M=143.5ab/c
(5)偏大
[典型例题]
例1. 检验溴乙烷中是否有溴元素,主要的实验方法是( )
A. 加入氯水后振荡,看水层里是否有棕红色的溴出现
B. 加入硝酸银溶液,再加稀硝酸,观察有无浅黄色沉淀生成
C. 加入NaOH溶液共热,冷却后加硝酸银溶液,观察有无浅黄色沉淀生成
D. 加入NaOH溶液共热,冷却后用过量稀硝酸中和过量碱后,再加硝酸银溶液,观察有无浅黄色沉淀生成
 例2. 已知有机物A与NaOH的醇溶液混合加热得产物C和溶液D。C与乙烯混合在催化剂作用下可反应生成
例2. 已知有机物A与NaOH的醇溶液混合加热得产物C和溶液D。C与乙烯混合在催化剂作用下可反应生成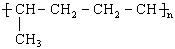 的高聚物。而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式为( )
的高聚物。而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式为( )
A. 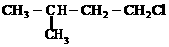 B.
B.
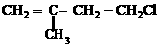
C. 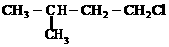 D.
D.
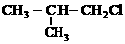
 例3. 由2-氯丙烷制取少量的1,2-丙二醇时,需要经过下列哪几步反应( )
例3. 由2-氯丙烷制取少量的1,2-丙二醇时,需要经过下列哪几步反应( )
A. 加成→消去→取代 B. 消去→加成→水解
C. 取代→消去→加成 D. 消去→加成→消去
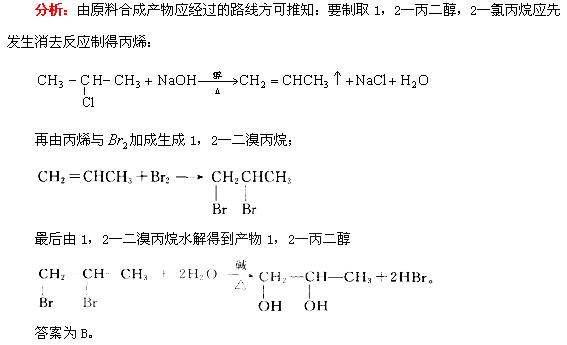 例4. 在实验室鉴定氯酸钾晶体和1-氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取滤渣;⑦用HNO3酸化。(1)鉴定氯酸钾中氯元素的操作步骤是_________(填序号)。(2)鉴定1-氯丙烷中氯元素的操作步骤是_________(填序号)。
例4. 在实验室鉴定氯酸钾晶体和1-氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取滤渣;⑦用HNO3酸化。(1)鉴定氯酸钾中氯元素的操作步骤是_________(填序号)。(2)鉴定1-氯丙烷中氯元素的操作步骤是_________(填序号)。
分析:鉴定样品中是否含有氯元素,应将样品中氯元素转化为Cl-,再转化为AgCl,通过沉淀的颜色和不溶于稀HNO3来判断氯元素。鉴定1-氯丙烷中氯元素实验的关键是在加入AgNO3溶液之前,应加入HNO3酸化,以用于中和NaOH溶液,防止NaOH与AgNO3溶液反应生成沉淀对实验产生干扰。
答案:(1)④、③、⑤、⑦、①。(2)②、③、⑦、①。
例5. 在有机反应中,反应物相同而条件不同,可得到不同的主要产物。下式中R代表烃基,副产物均已略去。
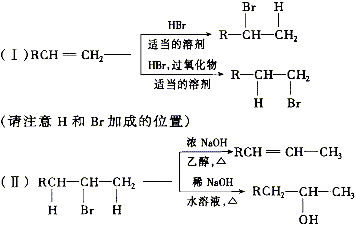
请写出实现下列转变的各步反应的化学方程式,特别注意要写明反应条件。
(1)由CH3CH2CH2CH2Br分两步转变为CH3CH2CHBrCH3
(2)由(CH3)2CHCH═CH2分两步转变为(CH3)2CHCH2CH2OH
 例6. 卤代烃在NaOH的存在下水解,这是典型的取代反应,其实质是带负电的原子团(例如
例6. 卤代烃在NaOH的存在下水解,这是典型的取代反应,其实质是带负电的原子团(例如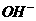 等阴离子)取代了卤代烃分子中的卤原子。例如:
等阴离子)取代了卤代烃分子中的卤原子。例如:
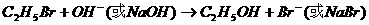
写出下列反应的方程式:
(1)溴乙烷跟NaHS反应
(2)碘甲烷跟 反应
反应
 例7. 某液态卤代烷RX(R是烷基,X是某种卤素原子)的密度是
例7. 某液态卤代烷RX(R是烷基,X是某种卤素原子)的密度是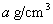 。该RX可以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测定RX的相对分子质量,拟定的实验步骤如下:①准确量取该卤代烷6mL,放入锥形瓶中。②在锥形瓶中加入过量稀
。该RX可以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测定RX的相对分子质量,拟定的实验步骤如下:①准确量取该卤代烷6mL,放入锥形瓶中。②在锥形瓶中加入过量稀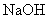 溶液,塞上带有长玻璃管的塞子,加热,发生反应。③反应完成后,冷却溶液,加稀
溶液,塞上带有长玻璃管的塞子,加热,发生反应。③反应完成后,冷却溶液,加稀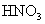 酸化,滴加过量
酸化,滴加过量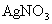 溶液,得白色沉淀。④过滤,洗涤,干燥后称重,得到cg固体。回答下面问题:
溶液,得白色沉淀。④过滤,洗涤,干燥后称重,得到cg固体。回答下面问题:
(1)装置中长玻璃管的作用是___________。
(2)步骤④中,洗涤的目的是为了除去沉淀上吸附的___________离子。
(3)该卤代烷中所含卤素的名称是___________,判断的依据是___________。
(4)该卤代烷的相对分子质量是___________(列出算式)。
(5)如果在步骤③中加 的量不足,没有将溶液酸化,则步骤④中测得的c值(填下列选项代码)___________。
的量不足,没有将溶液酸化,则步骤④中测得的c值(填下列选项代码)___________。
A. 偏大 B. 偏小 C. 不变 D. 大小不定
分析:本题是定性和定量实验的综合,考察的是卤代烃的卤原子的鉴别实验。在步骤③中,若加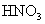 的量不足,则
的量不足,则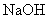 会与
会与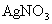 反应生成
反应生成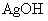 (最终转化为
(最终转化为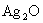 )沉淀,这样生成的
)沉淀,这样生成的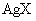 沉淀中因混有
沉淀中因混有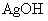 而使其质量偏大。
而使其质量偏大。
答案:(1)防止卤代烷挥发(或冷凝)。(2)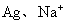 和
和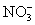 。(3)氯;得到的卤化银沉淀是白色的。(4)
。(3)氯;得到的卤化银沉淀是白色的。(4)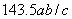 。(5)A。
。(5)A。
1、为什么要在气体通入KMnO4酸性溶液前加一个盛有水的试管?起什么作用?
因为挥发出的乙醇也能使酸性高锰酸钾溶液褪色,干扰乙烯的检验。目的是除去挥发出的乙醇。
2、用何种波谱的方法检验反应物中有乙醇生成?
CH3CH2Br的分子中只有两类氢原子,而水解反应生成的乙醇有三种氢原子,核磁共振氢谱不同,所以用核磁共振氢谱的方法检验反应物中有乙醇生成。
实验2:组装如上图所示装置,向大试管中注入5mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,加热。如发现有气体放出,尝试采用排水法收集气体。
思考:有人设计了用高锰酸钾酸性溶液是否褪色来检验生成的气体是否是乙烯,装置如图所示。请思考下面问题:
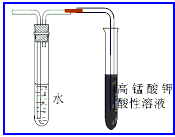
1、如何确定Br来自水解后的Br-,而不是CH3CH2Br中的Br?
首先向大试管中注入5mL溴乙烷,再向试管中加入AgNO3溶液,没有黄色沉淀生成,说明溴乙烷分子中的溴原子与AgNO3溶液不会反应生成AgBr。
另取一大试管,向大试管中注入5mL溴乙烷,再向试管中加入饱和氢氧化钠溶液加热,反应后向溶液中滴加硝酸酸化后,再滴加AgNO3溶液,有浅黄色沉淀产生,说明Br来自水解后的Br-,而不是CH3CH2Br中的Br。
3. 溴乙烷的化学性质:
由于官能团(-Br)的作用,溴乙烷的化学性质比乙烷活泼,能发生许多化学反应。
1)溴乙烷的取代反应-水解反应:
思考:溴乙烷在水中能否电离出Br-?它是否为电解质?加硝酸银溶液是否有沉淀?
溴乙烷在水溶液中或熔化状态下均不电离,是非电解质。溴乙烷分子中的溴原子与AgNO3溶液不会反应生成AgBr。
实验:
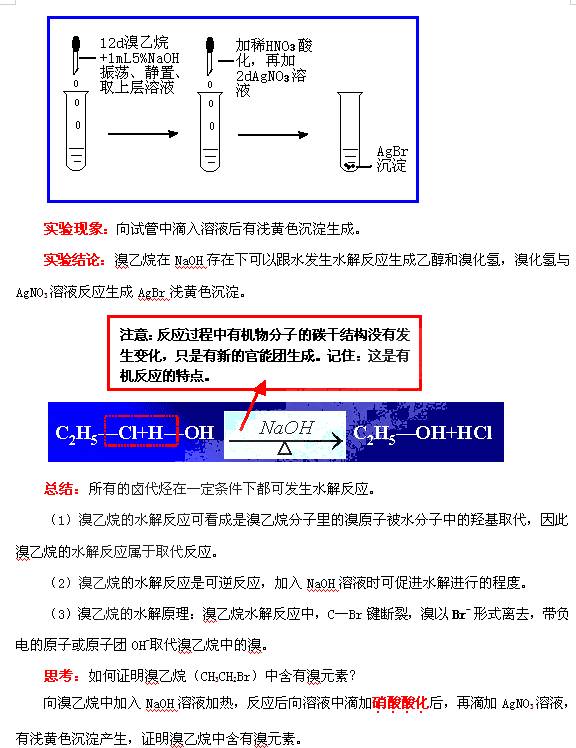 注意:检验卤代烃中卤素的实验步骤:a、取少量样品b、加NaOH溶液c、加热 d、冷却e、取上层清液向其中加入稀HNO3溶液f、加AgNO3溶液。
注意:检验卤代烃中卤素的实验步骤:a、取少量样品b、加NaOH溶液c、加热 d、冷却e、取上层清液向其中加入稀HNO3溶液f、加AgNO3溶液。
(1)加热煮沸是为了加快水解反应的速率,因为不同的卤代烃水解难易程度不同。
(2)加入稀硝酸酸化,一是为了中和过量的NaOH,防止NaOH与AgNO3反应对实验产生影响;二是检验生成的沉淀是否溶于稀硝酸。
 探究试验:
探究试验:
如何设计实验验证溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物?
(1)实验装置
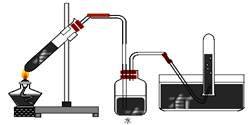
(2)实验设计
实验1:组装如上图所示装置,向大试管中注入5mL溴乙烷和15mL饱和氢氧化钠水溶液,加热。如发现有气体放出,尝试采用排水法收集气体。
思考:
2.
 溴乙烷的物理性质:
溴乙烷的物理性质:
纯净的溴乙烷是无色液体,沸点,不溶于水,可溶于大多数有机溶剂。其密度大于水的密度。溴乙烷的式量大于乙烷,其熔、沸点、密度大于乙烷。
3. 理解消去反应的特点,并能熟练判断有机物消去反应的条件。
考点一、卤代烃
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com