
题目列表(包括答案和解析)
98.填表:
|
实验操作 |
实验现象 |
离子反应方程式 |
|
一小块钠投入FeCl3 溶液中 |
|
|
|
碳酸钠与醋酸溶液 混合 |
|
|
|
盐酸加入KHCO3 溶液中 |
|
|
|
澄清石灰水加入 NaHCO3溶液中 |
|
|
97.一定质量的Na2CO3和NaHCO3混合物共热,反应前Na2CO3在混合物中的质量分数为55.7%,当Na2CO3的含量提高到70%时,NaHCO3约分解了( )
A.20% B.36% C.42% D.50%
96、某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理不正确的是 ( )
|
|
50
mL盐酸 |
50
mL盐酸 |
50
mL盐酸 |
|
m(混合物) |
9.2g |
15.7g |
27.6g |
|
V(CO2)(标况) |
2.24L |
3.36L |
3.36L |
A.盐酸的物质的量浓度为3.0mol/L
B.根据表中数据不能计算混合物中NaHCO3的质量分数
C.加入混合物9.2g时盐酸过量
D.15.7g混合物恰好与盐酸完全反应
95、下列反应的离子方程式书写正确的是 ( )
A.铁屑溶于足量稀硝酸:Fe+4H++NO3-=Fe3++NO↑+2H2O
B.碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O
C.金属钠溶于足量水中:2Na+2H2O=2Na++H2↑+2OH-
D.苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
(4)请简述制备和收集氢气的操作 。
(5)分析上述三个实验,套管实验中“外管”所起的作用通常有 。
94、在体积均为1L,pH均等于2的盐酸和醋酸溶液,分别投入0.23g Na,则下图中比较符合反应事实的曲线是( )
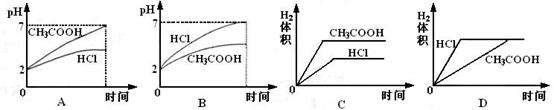
(3)反应开始后 ,能观察到的现象是 。
(1)将胶头滴管中的水滴入小试管 ,然后,在导管口A处放带火星的木条,观察图甲现象,你可得到的两个结论是 、
。
(2)写出甲中反应的化学方程式 。
120.我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:
NH3+CO2+H2O NH4HCO3 ; NH4HCO3+NaCl NaHCO3↓+NH4Cl
;
2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填字母标号);
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。

试回答下列有关问题:
(Ⅰ)乙装置中的试剂是 ;
(Ⅱ)丁装置中稀硫酸的作用是 ;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称)。
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从a管通入 气体,再从b管中通入 气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是 ;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法: 。
119.向某NaOH溶液中通人CO2气体后得溶液M,因CO2通人量的不同,溶液M的组成也不同。若向M中逐滴加人盐酸,产生的气体体积V(CO2)与加人盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA<AB,OA=AB,OA>AB,则下列分析与判断不正确的是(不计CO2的溶解)( )

A.M中只有一种溶质的有(1)和(3) B.M中有两种溶质的有(2)和(4)
C.2)图显示M中c(NaHCO3)>c(Na2CO3) D.(4)图显示M中c(NaHCO3)>c(Na2CO3)
118.已知:在氢氧化钠浓溶液中加入氧化钙,加热,制成的白色固体就是碱石灰。有两个实验小组的同学决定通过实验探究碱石灰的组成。
(1)第一小组设计方案的流程如下:
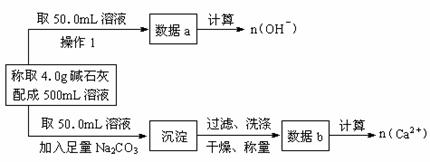
① 写出n (OH-)、n (Ca2+)与n (Na+)的关系:n(Na+)= 。
② 设n (Na+)=x mol、n (Ca2+)=y mol,请填写下表:
|
碱石灰的 可能组成 |
NaOH、CaO |
NaOH、CaO、 Ca (OH)2 |
NaOH、 Ca (OH)2 |
NaOH、 Ca (OH)2、H2O |
|
n (Na+)、n (Ca2+) 的关系 |
40x+56y = 4 |
|
|
|
(2)第二小组同学查得如下资料:Ca(OH)2在250℃时不分解、NaOH在580℃时不分解。
他们设计了如下方案并得出相关数据:取市售碱石灰4.0g,在250℃时加热至恒重,测得固体质量减少了0.42g,剩余固体在580℃时继续加热至恒重,固体质量又减少了0.75g。请通过计算确定该碱石灰各成分的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com