
题目列表(包括答案和解析)
9.如果Fe3+、SO、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是( )
A.Na+ B.I-
C.CO D.Cl-
解析:选D。从溶液中离子共存的角度可知:Fe3+与I-、CO不能共存,Al3+与CO不能共存,可排除B、C项;再从电荷守恒可知应选D项。
8.设NA为阿伏加德罗常数。下列说法中,不正确的是( )
A.46 g NO2与46 g N2O4中所含原子总数相等,为3NA
B.1 mol Na2O2与足量水充分反应,转移电子总数为2NA
C.32 g CH4中含有C-H键总数为8NA
D.标准状况下,11.2 L NH3溶于1 L水,溶液中含有N原子的微粒总数为0.5NA
解析:选B。A中NO2与N2O4具有相同的最简式,所以等质量的两种物质有相同的原子组成,A正确;B中1 mol过氧化钠反应转移1 mol电子;C中1 mol甲烷含有4 mol C-H键,32 g甲烷含有8NA个C-H键;D中11.2 L氨气即0.5 mol,根据氮原子守恒,D正确。
7.配制0.1 mol·L-1的NaCl溶液,下列操作会导致所配溶液的物质的量浓度偏高的是( )
A.称量时,左盘高,右盘低 B.定容时俯视读取刻度
C.原容量瓶洗净后未干燥 D.定容时液面超过了刻度线
解析:选B。A项称量时左盘高说明溶质质量少,偏低;B项俯视时加入的水少,结果偏高;C项无影响;D项加水过多,结果偏低。
6.一定温度下,将少量生石灰放入一定量的饱和石灰水中,搅拌并冷却到原温度,下列说法正确的是( )
A.溶质的质量增大 B.溶质的物质的量浓度增大
C.Ca(OH)2溶解度不变 D.溶质的质量分数增大
解析:选C。A项,加入生石灰后会参与反应,使水的质量减少,溶质析出,故溶质质量减小;B项,因为溶液始终为饱和溶液,故溶质的物质的量浓度不变;D项,质量分数不变;C项,温度不变,溶解度不变。
5.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.1 mol DO+中含有的中子数为10NA
B.1 mol SiC晶体中含有的Si-C键数目为2NA
C.44 g乙醛与乙酸乙酯的混合物中含有的氢原子数为4NA
D.22.4 L Cl2中含有的分子数为NA
解析:选C。D中含有1个中子,18O中含有10个中子,所以1 mol DO+中含有13NA个中子。1 mol SiC晶体中含有4NA个Si-C键。D项中没有指明是标准状况,无法判断22.4 L氯气的物质的量。
4.设NA为阿伏加德罗常数,下列对于0.3 mol/L硫酸钾溶液的说法不正确的是( )
A.1 L溶液中含有0.6NA个钾离子
B.1 L溶液中含有钾离子和硫酸根离子总数为0.9NA
C.2 L溶液中钾离子浓度为1.2 mol/L
D.2 L溶液中含有硫酸根离子0.6NA个
解析:选C。C项溶液是均一、稳定的,浓度与体积无关,K+的浓度为0.6 mol/L。
3.(2009年滨州模拟)14C是碳的一种同位素,NA为阿伏加德罗常数,下列说法中正确的是( )
① mol 14CH4分子中所含中子数为NA ②7 g 14C原子形成的石墨中所含质子数为3NA ③17 g甲基(- 14CH3)所含电子数为8NA ④11.2 L乙烯所含原子个数为3NA
A.①② B.①②④
C.②③ D.③④
解析:选A。本题考查原子、分子结构、阿伏加德罗常数等知识。①中 mol 14CH4分子中所含中子的物质的量为1 mol 故①正确;②中7 g 14C原子含质子7÷14×6 mol 即3 mol ,故②正确;③中17 g甲基(- 14CH3)含电子的物质的量为9 mol,故③错;④应指明为标准状况下。
2.下列实验操作或记录正确的是( )
A.常温常压下测得1 mol N2的质量为28 g
B.用量筒测得排水法收集制得的氢气体积为50.28 mL
C.用两只250 mL的容量瓶配制0.1 mol/L 500 mL的NaOH溶液
D.用托盘天平称得2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g
解析:选A。B项,量筒的精确度为0.1 mL;C项,直接使用500 mL的容量瓶配制;D项托盘天平的精确度为0.1 g。
1.下列有关物理量相应的单位表达错误的是( )
A.摩尔质量g/mol B.气体摩尔体积L/mol
C.溶解度g/100 g D.密度g/cm3
解析:选C。溶解度的单位是g。
21.(8分)已知:A、B、F是家庭中常见的有机物,E是石油化工发展水平的标志。根据下面转化关系回答问题。
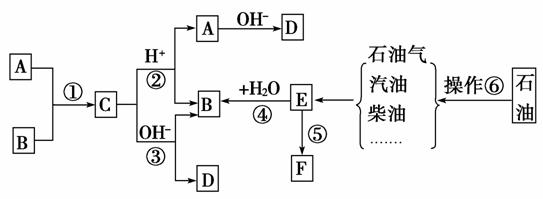
(1)操作⑥的名称为 。
(2)取代反应的范畴很广,①-⑤中属于取代反应的是________(填序号)。
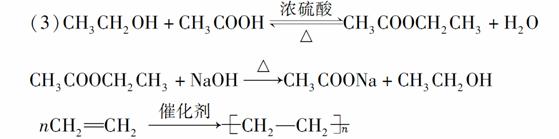
(3)请写出下列反应的化学方程式:
①_____________________________________________________;
③_____________________________________________________;
⑤_____________________________________________________。
(4)F是一种常见的高分子材料,它给我们带来了巨大的方便。然而,这种材料造成的当今的环境问题是________________________。
解析:根据“E是石油化工发展水平的标志”可知E为乙烯。一方面,乙烯可以转化成F,另一方面,乙烯与水反应生成B。结合“B、F是家庭中常见的有机物”的信息,推断B是乙醇,F是聚乙烯。观察框图,C在酸性或碱性条件下都可以得到乙醇,说明C是某种酸与乙醇反应生成的酯。既然这种酸是常见的物质,则A是醋酸。其他答案可依次推出。
答案:(1)分馏 (2)①②③
( 4 )白色污染
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com