
题目列表(包括答案和解析)
3.(2010×山师附中1月考题)A、B、C、D为四种短周期主族元素,且原子序数依次增大。已知
A的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子
数是D原子最外层电子数的2倍,C原子最外层只有一个电子。下列说法中正确的是( )
A.原子半径:C<A B.离子半径:D>B
C.非金属性:A>B D.最高价氧化物对应水化物的碱性:C>D
解析:该题以元素的推断为载体,考查学生对元素周期表的熟悉程度及对表中各元素性质
和相应原子结构的周期性递变规律的认识和掌握程度。由题意可知A、B、C、D分别是C、
O、Na、Al。
答案:D
2.(2010×南京师大附中1月考题)A、B、C、D是原子序数依次递增的短周期元素。A原子核内
没有中子,C原子的次外层电子数与最外层电子数之比为1∶3,B和C形成的气态化合物
种类较多,C和D形成的化合物X是水晶的主要成分,A、B、C三种元素可形成离子化合
物Y,该离子化合物中各元素原子的物质的量之比为4∶2∶3。下列说法正确的是( )
A.X既能与酸反应,也能与碱反应,属于两性氧化物
B.Y为盐,其水溶液呈中性
C.A2C和BA3分子中电子数相同
D.由B、C元素组成且元素质量比为7∶8的化合物能溶解于水
解析:根据题意可推出A、C分别为H、O;与O可形成多种气态化合物,且原子序数在1-
8之间的元素B只能是N;水晶的主要成分是SiO2,故D为Si。SiO2为酸性氧化物,A错;
Y为NH4NO3,NH4+水解,溶液呈酸性,B错;A2C、BA3即H2O、NH3,分子中均含有10
个电子,C正确;由B、C元素组成且元素质量比为7∶8的化合物是NO,不溶于水,D错。
答案:C
1.(2010×北京-黄冈预测卷八)在周期表主族元素中,X元素位于第二周期,且分别与元素
Y、Z、W相邻,X、Y的原子序数之和等于Z的原子序数;这四种元素原子的最外层电子
数之和为20。下列判断正确的是( )
A.原子序数:Z>Y>X>W
B.X、Y、Z、W形成的单质最多有6种
C.X元素最高价氧化物对应水化物的化学式为H3XO4
D.四种元素的气态氢化物中,W的气态氢化物最稳定
解析:设X元素原子的最外层电子数为a,则与之相邻的同周期的两元素原子最外层电子数
分别是a-1、a+1,依据元素周期表的结构,另外一种与X相邻的元素在X的下一周期,且
X同主族,则最外层电子数为a,所以有a-1+a+1+a+a=20,a=5,即X是氮元素,与之相邻
的元素为碳元素、氧元素、磷元素,再根据X、Y的原子序数之和等于Z的原子序数,可知
Y是氧元素,Z是磷元素,进而推知W是碳元素。A选项正确;碳元素形成的单质有金刚
石、石墨、C60,氧元素形成的单质有氧气和臭氧,磷元素可以形成白磷与红磷,再加上氮
气已超过6种单质,B选项错误;氮元素最高价氧化物对应水化物的化学式为HNO3,C选
项错误;四种元素中非金属性最强的是氧元素,H2O最稳定,D选项错误。
答案:A
15.现有A、B、C三种烃,其球棍模型如下图:

(1) 等质量的以上物质完全燃烧时耗去O2的量最多的是________(填对应字母,下同);
(2) 同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是________;
(3) 等质量的以上三种物质燃烧时,生成二氧化碳最多的是________,生成水最多的是________。
(4) 在120℃、1.01×105 Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前
后气体体积没有发生变化,这两种气体是________。
解析:据球棍模型可知A为CH4,B为C2H4,C为C2H6。,(1)等质量的烃CxHy完全燃烧时,氢
元素的质量分数越大,耗氧量越大,CH4、C2H4、C2H6中的依次为、、,故CH4耗O2最多;
(2)等物质的量的烃CxHy完全燃烧时,(x+)的值越大,耗氧量越大,CH4、C2H4、C2H6的x+依
次为1+=2、2+=3、2+=3.5,故C2H6耗O2最多;
(3)n(CO2)=n(C)=×1、×2、×2,×2最大,故C2H4生成的CO2最多;
n(H2O)=n(H)=×4、×4、×6,×4最大,故CH4生成的H2O最多。
(4)温度≥100℃条件下,当烃分子中含有4个氢原子时,该烃完全燃烧前后气体体积不变,
y=4的为CH4、C2H4,故答案为CH4、 C2H4。
答案:(1)A (2)C (3)B A (4)A、B
13.某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如右图。
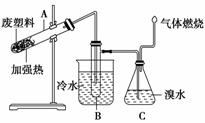
加热聚丙烯废塑料得到的产物如下表:,
|
产物 |
氢气 |
甲烷 |
乙烯 |
丙烯 |
苯 |
甲苯 |
碳 |
|
质量分数(%) |
12 |
24 |
12 |
16 |
20 |
10 |
6 |
(1)试管A中残留物有多种用途,如下列转化就可以制取高聚物聚乙炔。
A中残留物聚乙炔,
写出反应②③的化学方程式_________________ _______________、
________________________________________________________________________。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有________种。
(3)锥形瓶C中观察到的现象是
________________________________________________________________________。
经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为________。
(4)写出C中逸出的气体在工业上的两种用途________、________________。
解析:塑料废弃物形成污染的主要原因是所用的合成树脂之间以碳碳共价键相连,结构稳定,不容易降解成小分子。目前已开发出多种可降解的塑料,其类型主要有:生物自毁塑料、化学自毁塑料、光学自毁塑料、医用自毁塑料等。这里采取的是化学自毁,根据题给的信息可知,它的分解产物之一为碳,留在A中。,因为乙烯、丙烯常温下为气体,所以试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质为甲苯,其一氯代物有4种,
分别为: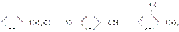
 通入C之前的气体主要成分为氢气、甲烷、乙烯和丙烯,通过C以后,乙烯和丙烯被溴水吸收而使溴水褪色,还有氢气和甲烷没有反应。根据题中所给出的数据,可以算出,二者的物质的量之比为4∶1,所以其平均相对分子质量为:2×4/5+16×1/5=4.8。H2和甲烷在工业上的主要用途为:作为合成氨原料、燃料或有机化工原料。
通入C之前的气体主要成分为氢气、甲烷、乙烯和丙烯,通过C以后,乙烯和丙烯被溴水吸收而使溴水褪色,还有氢气和甲烷没有反应。根据题中所给出的数据,可以算出,二者的物质的量之比为4∶1,所以其平均相对分子质量为:2×4/5+16×1/5=4.8。H2和甲烷在工业上的主要用途为:作为合成氨原料、燃料或有机化工原料。
答案:
(2)4 (3)溴水褪色 4.8 (4)合成氨原料 作燃料或有机化工原料
12.(2007·上海卷)乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题:
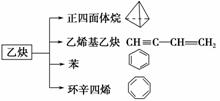 ,
,
(1)正四面体烷的分子式为______________,其二氯取代产物有____ ____种。
(2)关于乙烯基乙炔分子的说法错误的是________(填序号)。
a.能使酸性KMnO4溶液褪色,b.1摩尔乙烯基乙炔能与3摩尔Br2发生加成反应,c.乙烯基乙炔分子
内含有两种官能团,d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
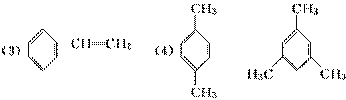
(3)写出与环辛四烯
互为同分异构体且属于芳香烃的分子的结构简式________________________________________________________________________。
(4)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例)__________、__________。
解析:(1)由于正四面体烷的每一个面均是正三角形,因此其一氯代物、二氯代物、三氯代物和四氯代物均只有一种。(2)乙烯基乙炔分子中含有两种官能团,分别是碳碳双键和碳碳三键,均能被酸性KMnO4溶液氧化;1 mol乙烯基乙炔分子和Br2完全反应消耗Br2 3 mol;由于乙炔和乙烯基乙炔的最简式相同,因此等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同。(3)环辛四烯的化学式为C8H8,分子内有5个不饱和度,它的一种同分异构体属于芳香烃,苯基有4个不饱和度,还有一个不饱和度用碳碳双键构建,易得它的一种同分异构体是苯乙烯。(4)本题中最关键要注意到题中只是笼统地描述一氯代物只有两种,因此它包括两部分,一部分是侧链上的取代,另一部分是苯环上的取代,弄清这个问题后其同分异构体不难写出。
答案:(1)C4H4 1 (2)d
 (合理即可)
(合理即可)
11.已知一定质量的某烃完全燃烧后得标准状况下CO2气体6.72 L,生成H2O 7.2 g。根据以上条件能否推出该烃的分子式?________(填“能”或“不能”)。若能,则该烃的分子式为________,并说明理由;若不能也必须说明原因。
解析:
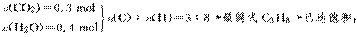
答案:能 C3H8 因依据题干条件可推断出该烃最简式为C3H8,H原子个数为C原子个数的2倍加2,说明3个C原子均为饱和的C原子,最简式即分子式。,
10.有1体积的乙烯和乙炔的混合气体,恰好能跟相同条件下的1.6体积的H2完全反应生成乙烷,则混合气体中,乙烯和乙炔的物质的量之比是( )
A.1∶4 B.3∶7 C.2∶3 D.2∶1
解析:CH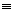 CH+2H2CH3CH3 CH2=CH2+H2CH3CH3
CH+2H2CH3CH3 CH2=CH2+H2CH3CH3
设混合气体中有x体积乙炔,则乙烯为1-x体积,则2x+(1-x)=1.6,x=0.6,
所以V(乙炔)∶V(乙烯)=x∶(1-x)=0.6∶(1-0.6)=3∶2,则乙炔与乙烯物质的量的比为3∶2。
答案:C
9.已知乙烯分子是平面结构,因此1,2?二氯乙烯可以形成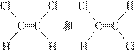 两种不同的空间异构体。下列各物质中,能形成类似上述两种空间异构体的是( )
两种不同的空间异构体。下列各物质中,能形成类似上述两种空间异构体的是( )
A.1-丁烯 B.丙烯 C.2-甲基-2-丁烯 D.2-氯-2-丁烯
解析:由题意可知,只要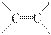 双键的碳原子上都连接两个不同的取代基,就存在空间异构体。显然,只有2?氯?2?丁烯存在空间异构体,选D。
双键的碳原子上都连接两个不同的取代基,就存在空间异构体。显然,只有2?氯?2?丁烯存在空间异构体,选D。
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com