
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
23£Æ‘⁄Ã’¥…𧓵…œ≥£”ˆµΩ“ÚÃ’Õ¡¿ÔªÏ”–—ıªØÃ˙∂¯”∞œÏ≤˙∆∑÷ ¡øµƒŒ °£Ω‚æˆ∑Ω∑®÷Æ“ª «∞—’‚–©Ã’Õ¡∫Õ
ÀÆ“ª∆Ω¡∞Ë£¨ π¡£◊”÷±æ∂‘⁄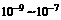 ÷ƺ‰£¨»ª∫Û≤»ΡΩ∏˘µÁº´£¨Ω”Õ®÷±¡˜µÁ‘¥£¨’‚ ±—Ùº´æ€ºØ°°°°°°°°°°°°°°°°°°°°
£¨“ıº´æ€ºØ°°°°°°°°°°°°°°°°°°°°
£¨¿Ì”… «°°°°°°°°°°°°°°°°°°°°°°°°
°°°°°°°°°°°°°°°°°£(√øø’1∑÷)
÷ƺ‰£¨»ª∫Û≤»ΡΩ∏˘µÁº´£¨Ω”Õ®÷±¡˜µÁ‘¥£¨’‚ ±—Ùº´æ€ºØ°°°°°°°°°°°°°°°°°°°°
£¨“ıº´æ€ºØ°°°°°°°°°°°°°°°°°°°°
£¨¿Ì”… «°°°°°°°°°°°°°°°°°°°°°°°°
°°°°°°°°°°°°°°°°°£(√øø’1∑÷)
¥∞∏£∫23£Æ¥¯∏∫µÁ∫…µƒΩ∫á£◊”Ã’Õ¡£ª¥¯’˝µÁ∫…µƒ—ıªØÃ˙Ω∫á£◊”£ª¥¯œý∑¥µÁ∫…µƒΩ∫á£◊”Õ®µÁ ±≤˙…˙µÁ”æœ÷œÛ£¨∑÷±œÚ¡Ωº´“∆∂Ø£¨¥”∂¯¥ÔµΩ≥˝‘”ƒøµƒ
«±ƒÐ≤‚ ‘
22£Æœ÷‘⁄𧓵…œ÷˜“™≤…”√¿Î◊”Ωªªªƒ§∑®µÁΩ‚±•∫Õ ≥—ŒÀÆ÷∆»°H2°¢Cl2°¢NaOH°£
«Îªÿ¥œ¬¡–Œ £∫
°°°° (1)‘⁄µÁΩ‚π˝≥Ã÷–£¨”εÁ‘¥’˝º´œý¡¨µƒµÁº´…œÀ˘∑¢…˙µƒµÁº´∑¥”¶ ΩŒ™°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°£(2∑÷)
°°°° (2)µÁΩ‚÷Æ«∞ ≥—ŒÀÆ–Ë“™æ´÷∆£¨ƒøµƒ «≥˝»•¥÷—Œ÷–µ»‘”÷ ¿Î◊”£¨ π”√µƒ ‘º¡”–£∫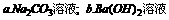 c.œ°HCI£¨∆‰∫œ¿Ìµƒº”»ÎÀ≥–Ú «°°°°°°°°°°°°°°°°°°°°°°
°£(3∑÷)
c.œ°HCI£¨∆‰∫œ¿Ìµƒº”»ÎÀ≥–Ú «°°°°°°°°°°°°°°°°°°°°°°
°£(3∑÷)
°° (3)»Áπ˚‘⁄»ðª˝Œ™10Lµƒ¿Î◊”Ωªªªƒ§µÁΩ‚≤€÷–£¨1min‘⁄“ıº´ø…≤˙…˙Cl211£Æ2L(±Í◊º◊¥øˆ)£¨’‚ ±»Ð“∫µƒpH «°°°°°°°°°°°°°°°°°°°°°° °£(…Ëê˝Œ¨≥÷≤ª±‰)(3∑÷)
°°°° (4)Cl2≥£”√”⁄◊‘¿¥ÀƵƒœ˚∂æ…±æ˙£¨œ÷”–“ª÷÷–¬–Õœ˚∂溡ClO2£¨»ÙÀ¸√«‘⁄…±æ˙π˝≥Ã÷–µƒªπ‘≠≤˙ŒÔæ˘Œ™Cl-£¨œ˚∂æµ»¡øµƒ◊‘¿¥ÀÆÀ˘–ËCl2∫ÕClO2µƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™°°°°°°°°°°°°°°°°°°°° .(3∑÷)
¥∞∏£∫
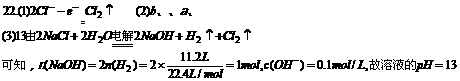
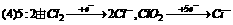 µ±¡Ω’þµ√µÁ◊” ˝œýµ» ±£¨œ˚∂æƒÐ¡¶œýµ±£¨¥À ±¡Ω’þŒÔ÷ µƒ¡ø÷Ʊ»Œ™5£∫2
µ±¡Ω’þµ√µÁ◊” ˝œýµ» ±£¨œ˚∂æƒÐ¡¶œýµ±£¨¥À ±¡Ω’þŒÔ÷ µƒ¡ø÷Ʊ»Œ™5£∫2
21£Æœ¬Õº÷–√ø“ª∑ΩøÚ÷–µƒ◊÷ƒ∏¥˙±Ì“ª÷÷∑¥”¶ŒÔªÚ…˙≥…ŒÔ£∫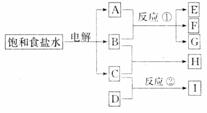
|
œÓƒø |
C |
D |
1 |
|
∆ º◊È≥…/mol |
6 |
4 |
0 |
|
ƒ≥ ±øÃ◊È≥…/mol |
3 |
3 |
2 |
°°°° ŒÔ÷ A∏˙B∑¥”¶…˙≥…E°¢F∫ÕG£ªŒÔ÷ C∏˙D∑¥”¶…˙≥…I£¨ƒ≥Œ¬∂»œ¬∏√∑¥”¶∆ º∫Õƒ≥ ±øõƒ∑¥”¶ªÏ∫œŒÔ◊È≥…»Á…œ±Ì£¨«ÎÃÓ–¥œ¬¡–ø’∞◊£∫
°°°° (1)ŒÔ÷ Hµƒ∑÷◊” Ω «°°°° °°°°°°°°°°°°°°°°°°°°°°°°(1∑÷)
°°°° (2)∑¥”¶¢ŸµƒªØ—ß∑Ω≥Ã Ω «°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°£(2∑÷)
°°°° (3)∑¥”¶¢⁄µƒªØ—ß∑Ω≥à Ω(±ÿ–Î◊¢√˜∑¥”¶Ãıº˛) «°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°£(2∑÷)
¥∞∏£∫
°°°°°°°°°°°° ∏þŒ¬∏þ—π
 °°°°
⇌°°°°°°°°°°
2NH3
°°°°
⇌°°°°°°°°°°
2NH3
°°°°°°°°°° ¥þªØº¡
20.”√¡Ω∏ˆ∂Ë–‘µÁº´≤»Î500mAgNO3»Ð“∫÷–Õ®µÁµÁΩ‚£¨µ±µÁΩ‚“∫µƒpH¥”6£Æ0±‰Œ™3£Æ0 ±(…˵ÁΩ‚ ±“ıº´√ª”–«‚∆¯“ð≥ˆ£¨«“µÁΩ‚“∫‘⁄µÁΩ‚«∞∫Ûê˝±‰ªØø…“‘∫ˆ¬‘)£¨µÁº´…œŒˆ≥ˆ“¯µƒ÷ ¡ø¥Û‘º «°°°°°° (°°°° )
A£Æ27 mg°°°° B£Æ54 mg°°°° C£Æ108 mg°°°° D£Æ216 mg
¥∞∏£∫
 ∂˛°¢ÃÓø’°°
∂˛°¢ÃÓø’°°
19£Æœ¬¡–π˝≥⟵Á¿Î£ª¢⁄µÁΩ‚£ª¢€µÁ∂∆£ª¢ÐµÁ”棪¢ðµÁªØ∏Ø ¥£¨–ËÕ®µÁ∫Û≤≈ø…Ω¯––µƒ «°°°° (°°°° )
A.¢Ÿ¢⁄¢€°° B.¢⁄¢€¢Ð°°°° C£Æ¢€¢Ð¢ð°°°° D£Æ¢Ÿ¢⁄¢€¢Ð¢ð
¥∞∏£∫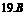
18£ÆC°° ∑÷Œˆ£∫µÁΩ‚æ´¡∂Õ≠£¨”¶”√¥÷Õ≠∞ÂÃÂ◊˜—Ùº´∑¢…˙∑¥”¶£∫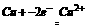 £¨Õ¨ ±¥÷Õ≠÷–À˘∫¨ Na°¢Fe°¢Znµ»‘”÷ “≤ ßµÁ◊”£¨“‘¿Î◊”–Œ Ω»ÐΩ‚”⁄µÁΩ‚“∫÷–
£¨Õ¨ ±¥÷Õ≠÷–À˘∫¨ Na°¢Fe°¢Znµ»‘”÷ “≤ ßµÁ◊”£¨“‘¿Î◊”–Œ Ω»ÐΩ‚”⁄µÁΩ‚“∫÷–
18£Æœ¬¡–πÿ”⁄µÁΩ‚æ´¡∂Õ≠µƒ– ˆ÷–≤ª’˝»∑µƒ «°°°° (°°°° )
°°°° A.¥÷Õ≠∞Âã∫—Ùº´
°°°° B.µÁΩ‚ ±£¨—Ùº´∑¢…˙—ıªØ∑¥”¶£¨∂¯“ıº´∑¢…˙µƒ∑¥”¶Œ™Cu2++2e- Cu
Cu
°°°° C£Æ¥÷Õ≠÷–À˘∫¨Na°¢Fe°¢Znµ»‘”÷ £¨µÁΩ‚∫Û“‘µ•÷ –Œ Ω≥¡ª˝≤€µ◊£¨–Œ≥…—Ùº´ƒý
D£ÆµÁΩ‚Õ≠µƒ¥ø∂»ø…¥Ô99£Æ95%-99£Æ98%
¥∞∏£∫
17£Æ µ—È “”√«¶–ÓµÁ≥ÿ◊˜µÁ‘¥µÁΩ‚±•∫Õ ≥—ŒÀÆ÷∆»°Cl2£¨“—÷™«¶–ÓµÁ≥ÿ∑≈µÁ ±∑¢…˙»Áœ¬∑¥”¶£∫
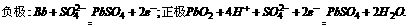
∏∫º´ΩÒ»Ù÷∆µ√Cl20£Æ050mol£¨’‚ ±µÁ≥ÿƒ⁄œ˚∫ƒµƒH2SO4µƒŒÔ÷ µƒ¡ø÷¡…Ÿ «°°°° (°°°° )
A£Æ0£Æ025 mol°°°° B£Æ0£Æ050 mol°°°° C£Æ0£Æ10 mol°°°° D£Æ0£Æ20 mol
¥∞∏£∫17£¨A°°
16£Æ‘⁄Ã˙÷∆∆∑…œ∂∆“ª∂®∫Ò∂»µƒ–ø≤„£¨“‘œ¬∑Ω∞∏…˺∆’˝»∑µƒ «°°°° (°°°° )
°°°° A.–ø◊˜—Ùº´£¨Ã˙◊˜“ıº´£¨»Ð“∫÷–∫¨”––ø¿Î◊”°°°° B.≤¨◊˜“ıº´£¨Ã˙◊˜—Ùº´£¨»Ð“∫÷–∫¨”––ø¿Î◊”
C.Ã˙◊˜—Ùº´£¨Ã˙◊˜“ıº´£¨»Ð“∫÷–∫¨”–—«Ã˙¿Î◊”°°°° D£Æ–ø◊˜“ıº´£¨Ã˙◊˜—Ùº´£¨»Ð“∫÷–∫¨–ø”–¿Î◊”
¥∞∏£∫16£ÆA°° µÁ∂∆ ±£¨”¶”√µÁΩ‚‘≠¿Ì£¨∂∆º˛◊˜“ıº´£¨“™∂∆µƒΩ Ù◊˜—Ùº´£¨µÁ∂∆“∫“ª∞„ «“™∂∆Ω Ùµƒ—Œ»Ð“∫
15£Æ“‘Ã˙Œ™—Ùº´°¢“‘Õ≠Œ™“ıº´£¨∂‘◊„¡øµƒNaOH»Ð“∫Ω¯––µÁΩ‚£¨“ª∂Œ ±º‰∫Ûµ√µΩ2molFe(OH)2≥¡µÌ£¨¥Àº‰π≤œ˚∫ƒÀƵƒŒÔ÷ µƒ¡øŒ™°°°°°° (°°°° )
°° A£Æ2 mol°°°° B£Æ3 mol°°°° C£Æ4 mOl°°°° n 5 mOl
¥∞∏£∫

π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com