
题目列表(包括答案和解析)
4.氯化苄(C6H5CH2C1)由甲苯和氯反应而合成,反应条件是 ( )
A.浓H2SO4存在下 B.加热 C.铁粉催化 D.光照
答案: 4.C 考查学生对知识的迁移能力,溴与苯的反应就需铁作催化剂,氯与苯的反应相同
3.已知HBrO比H2C03酸性弱,HC03比HBrO难电离,则下列反应不能发生的是 ( )
A.2HBrO+Na2C03 --2NaBrO+H2O+C02
--2NaBrO+H2O+C02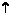 B.HBrO+Na2CO3
B.HBrO+Na2CO3 NaBrO+NaHCO3
NaBrO+NaHCO3
C.C02+H20+NaBrO NaHCO3+HBrO D.C02+H2O+2NaBrO
NaHCO3+HBrO D.C02+H2O+2NaBrO Na2C03+2HBrO
Na2C03+2HBrO
答案: 3.A 已知HBrO比H2CO3的酸性弱,所以不可能用HBrO与Na2CO3反应制出CO2
2.下列实验方案不能达到预期目的的是 ( )
A.用Na、Mg分别与冷水反应的实验来证明Na、Mg的金属性强弱
B.用MgCl2和AICl3分别与过量氨水反应的实验来证明Mg、A1金属性的强弱
C用MgCl2和A1Cl3分别与过量NaOH溶液逐步反应的实验来证明Mg、A1金属性的强弱
D.用Mg、A1分别与盐酸反应的实验来证明Mg、A1的金属性强弱
答案: 2.B MgCl2和AlCl3分别与过量的氨水反应现象相同匀产生白色沉淀,不能说明Mg、A1的金属性
1.制取Fe(OH)2并使之能长时间保存,采取的步骤有:(1)加入一些植物油;(2)溶解FeSO:制成溶液;(3)把蒸馏水加热;(4)加入少许铁粉;(5)加一些CCl4;(6)把氨水滴人FeS04溶液中;(7)滴管伸人FeS04 溶液里再挤出氨水。其中必须用到的操作并按正确顺序排列的是 ( )
A.(3)(2)(5)(6)(4) B.(3)(2)(4)(1)(7)
C.(3)(2)(4)(1)(6) D.(2)(4)(7)(1)(5)
答案:1.B 从题意可知制Fe(OH)2并较久地保存应为:把蒸馏水加热,溶解FeSO4制成溶液后再加少许Fe粉防止氧化;再在上加一层植物油防止空气中的氧气进一步氧化;用较长的滴管吸入氨水伸入液下来制取Fe(OH)2
3.注意化学实验对量的有关要求。
潜能开发
例1用最简便的实验方法,只用酚酞试液就能鉴别出浓度相同的(0.1mol儿)食盐、盐酸和NaOH溶液,简述其实验方法和步骤。
食盐、盐酸和NaOH三种溶液分别为中性、酸性和碱性,而酚酞试液在碱性范围才能显红色,在酸性溶液、中性溶液里均为无色。从表面上看,酚酞无法区别食盐水和盐酸,但仔细地进行深入分析,就会发现食盐水不会与NaOH溶液反应,而盐酸可与NaOH发生反应,使其红色酚酞溶液褪色。这样就可以区分上述三种溶液。
[答案]各取三种未知液少许,分别滴入2滴酚酞试液,溶液显红色的原溶液为NaOH溶液,另取少量余下的两种未知液,分别向其中滴加含有酚酞试液的NaOH溶液,可使溶液褪去颜色的原溶液为盐酸,余下的原溶液(红色不褪)为食盐溶液。
[例2]设计一个以 为原料制取
为原料制取 溶液的方案,并写出实验步骤。
溶液的方案,并写出实验步骤。
思路分析
解答此题可能有几种不同的方案:
其中方案①所用的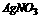 的价格很高,用它来制备Ca(NO3)2 不合算;方案②要消耗电能,且钙与HNO3反应很剧烈,不易控制,还要在反应中产生污染环境的氮的氧化物,惟独方案③既经济,又可行。
的价格很高,用它来制备Ca(NO3)2 不合算;方案②要消耗电能,且钙与HNO3反应很剧烈,不易控制,还要在反应中产生污染环境的氮的氧化物,惟独方案③既经济,又可行。
[答案]实验步骤:(1)在烧杯1中放入一份CaCl2,加适量蒸馏水使其溶解。
(2)在烧杯2中放人1份Na2C03,加适量蒸馏水使其溶解。
(3)将烧杯1和烧杯2中的溶液混合,将沉淀过滤。
(4)把沉淀转移到烧杯里,用蒸馏水洗涤2-3次,至洗涤液不含Cl-。
(5)过滤,得到固体CaC03。
(6)将CaC03放人烧杯中,加适量稀HNO3,使CaC03反应,完全溶解,即得Ca(N03)2溶液。
思维诊断
本题考查设计简单实验和文字表达的能力。设计实验的关键在于认清原理再根据原理设计实验装置,同时要注意使用题目所供实验用品进行设计。本题难点是如何区别盐酸和食盐溶液,虽然二者均不能使酚酞变色,但其溶液的酸碱性有本质的区别,要从盐酸的酸性以及与NaOH作用,可以使NaOH溶液的碱性消失,逐步转化为酸性溶液的特点出发,进行思维,即可解决难点。
思维诊断
本题在制备难溶物CaCO3时,必须在溶液中进行,否则将无法控制反应的量,而使制得的CaCO3不纯,这将增加后面实验的难度。
知能达标训练
2.还要注意化学实验中的特殊操作,中学化学实验对各项基本操作都做了严格的要求和限制,但某些时候却有必要进行反常规操作。
1.严格遵守化学实验中的基本操作。
7.新情境实验题,运用已有知识解决新情境中的新问题,考查学生灵活运用知识的迁移能力、自学能力、观察能力、实验能力和思维能力。
6.对给出的实验方案,做出科学的评估,依据“仪器简单、操作方便、药品易得、节省试剂、现象明显、安全防污”原则选择出最佳方案。
5.根据实验目的、实验进行的条件选取适当药品、仪器(或应用所指定的药品、仪器)完成某次指定的实验操作。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com