
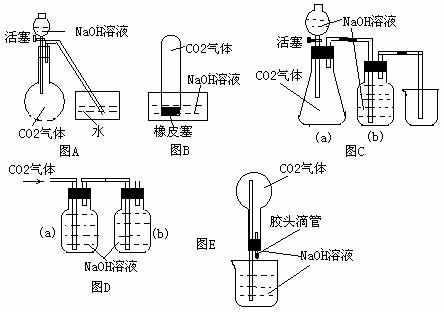
22.(14分)设计一个实验,能通过观察到的明显现象,说明CO2与NaOH溶液发生了反应。实验用品:集气瓶、烧瓶、分液漏斗、导管、橡皮管、弹簧夹、烧杯、量筒、水、CO2气体、NaOH溶液以及你认为所能用到的仪器和药品。现有五位同学设计了如图A-E五个装置,试回答:
(1)对图A,当将分液漏斗中的NaOH溶液滴入烧瓶时,如果看到水槽中的水被吸入到烧瓶中,则证明CO2与NaOH溶液发生了反应。请写出NaOH溶液与过量CO2反应的化学方程式:
(2)若用100mL 1mol/LNaOH溶液吸收0.06 mol CO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比为 。
(3)设NA为阿伏加德罗常数,下列关于0.2mol/L的Na2CO3溶液说法不正确的是
A.2L溶液中阴阳离子总数为0.8NA
B.500mL溶液中CO32-离子浓度为0.2mol/L
C.500mL溶液中Na+离子浓度为0.2mol/L
D.500mL溶液中CO32-物质的量为0.4NA
(4)对图B-E,请指出能达到实验目的的装置 (用B、C、D、E填空),并选出其中两种,说明能证明CO2与NaOH溶液发生了反应的操作及实验现象,将结果填入下表:
|
所选装置 |
操作方法 |
实验现象 |
 |
|
|
21.(13分)将250C 101KPa条件下的氯化氢(HCl)气体49.6L,通入492mL水中,(已知水的密度为:1.00g/mL),得到密度为1.13g/mL的盐酸(即氯化氢的水溶液)。注:250C 101KPa条件下气体摩尔体积为24.8L/mol。(计算结果保留一位小数)
(1)求此盐酸的质量分数?(5分)
(2)求此盐酸的物质的量浓度?(5分)
(3)取出20.0 mL该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?(3分)
第Ⅲ卷(附加题 共14分)
20.(10分)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________________mol。
(2)该气体所含原子总数为________________个。
(3)该气体在标准状况下的体积为_________________L。
(4)该气体在标准状况下的密度为_______________ g/L。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为________________mol/L。
19.(1)(6分)CCl4和蒸馏水都是无色液体,请按下列要求用实验方法鉴别之(简要地写出实验过程)
① 只允许用一种试剂
② 不用任何试剂
(2)(3分)NaCl溶液中含有少量的CaCl2,某学生用过量的Na2CO3使Ca2+离子转化为沉淀而除去,确认Na2CO3已过量的实验方法是
18.(14分)实验室用NaOH固体配制250mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250mL 1.25mol/L的NaOH溶液
|
应称取NaOH的质量/g |
应选用容量瓶的规格/mL |
除容量瓶外还需要的其它仪器 |
|
|
|
|
(2)容量瓶上需标有以下五项中的 ;A
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) ;
A、用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是 ,溶液注入容量瓶前需恢复到室温,这是因为_____________________________;
(5)下列配制的溶液浓度偏低的是 ;
A、称量NaOH时,砝码错放在左盘
B、向容量瓶中转移溶液时(实验步骤②)不慎有液滴洒在容量瓶外面
C、加蒸馏水时不慎超过了刻度线
D、定容时俯视刻度线
E、配制前,容量瓶中有少量蒸馏水
16.(6分)把下面所列实例填入表中相对应的位置
|
分离和提纯方法 |
过程 |
实例 |
|
倾洗 |
用液体分离密度相差较大且不溶的固体 |
|
|
过滤 |
从液体中分离不溶的固体 |
|
|
结晶 |
从溶液中分离已溶解的溶质 |
|
|
蒸馏 |
从溶液中分离溶剂和非挥发性溶质 |
|
|
萃取 |
加入适当溶剂把混合物中某成分溶解及分离 |
|
|
吸附 |
除去混合物中的气态或固态杂质 |
|
A、大米中混有沙子
B、做豆腐时,将豆腐花与豆浆水分离
C、从酒水中制取浓度较大的酒
D、用活性炭除去冰箱内的臭味
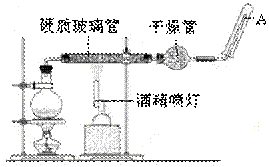 E、不慎洒在衣服上的油汤用酒精除去
E、不慎洒在衣服上的油汤用酒精除去
F、从海水中提取食盐
|
|
(1)该反应的化学方程式为:3 Fe + 4 H2O ==== Fe3O4 + 4 H2↑;请指出该氧化还原反应的还原剂是 。
(2)实验前必须对整套装置进行气密性检查,操作方法是 。
(3)圆底烧瓶中盛装了水,烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 。
(4)酒精灯和酒精喷灯点燃的顺序是 。
(5)干燥管中盛装的物质是 ,作用是 。
(6)试管中收集的气体是 ,如果要在A处玻璃管点燃该气体,则必须对该气体进行 。
15.(8分)如右图所示a、b、c、d分别是几种常见漏斗的上部,A、B、C、D是实际操作中各漏斗的下部插入容器中的示意图,请指出A、B、C、D分别与a、b、c、d相匹配的组合及其组合后装置在实验中的应用,例如:C和a组合,用于制取气体。
(1)A与 组合,用于 ,
(2)B与 组合,用于 ,
(3)B与 组合,用于 ,
(4)D与 组合,用于 。
14.标准状况下,①6.72L NH3 ②1.204×1023个 H2S ③5.6g CH4 ④0.5mol HCl ,下列关系正确的是
A.体积大小:④>③>②>① B.原子数目:③>①>④>②
C.密度大小:④>②>③>① D.质量大小:④>③>②>①
第Ⅱ卷(非选择题 共72分)
13.下列条件下,两瓶气体所含原子数一定相等的是
A.同质量、不同密度的N2和CO
B.同温度、同体积的H2和N2
C.同体积、同密度的C2H4和C3H6
D.同压强、同体积的N2O和CO2
12.已知某溶液的:①体积;②密度;③溶质和溶剂的质量比;④溶质的摩尔质量,要根据溶质的溶解度计算其饱和溶液的物质的量浓度时,上述条件中必不可少的是
A.①②③④ B.①②③
C.②④ D.①④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com