
读地球公转到某位置时的示意图,图中虚线箭头代表地球公转轨道和方向,弧线MPN表示晨昏线,虚线圈表示回归线和极圈,最外圈表示赤道。回答1-3题。
1.此时在M地某人观测太阳,太阳位于观测者的( )
A.东北方 B.东南方
C.西北方 D.正西方
2.如果Q点所在经线两侧日期不同,则此时( )
A.地球公转速度较快
B.北京时间为8时
C.东京地方时为6:00
D.新的一天所占经度范围小于全球的二分之一
3.图示季节,下列现象可能发生的是 ( )
A.江淮地区农民忙于抗旱 B.希腊雅典阴雨连绵
C.开普敦附近海域的船员常感闷热异常 D.巴西高原草木茂盛
19、C
参考译文:
孙泰是山阳人,年轻时师从皇甫颖,志行品德很有古代人的风度。孙泰的妻子是姨母的女儿。起初是姨母年纪老了,把两个女儿托付给孙泰,说:“长女一只眼睛有毛病,你可以娶她的妹妹。”姨母去世了,孙泰娶了姨母的长女为妻。有人问他的缘故,孙泰说:“那人眼睛有毛病,除了嫁给我就嫁不出去了。”众人都佩服孙泰的义气。孙泰曾经在都市遇见一座铁灯台,把它买了下来,叫人洗刷,原来是银制品。孙泰赶忙前往归还卖主。中和年间,孙泰将在义兴安家,购置一座别墅,用两百贯钱。已经交付了一半钱,孙泰就前往吴兴郡游览,约定回来后就到新买的别墅去。过了两个月,孙泰回来,停船步行,又把其余的款项交给房主,让那人搬迁到别处。在这个时候,看到一个老妇人连声痛哭。孙泰听了心里惊悸,叫她来问。老妇人说:“我曾经在这里侍奉过公婆,子孙不成材,使别墅被别人拥有,因此悲伤。”孙泰茫然自失了很久,就骗她说:“我刚好收到京师文书,已经另外授职,不能住在这里,所住的地方暂且由你的儿子掌管它。”说完,解开船绳就离去了,不再回来。
18、B
17、A(都:大)
翻译:再说,所谓文章,(是)一定要有益于社会罢了;所谓修辞,(就)好像器具上面的雕刻和绘画,如果(光是)花巧而且华丽,不一定适合使用;如果适合使用,也不一定花巧而且华丽。总之,以适合使用为根本,以雕刻绘画作为它的修饰罢了。不适合使用,不是制造器具的本意;不加以修饰,那结果也像这样吗?不是的。但修饰也不是可以不顾的,(只要)不(把它)放在首要地位就可以了。
15、主要观点:文章要以内容为第一,但也不能不顾形式。
本部分是高考考查的重点,考点主要集中在如下几个方面:①平衡状态的判断(即达到平衡状态的标志);②平衡移动的原因及平衡移动后结果(包括反应物转化率,各组分的含量及混合气体的平均相对分子质量等的变化)的分析;③平衡状态的比较;④化学平衡状态的计算。由于化学平衡移动与化学实验、工农业生产、环境保护、日常生活等有密切联系,预计这方面的结合会成为今后“3+X”理科综合命题的热点,以考查学生应用理论分析问题和解决问题的能力。
出现的题目类型有选择题和填空题。在选择题部分中多以考查化学平衡的基本概念和影响平衡移动的条件为主,对化学平衡计算的考查也时有出现。而在Ⅱ卷中,常出现高思维强度的题目,以考查学生的思维判断能力。例如等效平衡的比较判断,应用数学方法对化学平衡原理进行理论分析等。
解答该类题目时,在理解平衡状态的概念及其影响因素的基础上,应注意对它们的引申,不能局限于概念和规律的表面,同时要注意同一考点而不同出题形式的变化。
[例题](2001年全国,14)在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是
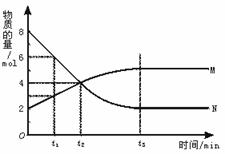
A.反应的化学方程式为:2M===N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
解析:改变外界条件对化学反应速率及化学平衡的影响,可用各种图象来表示,解答图象题目的方法思路是:
(1)看懂图象:一看面(即看清横坐标和纵坐标),二看线(即看线的走向、变化的趋势),三看点(即看线是否通过原点,两条线的交点及线的拐点),四看要不要作辅助线(如等温线、等压线),五看定量图象中有关量的多少。
(2)联想规律:即联想外界条件对化学反应速率和化学平衡的影响规律,且熟练准确。
(3)作出判断:依题意仔细分析作出正确判断。
分析本题图象可知,反应开始到时间t3时建立化学平衡。N的变化为8
mol-2 mol=6 mol;M的变化为:5
mol-2 mol=3 mol。因此反应方程式应为:2N M或M
M或M 2N。t2时,M和N的物质的量相等(反应在同一容器中进行,也可理解为浓度相等),但正、逆反应速率并不相等,因为从图中可以看出,反应并未达到平衡。t3时,已达到平衡。此时的正、逆反应速率相等。t1时,N和M的物质的量分别为6
mol 和3 mol,故N的浓度是M的2倍。
2N。t2时,M和N的物质的量相等(反应在同一容器中进行,也可理解为浓度相等),但正、逆反应速率并不相等,因为从图中可以看出,反应并未达到平衡。t3时,已达到平衡。此时的正、逆反应速率相等。t1时,N和M的物质的量分别为6
mol 和3 mol,故N的浓度是M的2倍。
答案:D
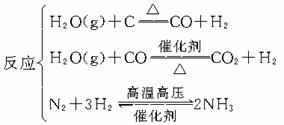
5.合成氨工业
(1)合成氨反应的特点及适宜条件
合成氨反应的特点:正反应是体积缩小的放热反应

(2)合成氨工业简介
原料:空气、燃料(煤、天然气、石油)、水
设备:氨合成塔
过程:原料气制备→净化→压缩→合成→分离
4.改变反应物的用量对转化率的影响
(1)若反应物只有一种,如aA(g) bB(g)+cC(g)增加A的量:①若a=b+c,xA不变;②若a>b+c,xA增大;③若a<b+c,xA减小。即a≠b+c时,增大或减小反应物浓度,平衡按加压或减压处理。
bB(g)+cC(g)增加A的量:①若a=b+c,xA不变;②若a>b+c,xA增大;③若a<b+c,xA减小。即a≠b+c时,增大或减小反应物浓度,平衡按加压或减压处理。
(2)若反应物不止一种,如mA(g)+nB(g) pC(g)+qD(g)
①若只增加A的量,平衡正向移动,xA减小,xB增大;②若按原比例同倍数增加A和B的量,平衡正向移动。当m+n=p+q时,xA、xB均不变;当m+n<p+q时,xA、xB均减小;当m+n>p+q时,xA、xB均增大。
pC(g)+qD(g)
①若只增加A的量,平衡正向移动,xA减小,xB增大;②若按原比例同倍数增加A和B的量,平衡正向移动。当m+n=p+q时,xA、xB均不变;当m+n<p+q时,xA、xB均减小;当m+n>p+q时,xA、xB均增大。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com