
2、不包括地球的天体系统是: A、太阳系 B、银河系 C、总星系 D、河外星系 3.下列地理现象中,由于地球自转而造成的现象是( )
A.昼夜的交替 B.昼夜长短的变化 C.春夏秋冬的更替 D.正午太阳高度的变化
1、下列关于天体的描述,正确的是:
A、星光闪烁的是行星 B、在星空有明显位移的是恒星
C、轮廓模糊的是星云 D、拖着长尾的是流星
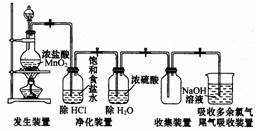
(六)吸收装置:Cl2有毒,多余的Cl2排放到空气中会造成环境污染,须用强碱溶液(如NaOH溶液)吸收。
[思考感悟]
在空气中及置的漂白粉是否还有漂白作用?
 在空气中及置的漂白粉会发生如下反应:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,
在空气中及置的漂白粉会发生如下反应:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,
2HClO 2HCl+O2↑,从而失去漂白作用。
[基础训练]
1、自来水厂常使用氯气消毒,市场上有些小商贩用自来水充当纯净水出售。下列试剂中可用来辨别纯净水真伪的是( D )
A、酚酞试液 B、氯化钡溶液 C、氢氧化钠溶液 D、硝酸银溶液
2、下列说法不正确的是( D )
①钠、氢气都能在氯气中燃烧生成白色烟雾;②铜丝在氯气中燃烧,生成蓝绿色的氯化铜;③液氯就是氯气的水溶液,它能使干燥的有色布条褪色;④久置的氯水,因氯气几乎完全挥发掉,剩下的就是水。
A、① B、①和② C、①和④ D、①②③④
3、下列关于氯水的叙述,不正确的是( A )
A、新制氯水中只含有Cl2和H2O分子
B、加入AgNO3溶液有白色沉淀产生
C、光照氯水有气泡逸出,久置的氯水,酸性增强
D、饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法
 [高考模拟]
[高考模拟]
4、(2006江苏理综16)实验室制Cl2的反应为4HCl(浓)+MnO2 MnCl2+C12↑+2H2O。下列说法错误的是( C )
A、还原剂是HCl,氧化剂是MnO2
B、每生成1 molCl2,转移电子的物质的量为2 mol
C、每消耗1 molMnO2,起还原剂作用的HCl消耗4mol
D、生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质
5、(2004上海化学6)下列物质中不会因见光而分解的是( A )
A、NaHCO3 B、HNO3 C、.AgI D、HClO
[作业]
(五)净化方法:用饱和食盐水除去HCl,再用浓H2SO4除去水蒸气。
(四)验满方法:将湿润的淀粉KI试纸放在集气瓶口,若试纸变蓝,证明已收集满。
(三)收集方法:向上排空气法或排饱和食盐水法。
(二)制备装置:固体+液体 气体。
(一)反应原理:(见课题15)。其中可以用KMnO4、K2Cr2O7、KClO3等氧化剂代替MnO2,如:
 2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O。
2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O。
(三)新制氯水、久置氯水、液氯的比较
|
名称 |
新制氯水 |
久置氯水 |
液氯 |
|
物质类别 |
混合物 |
混合物 |
纯净物 |
|
微粒种类 |
Cl2、HClO、H2O、 H+、Cl-、ClO-、OH- |
H2O、 H+、Cl-、OH- |
Cl2 |
|
主要性质 |
黄绿色溶液,能导电,有酸性、 漂白性 |
即为稀盐酸,无色溶 液,只有强酸性 |
黄绿色液体,不导 电,有Cl2的氧化性 |
|
存在条件 |
常温常压下避光可存在,不宜 久置 |
常温常压下可存在,不宜 久置 |
常温常压下不能存在 |
|
保存方法 |
棕色瓶盛装,并避光保存,瓶塞 必须用玻璃塞,不能用橡皮塞 |
密封可久置 |
低温密封 |
(二)性质:氯水的多种成分决定了它具有多重性质:Cl2的强氧化性;HCl的强酸性;HClO的强氧化性、弱酸性;Cl-的性质。在不同的反应中,氯水起作用的成分不同,现列表如下:
|
参与反应的微粒 |
所加试剂 |
实验现象 |
离子方程式或解释 |
|
Cl- |
AgNO3溶液 |
白色沉淀 |
Cl-+Ag+=AgCl↓ |
|
H+ |
Na2CO3固体 |
有气泡产生 |
2H++CO32-=CO2↑+H2O |
|
HClO |
有色布条 |
布条颜色褪去 |
发生氧化还原反应 |
|
Cl2 |
FeCl2溶液 |
溶液变棕黄色 |
2Fe2++Cl2=2Fe3++2Cl- |
|
Cl2、H2O |
SO2 |
黄绿色褪去 |
SO2+Cl2+2H2O=4H++2Cl-+SO42- |
|
HClO、H+ |
石蕊溶液 |
先变红后褪色 |
酸性和漂白性 |
|
Cl2、H+ |
镁粉 |
氯水的颜色褪去并 有气泡产生 |
Mg+2H+=Mg2++H2↑,H+被消耗,使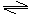 Cl2+H2O
HCl+HClO平衡右移, Cl2+H2O
HCl+HClO平衡右移,Cl2减少,颜色变浅直至褪色 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com