
10、 用0.10 mol·L-1的盐酸滴定0.10 mol·L-1的氨水,滴定过程中不可能出现的结果是
用0.10 mol·L-1的盐酸滴定0.10 mol·L-1的氨水,滴定过程中不可能出现的结果是
 A.c(NH4+)>c(Cl-),c(OH-)>c(H+)
A.c(NH4+)>c(Cl-),c(OH-)>c(H+)
 B.c(NH4+)=c(Cl-),c(OH-)=c(H+)
B.c(NH4+)=c(Cl-),c(OH-)=c(H+)
 C.c(Cl-)> c(NH4+), c(OH-)>c(H+)
C.c(Cl-)> c(NH4+), c(OH-)>c(H+)
 D.c(Cl-)> c(NH4+),c(H+)> c(OH-)
D.c(Cl-)> c(NH4+),c(H+)> c(OH-)
 答案.C
答案.C
 [解析]溶液中不可能出现阴离子均大于阳离子的情况,不遵循电荷守恒,故C项错。
[解析]溶液中不可能出现阴离子均大于阳离子的情况,不遵循电荷守恒,故C项错。
9、现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a,则碳的质量分数是
 A.
A.  B.
B. a C.
a C.  (1-a) D.
(1-a) D. (1-a)
(1-a)
 答案.C
答案.C
 [解析]乙酸的化学式为C2H4O2,而单烯烃的通式为CnH2n,从化学式可以发现两者中,C与H之间的数目比为1:2,质量比为6:1,碳氢的质量分数一共为1-a,其中碳占
[解析]乙酸的化学式为C2H4O2,而单烯烃的通式为CnH2n,从化学式可以发现两者中,C与H之间的数目比为1:2,质量比为6:1,碳氢的质量分数一共为1-a,其中碳占 。
。
8、 下列表示溶液中发生反应的化学方程式错误的是
下列表示溶液中发生反应的化学方程式错误的是
A.2Al+2NaOH+2H2O=2NaAlO2+3H2↑
B.KMnO4+HCOOK+KOH=2K2MnO4+CO2↑+H2O
C.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
D.K2Cr2O7+6FeSO4+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+K2SO4+7H2O
答案.B
[解析]在碱性条件下,可能产生CO2气体,而应是CO32 -,故B项错。
7、将15 mL 2 mol·L-1 Na2CO3溶液逐滴加入到40 mL 0.5 mol·L-1 MCln盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中n值是
A.4 B.3 C.2 D.1
答案.B
[解析]M的化合价为+n,Na2CO3与MCln反应对应的关系式为:2Mn+ ~ nCO32 -
2 n
15×10-3×2 40×10-3×0.5
可得n=3,故选B。
6、下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是
A.Ba2+、NO3-、NH4+、Cl-
B.Ca2+、HCO3-、NH4+、AlO2-
C.K+、Ba2+、Cl-、HSO3-
D.Mg2+、NH4+、SO42-、K+
答案.D
[解析]A项,加入NaOH会与NH4+ 产生NH3,但没有沉淀;B项HCO3- 与AlO2- 不能共存,会生成Al(OH)3 沉淀。C项,OH-与HSO3- 生成SO32 -,与Ba2+可生成BaSO3沉淀,但无气体。D项,OH-与NH4+ 产生NH3,与Mg2+会产生Mg(OH)2沉淀,正确。
15. 右图是某燃煤发电厂处理废气的装置示意图。装置内发生的主要反应中不含
右图是某燃煤发电厂处理废气的装置示意图。装置内发生的主要反应中不含

 A.化合反应 B.分解反应
A.化合反应 B.分解反应
 C.置换反应 D.氧化还原反应
C.置换反应 D.氧化还原反应
 答案C
答案C
 [解析]装置内没有单质出现,故不存在置换反应。化合反应为SO2+CaO=CaSO3,分解反应为:CaCO3=CaO + CO2 ,氧化还原反应为:2CaSO3 + O2 =2CaSO4 。
[解析]装置内没有单质出现,故不存在置换反应。化合反应为SO2+CaO=CaSO3,分解反应为:CaCO3=CaO + CO2 ,氧化还原反应为:2CaSO3 + O2 =2CaSO4 。
 [考点分析]考查燃煤中所发生的反应的类型判断。
[考点分析]考查燃煤中所发生的反应的类型判断。

14. 生活中难免会遇到一些突发事件,我们要善于利用学过的知识,采取科学、有效的方法保护自己。如果发生了氯气泄漏,以下自救方法得当的是
生活中难免会遇到一些突发事件,我们要善于利用学过的知识,采取科学、有效的方法保护自己。如果发生了氯气泄漏,以下自救方法得当的是
 A.只要在室内放一盆水
A.只要在室内放一盆水
 B.向地势低的地方撤离
B.向地势低的地方撤离
 C.观察风向,顺风撤离
C.观察风向,顺风撤离
 D.用湿毛巾或蘸有石碱水的毛巾捂住口鼻撤离
D.用湿毛巾或蘸有石碱水的毛巾捂住口鼻撤离
 答案.D
答案.D
 [解析]氯气与水反应,其速度慢且反应不充分,故A项错;氯气的密度大于空气,故应向地势高的地方、逆风跑,才可以在氯气之上,B、C项均错。D项,石碱水即为Ca(OH)2可以吸收氯气,正确。
[解析]氯气与水反应,其速度慢且反应不充分,故A项错;氯气的密度大于空气,故应向地势高的地方、逆风跑,才可以在氯气之上,B、C项均错。D项,石碱水即为Ca(OH)2可以吸收氯气,正确。
 [考点分析]考查氯气的物理、化学性质。
[考点分析]考查氯气的物理、化学性质。
13. 酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2C7酸性水溶液乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是
酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2C7酸性水溶液乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是
①乙醇沸点低 ②乙醇密度比水小
③乙醇有还原性 ④乙醇是烃的含氧化合物
A.②④ B.②③ C.①③ D.①④
答案C
[解析]乙醇沸点低,易挥发,故可以易被检测。K2Cr2C7具有强氧化性,可以氧化乙醇,自身生成Cr3+。
[考点分析]本题考查乙醇的性质。
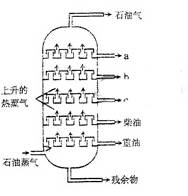
12.右图是石油分馏塔的示意图,a、b、c三种馏分中
A.a的沸点最高
B.b的熔点最低
C.c的平均分子量最大
D.每一种馏分都是纯净物
答案C
[解析]a、b、c三种馏分均为蒸气,故最上面的熔沸点最低,C的熔点最大,对应的平均相对分子量也最大。
[考点分析]考查物质熔沸点与相对分子质量间的关系。
11.茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池。在这种电池中
①铝合金是阳极 ②铝合金是负极
③海水是电解液 ④铝合金电极发生还原反应
A.②③ B.②④
C.①② D.①④
答案A
[解析]电池电极只称为正、负极,故①错。其中活泼的一极为负极,即为铝合金,②对。电极在海水中,故海水为电解质溶液,③对。④铝合金为负极,则发生氧化反应,故错。
 [考点分析]原电池的构成及电极反应的判断。
[考点分析]原电池的构成及电极反应的判断。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com