
| 编号 | KClO3质量(g) | 加入物质质量(g) | 待测数据 |
| 1 | 2.0 | CuO x | |
| 2 | 2.0 | MnO2 0.5 |
| 实验步骤 | 设计这一步骤的目的 |
| 实验表明,加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
| 将加热后残留的固体溶于足量的水,过滤后称重CuO的质量 | CuO的质量在反应前后是否保持不变 |
| 将过滤后的CuO重新与KClO3混合加热,观察是否依旧能加快KClO3的分解(或者利用CuO的常见化学性质如:将CuO加入稀硫酸中,观察无色溶液是否变成蓝色) | CuO的化学性质在反应前后是否保持不变 |
分析 (1)根据氢氧化铜受热时能分解成氧化铜和水分析;
(2)实验的目的是:证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较,上述实验中已有数据KClO3质量和其它物质质量,要比较催化效果就是看使用氧化铜与二氧化锰哪一种产生相同体积气体时所需时间短,或在相同时间内,哪一种物质产生的气体多.
(3)根据加入二氧化锰的质量分析回答;
(4)根据催化剂的特点分析验证的方法.
解答 解:(1)由题意可知,在步骤③中氢氧化铜受热时能分解成氧化铜和水,涉及到的化学方程式:Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O
(2)证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较,对比实验一定要控制变量,此实验中应控制氯酸钾质量、气体的体积、氧化铜与二氧化锰的质量相等,可变的量是生成等体积(50mL)气体所需用的时间.
(3)由于二氧化锰的质量为0.5g,为使本实验具有说服力,在本实验中CuO的质量应取x=0.5g.
(4)因为催化剂的特点是:能改变其它物质的化学反应速率,但它本身的质量和化学性质在反应前后不变,所以还应该做的实验如下表:
| 实验步骤 | 实验操作及现象 | 设计目的 |
| 1 | 实验表明,加入CuO后产生O2的速率比未加时快得多 | CuO能加快KClO3的分解 |
| 2 | 将加热后残留的固体溶于足量的水,过滤后称重CuO的质量 | CuO的质量在反应前后是否保持不变 |
| 3 | 将过滤后的CuO重新与KClO3混合加热,观察是否依旧能加快KClO3的分解(或者利用CuO的常见化学性质如:将CuO加入稀硫酸中,观察无色溶液是否变成蓝色) | CuO的化学性质在反应前后是否保持不变 |
| 实验步骤 | 设计这一步骤的目的 |
| 将过滤后的CuO重新与KClO3混合加热,观察是否依旧能加快KClO3的分解(或者利用CuO的常见化学性质如:将CuO加入稀硫酸中,观察无色溶液是否变成蓝色) | CuO的化学性质在反应前后是否保持不变 |
点评 本题属于实验探究题,同学需要根据题意并结合课本所学相关知识深入分析,这类题有些答案并不固定但必须合理.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 产品标准号: | GB5461-2000 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 质量等级 | 一级 |
| 碘含量 | 35±15mg/kg |
| 食用方法 | 待食品熟后加入碘盐 |
| 储藏方法 | 密封储存、防潮加热 |
| 分装日期 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合物都是由不同种元素组成的,不同元素组成的纯净物一定是化合物 | |
| B. | 碱中都有氢、氧元素,所以含氢、氧元素的化合物都是碱 | |
| C. | 中和反应有盐和水生成,生成盐和水的反应都属于中和反应 | |
| D. | 氧化物中一定含有氧元素,则另一种元素一定是金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 属于有机物的有③⑤⑨ | B. | 属于碱的有①④ | ||
| C. | 属于氧化物的有②⑧ | D. | 属于单质的有⑥⑦ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酒精的挥发;酒精的燃烧 | B. | 电解水;点燃氢气 | ||
| C. | 硝酸钾加热熔化;水结冰 | D. | 工业制氧气;实验室制氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
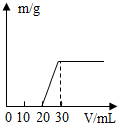 某澄清溶液由HNO3、Na2SO4、K2CO3、CuCl2 四种物质中的两种组成,向溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量(m)与加入Ba(OH)2溶液的体积(V)的关系如图所示.则该溶液所含的溶质是HNO3、CuCl2.(填化学式)
某澄清溶液由HNO3、Na2SO4、K2CO3、CuCl2 四种物质中的两种组成,向溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量(m)与加入Ba(OH)2溶液的体积(V)的关系如图所示.则该溶液所含的溶质是HNO3、CuCl2.(填化学式)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com