
����Ŀ����ͼ�Dz��ֶ�����Ԫ�صij������ϼ���ԭ�������Ĺ�ϵͼ��

��ش��������⣺
��1����ͼ��CԪ�ص�������Ϊ7����ԭ�ӷ���Ϊ_____��Ԫ��I��Gͬ����,λ�ڵ���������Ԫ��I��ԭ�ӽṹʾ��ͼ______��
��2��F��G��HԪ����̬�⻯����ȶ�����ǿ������˳��Ϊ_______________���û�ѧʽ��ʾ��
��3��������X��BԪ�ص��������������ʽΪ_________����ͼ��CԪ�ص�һ���⻯��Y��10������, Y��O2�����û���Ӧ�Ļ�ѧ����ʽΪ_________��
��4��H������������Ӧ��ˮ�����Ũ��Һ���ȶ������ȿɷֽ⣬����֮һ��H�ĵ��ʣ��ҵ���28mol����ת��ʱ���ָ������¹�����9mol���壬д���÷�Ӧ�Ļ�ѧ����ʽ__________��
��5��������Ԫ���еļ������a��b��c��d�����ʣ�ijͬѧ���ʵ������ͼװ��֤��Ԫ��B��C��F�ķǽ�����ǿ����������Һb����Һc��Ϊ��������
����Һa��b�ֱ�Ϊ_____��___���ѧʽ����
����Һc�е����ӷ���ʽΪ_________��
�����ԭ�ӽṹ�ĽǶȽ��ͷǽ�����C��B��ԭ��_________��
���𰸡�![]()
 HCl��H2S��SiH4
HCl��H2S��SiH4 ![]() 4NH3+3O2
4NH3+3O2![]() 2N2+6H2O 4HClO4�T2Cl2��+7O2��+2H2O HNO3 NaHCO3
2N2+6H2O 4HClO4�T2Cl2��+7O2��+2H2O HNO3 NaHCO3 ![]() +CO2+H2O=H2SiO3��+
+CO2+H2O=H2SiO3��+![]() ̼�͵���Ԫ��λ��ͬһ���ڣ����Ӳ�����ͬ������̼��ԭ��������ԭ�Ӱ뾶С��ԭ�Ӻ˶��������ӵ���������ǿ�����Ե���̼�ķǽ�����ǿ��
̼�͵���Ԫ��λ��ͬһ���ڣ����Ӳ�����ͬ������̼��ԭ��������ԭ�Ӱ뾶С��ԭ�Ӻ˶��������ӵ���������ǿ�����Ե���̼�ķǽ�����ǿ��
��������
��ͼ�л��ϼۿ�֪��D�Ļ��ϼ�ֻ��-2�ۣ�û�������ϼۣ���DΪOԪ�أ�A��+1��-1�ۣ���ԭ��������С��AΪHԪ�أ�B��ԭ������С��O ��B�Ļ��ϼ�Ϊ+4��-4�ۣ�BΪCԪ�أ�C��ԭ������С��O��C�Ļ��ϼ���+5��-3�ۣ���CΪNԪ�أ�E��ԭ����������O����E�Ļ��ϼ�Ϊ+1�ۣ����ڢ�A�壬��EΪNaԪ�أ�F��B�Ļ��ϼ���ͬ��F��Bλ��ͬ���壬F��ԭ����������FΪSi��G���������Ϊ+6�ۡ���ͼ�Ϊ-2��ӦΪSԪ�أ�H���������Ϊ+7��ԭ�����������HΪCl���Դ������
������������֪��AΪHԪ�أ�BΪCԪ�أ�CΪNԪ�أ�DΪOԪ�أ�EΪNaԪ�أ�FΪSiԪ�أ�GΪSԪ�أ�HΪClԪ�أ�
��1��CΪNԪ�أ��˵����Ϊ7��������Ϊ7��NԪ�ص�������Ϊ7����������Ϊ7+7=14����ԭ�ӷ���Ϊ![]() ��GΪSԪ�أ�λ�ڵ�������VIA�壬Ԫ��I��Gͬ���壬λ�ڵ������ڣ���IΪSeԪ�أ��˵����34������34�����ӣ�K��L��M��N�����������Ϊ2��8��18��6����ԭ�ӽṹʾ��ͼΪ
��GΪSԪ�أ�λ�ڵ�������VIA�壬Ԫ��I��Gͬ���壬λ�ڵ������ڣ���IΪSeԪ�أ��˵����34������34�����ӣ�K��L��M��N�����������Ϊ2��8��18��6����ԭ�ӽṹʾ��ͼΪ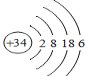 ����Ϊ
����Ϊ![]() ��
�� ��
��
��2��FΪSiԪ�أ�GΪSԪ�أ�HΪClԪ�أ�����ͬ����Ԫ�أ������ң�Ԫ�صķǽ�����������ǿ����ǽ�����Si��S��Cl���ǽ���Խǿ������̬�⻯��Խ�ȶ�������̬�⻯����ȶ�����ǿ������˳��ΪHCl��H2S��SiH4����ΪHCl��H2S��SiH4��
��3��BΪCԪ�أ�������X��BԪ�ص���������X��CO2��CO2��Cԭ����ÿ��Oԭ���γ����Թ��õ��Ӷԣ������ʽΪ![]() ��CΪNԪ�أ���һ���⻯��Y��10������ΪNH3��NH3��O2�����û���Ӧ�Ļ�ѧ����ʽΪ4NH3+3O2
��CΪNԪ�أ���һ���⻯��Y��10������ΪNH3��NH3��O2�����û���Ӧ�Ļ�ѧ����ʽΪ4NH3+3O2![]() 2N2+6H2O����Ϊ
2N2+6H2O����Ϊ![]() ��4NH3+3O2
��4NH3+3O2![]() 2N2+6H2O��
2N2+6H2O��
��4��HΪClԪ�أ�Cl������������Ӧ��ˮ�����Ũ��Һ���ȶ������ȿɷֽ⣬����֮һ���ȵĵ��ʣ��ҵ���28mol����ת��ʱ�����¹�����9mol���壬�ȵĵ���Ϊ������ClԪ����+7�۵õ��ӱ�Ϊ0�ۣ�����2mol����ʱ���ɵõ�28mol���ӣ����ɵ����غ��֪������7mol�������÷�ӦΪ4HClO4�T2Cl2��+7O2��+2H2O����Ϊ4HClO4�T2Cl2��+7O2��+2H2O��
��5��BΪCԪ�أ�CΪNԪ�أ�FΪSiԪ�أ�����ͼװ��֤��Ԫ��C��N��Si�ķǽ�����ǿ������ͼ��֪����ƿ�з���������̼��Ƶķ�Ӧ���ɶ�����̼����Һb�ɳ�ȥ������̼�лӷ������ᣬ�Լ�Ϊ����̼�����ƣ���ҺcΪ�����ƣ�������ǿ����ȡ����ķ�Ӧ��
����Һa��b�ֱ�ΪHNO3������NaHCO3����ΪHNO3��NaHCO3��
����Һc�е����ӷ���ʽΪ![]() +CO2+H2O=H2SiO3��+
+CO2+H2O=H2SiO3��+![]() ������SiO32-+CO2+H2O=H2SiO3��+
������SiO32-+CO2+H2O=H2SiO3��+![]() ��
��
�۴�ԭ�ӽṹ�ĽǶȽ��ͷǽ�����N��C��ԭ����Ϊ̼�͵���Ԫ��λ��ͬһ���ڣ����Ӳ�����ͬ������̼��ԭ��������ԭ�Ӱ뾶С��ԭ�Ӻ˶��������ӵ���������ǿ�����Ե���̼�ķǽ�����ǿ����Ϊ̼�͵���Ԫ��λ��ͬһ���ڣ����Ӳ�����ͬ������̼��ԭ��������ԭ�Ӱ뾶С��ԭ�Ӻ˶��������ӵ���������ǿ�����Ե���̼�ķǽ�����ǿ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
(1)28 g CO��ԭFe2O3���ɵ��������ų�8.3 kJ����____________________��
(2)1 mol������1 mol�Ȼ������廯�������Ȼ�粒��壬�ų�176 kJ����_________��
(3)N2��O2��������184 g NO2���壬����135.4 kJ����___________________________��
(4)1 g H2ȼ������Һ̬ˮ���ų�142.9 kJ����________________________��
(5)5.2 g��̬��Ȳ(C2H2)��ȫȼ������Һ̬ˮ����̬CO2���ų�260 kJ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����()
![]() ���ӻ����ﺬ���Ӽ���Ҳ���ܺ����Լ���Ǽ��Լ�
���ӻ����ﺬ���Ӽ���Ҳ���ܺ����Լ���Ǽ��Լ�
![]() ��������Դ���̼������ԣ����Էǽ�����
��������Դ���̼������ԣ����Էǽ�����![]()
![]() ������Ԫ�صĻ����ﲻһ�������ӻ�����
������Ԫ�صĻ����ﲻһ�������ӻ�����
![]() �ɷǽ���Ԫ����ɵĻ�����һ���ǹ��ۻ�����
�ɷǽ���Ԫ����ɵĻ�����һ���ǹ��ۻ�����
![]() ����״̬�ܵ���Ļ����������ӻ�����
����״̬�ܵ���Ļ����������ӻ�����
![]() �ɷ�����ɵ�������һ�����ڹ��ۼ�
�ɷ�����ɵ�������һ�����ڹ��ۼ�
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᾧ�����ɿɱ�ʾΪH2C2O4xH2O��ͨ������ʵ��ⶨxֵ���������£�
�ٳ�ȡ6.30 g���ᾧ�����100 mLˮ��Һ��
��ȡ25.00mL���������Һ������ƿ�У���������ϡ���ᣬ��0.5000molL-1KMnO4��Һ���еζ�������ζ��յ�ʱ������KMnO4��Һ10.02mL��
���ظ��ڲ���2�Σ�����KMnO4��Һ������ֱ�Ϊ11.02mL��9.98mL����֪��H2C2O4 ��MnO4- ��H+ �� CO2 ����Mn2+��H2O ������ʽδ��ƽ��
��1����������Ʋ�����Һʱ�����õIJ����������ձ�����������______;
��2���жϵ���ζ��յ��ʵ��������______;
��3������������ȷ������£����²�����ʹ�ⶨ��xֵƫС����______;
A �ζ���ˮϴ��δ��KMnO4��Һ��ϴ
B ��ƿ������ˮϴ��֮���ò�����Һ��ϴ
C ��ʼ�ζ�ʱ�ζ��ܼ��촦�����ݣ��ζ�����������ʧ
D �ζ��յ����ʱ�����ӵζ��ܵĿ̶�
��4����������ʵ�����ݼ���xֵ ______�� (д���������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��800��ʱ����2L�����ܱ�������Ͷ��0.20molNO��0.12mol O2�������з�Ӧ2NO(g)��O2(g) ![]() 2NO2(g)��n(NO)��ʱ��ı仯������±���
2NO2(g)��n(NO)��ʱ��ı仯������±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 |
n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.04 | 0.04 |
��1��800��ʱ���÷�Ӧƽ��ʱ��NO�����ʵ���Ũ��Ϊ______�������¶ȣ�NO��ƽ��Ũ��Ϊ0.03molL-1����÷�ӦΪ_______��Ӧ(��������������������)��
��2����O2��ʾ0��2s�ڸ÷�Ӧ��ƽ����Ӧ����v(O2)��______��
��3����˵���÷�Ӧһ���ﵽƽ��״̬����______��
a v(NO2)��2v(O2)���� b ������ѹǿ���ֲ���
c ������������ɫ���ֲ��� d �����������ܶȱ��ֲ���
��4�� ƽ������д�ʩ��ʹ�÷�Ӧ������Ӧ�����ƶ���������Ӧ�����������____��
a �ʵ������¶� b �ʵ������¶�
c ����O2��Ũ�� d ѡ���Ч����
��5��800��ʱ��������Ӧ��ƽ�ⳣ��K��______���������к�1.00 molL-1 NO��2.00 molL-1O2��2.00 molL-1 NO2�����ʱv��_______v�� (������������������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���ͬѧ��ʵ����������װ����ȡ��������������Ҫ�������£�
����30mL�Ĵ��Թ�A�а������2��3��2�ı�������Ũ���ᡢ�Ҵ�������Ļ����Һ��
�ڰ���ͼ���Ӻ�װ�ã�װ�����������ã�����С����ȵؼ���װ�л����Һ�Ĵ��Թ�5~10min��
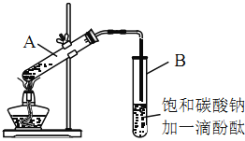
�۴��Թ�B�ռ���һ���������ֹͣ���ȣ������Թ�B��������Ȼ���ô��ֲ㡣
�ܷ�������������㡢ϴ�ӡ����
��֪�������ݣ�
���� | �۵㣨�棩 | �е㣨�棩 | �ܶȣ�g/cm3�� |
�Ҵ� | ��117.0 | 78.0 | 0.79 |
���� | 16.6 | 117.9 | 1.05 |
�������� | ��83.6 | 77.5 | 0.90 |
Ũ���ᣨ98%�� | �D�D | 338.0 | 1.84 |
��ش��������⣺
��1�����Ƹû����Һʱ���������������ʵ��Ⱥ�˳����___________��д����ȡ���������Ļ�ѧ����ʽ��___________��
��2����ʵ���У�Ũ�����������___________��
��3������ʵ���б���̼������Һ��������___________������ĸ����
A ���ղ����Ҵ�
B �����
C ���������������ܽ�ȣ������ڷֲ�����
D �����������ɣ���������
��4�����������ҪС����ȼ��Ȳ���������Ҫ������___________��
��5���������B�Թ��ڵ��ϲ�������___________�����������ƣ���
��6��������з�������õ�����Ҫ������___________����ѡ�õĸ����Ϊ___________������ĸ����
A ��ʯ�� B NaOH����
C ��ʯ�� D ��ˮNa2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������г���1 mol H2��1 mol Br2����һ���¶���ʹ�䷢����Ӧ��H2(g)��Br2(g)![]() 2HBr(g) ���ﵽ��ѧƽ��״̬��������²������й������������
2HBr(g) ���ﵽ��ѧƽ��״̬��������²������й������������
A. ���������ݻ����䣬�����м���1 mol H2������Ӧ��������ƽ�������ƶ�����H2��ת���ʱ�ԭƽ���
B. ���������ݻ����䣬�����м���1mol He�����ı�����ʵ�Ũ�ȣ���ѧ��Ӧ���ʲ��䣬ƽ�ⲻ�ƶ�
C. ��������������ѹǿ���䣬�����м���1 mol He����Ӧ��Ũ���½�����ѧ��Ӧ���ʼ�����ƽ�������ƶ�
D. ��������������ѹǿ���䣬�����м���1 mol H2��1 mol Br2��ƽ�������ƶ�����H2���յ�ת������ԭƽ��һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
������������־����־�����������й��ڰ�ͭ�ļ��أ���������ͭ(ͭ���Ͻ�)�������⣬����Ҫ������ң������������������Ʒ���ش��������⣺
(1)��Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ_________��3d�ܼ��ϵ�δ�ɶԵĵ�����Ϊ______��
(2)���������ڰ�ˮ�γ�[Ni(NH3)6]SO4��ɫ��Һ��
��SO42�������ӵ����幹����_____��
����[Ni(NH3)6]SO4��Ni2+��NH3֮���γɵĻ�ѧ����Ϊ______���ṩ�µ��ӶԵijɼ�ԭ����_____��
�۰��ķе�_____(��������������������)�(PH3)��ԭ����______������_____����(���������������Ǽ�����)������ԭ�ӵĹ���ӻ�����Ϊ_______��
(3)����ͭ����������______���γɵľ��壺Ԫ��ͭ�����ĵڶ������ֱܷ�Ϊ��ICu=1959kJ/mol��INi=1753kJ/mol��ICu>INi��ԭ����______��
(4)ij����ͭ�Ͻ�����������ṹ��ͼ��ʾ��
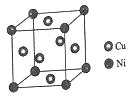
�پ�����ͭԭ������ԭ�ӵ�������Ϊ_____��
�����Ͻ���ܶ�Ϊdg/cm3����������a=________nm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ�����������в���ȷ���� (����)
A. ��״���£�22.4 L���ȼ���ķ�����ԼΪNA��
B. ���³�ѹ�£�7.0 g��ϩ���ϩ�Ļ�����к�����ԭ�ӵ���ĿΪNA
C. ���³�ѹ�£�92 g NO2��N2O4�Ļ�������к��е�ԭ������Ϊ6NA
D. ʢ��SO2���ܱ������к���NA����ԭ�ӣ���SO2�����ʵ���Ϊ0.5 mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com