
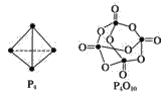
【题目】白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—PakJ·mol-1、P—ObkJ·mol-1、P=OckJ·mol-1、O=OdkJ·mol-1。根据图示的分子结构和有关数据计算该反应的反应热______。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】铁是应用泛的金属之一,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)某课题小组采用离子交换和滴定的方法来测定铁的某氯化物![]() 的化学式。实验中称取0.54g的
的化学式。实验中称取0.54g的![]() 样品,溶解后先进行阳离子交换预处理,再通过含有饱和
样品,溶解后先进行阳离子交换预处理,再通过含有饱和![]() 的阴离子交换柱,使
的阴离子交换柱,使![]() 和
和![]() 发生交换。交换完成后,流出溶液的
发生交换。交换完成后,流出溶液的![]() 用
用![]() 的盐酸滴定,滴定至终点时消耗盐酸25.00mL。通过计算求出
的盐酸滴定,滴定至终点时消耗盐酸25.00mL。通过计算求出![]() 中x的值为_________(取整数)。
中x的值为_________(取整数)。
(2)在实验室中,FeCl2可用铁粉和_________反应制备,FeCl3可用铁粉和_________反应制备。现有一瓶FeCl2溶液,某同学欲检验该溶液是否已经变质,首先取适量溶液于洁净的试管中,然后向溶液中滴加几滴______________,观察溶液是否变成红色即可得出结论。
(3)FeCl3与氢碘酸混合时有棕色物质生成,写出该反应的离子方程式:________;工业上还可以用FeCl3溶液来腐蚀印刷电路板上的铜,向反应所得的溶液中加入一定量的锌粉充分反应后,从理论上分析,下列说法合理的是____________。(填序号)。
A.若无固体剩余,则溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 四种离子
四种离子
B.若溶液中有![]() ,则体系中一定没有固体剩余
,则体系中一定没有固体剩余
C.若有固体剩余,则溶液中一定有反应![]() 发生
发生
D.当溶液中有![]() 存在时,则一定没有
存在时,则一定没有![]() 析出
析出
(4)高铁酸钾(![]() )是一种强氧化剂,可作为水处理剂和高容量电池的电极材料。在
)是一种强氧化剂,可作为水处理剂和高容量电池的电极材料。在![]() 中铁元素的化合价为_________,
中铁元素的化合价为_________,![]() 与
与![]() 在强碱性条件下反应可制取
在强碱性条件下反应可制取![]() ,其反应的离子方程式为________。
,其反应的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0.1mol·L-1的CH3COOH溶液中,c(H+)=1.0×10-3mol·L-1(忽略水的电离)。
(1)该温度下CH3COOH的电离度__。
(2)CH3COOH的电离平衡常数__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯是重要的基础化工原料,下图是大学化学教材《有机化学基础》上由甲苯合成J的一种合成路线。
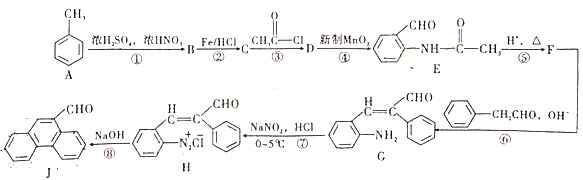
请依据上述流程回答以下问题
(1)B的化学名称为___________,J的分子式为___________。
(2)D生成E的反应类型为___________。
(3)设计第③步和第⑤步的目的是______________。
(4)由H生成J过程中生成的无机物除了![]() 外还有_________。
外还有_________。
(5)写出C→D的反应方程式为_______。
(6)D的同分异构体有多种。其中含有苯环和碳氧双键,且核磁共振氢谱有四组峰的有_________种。(不考虑立体异构)
(7)请依据流程图中相关信息,写出由甲苯和乙醛制备![]() 的合成路线________。(无机试剂任选)
的合成路线________。(无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学反应方程式:
反应Ⅰ:N2H4(g)![]() N2(g)+2H2(g) ΔH1
N2(g)+2H2(g) ΔH1
反应Ⅱ:N2(g)+3H2(g)![]() 2NH3(g) ΔH2
2NH3(g) ΔH2
(1)ΔH1__ΔH2(填“<”、“>”或“=”)。
(2)7N2H4(g)![]() 8NH3(g)+3N2(g)+2H2(g) ΔH=__(用ΔH1、ΔH2表示)。
8NH3(g)+3N2(g)+2H2(g) ΔH=__(用ΔH1、ΔH2表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.0mol SO2气体和2.0mol SO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)![]() 2SO3(g),达到平衡时SO3为n mol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是( )
2SO3(g),达到平衡时SO3为n mol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是( )
A. 1.6 mol SO2+0.3 mol O2+0.4 mol SO3
B. 4.0 mol SO2+1.0 mol O2
C. 2.0 mol SO2+1.0 mol O2+2.0 mol SO3
D. 2.0 mol SO2+0.5 mol O2+1.0 mol SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应可能是自发进行的吸热反应的是( )
A.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
B.(NH4)2CO3(s)=NH4HCO3(g)+NH3(g)
C.2CO(g)+O2(g)![]() 2CO2(g)
2CO2(g)
D.2Al+Fe2O3![]() Al2O3+2Fe
Al2O3+2Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在国际环境问题中,一次性使用的聚苯乙烯材料的“白色污染”甚为突出,这种材料难以分解,处理麻烦。最近研制出了一种新型的材料![]() 能替代聚苯乙烯。它是由乳酸缩聚而成的,该材料可在乳酸菌作用下发生降解。下列关于聚乳酸说法正确的是
能替代聚苯乙烯。它是由乳酸缩聚而成的,该材料可在乳酸菌作用下发生降解。下列关于聚乳酸说法正确的是
A.聚乳酸是一种纯净物
B.其聚合方式与聚苯乙烯相似
C.其单体为![]()
D.聚乳酸是一种线性高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下进行的下列实验,不能达到预期目的的是( )
序号 | 实验内容 | 实验目的 |
A | 测定NaClO溶液、CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
B | 向Mg(OH)2浊液中滴加少量0.1mol/LFeCl3溶液 | 比较Mg(OH)2和Fe(OH)3的溶解度 |
C | 将两个完全相同且充满NO2的密闭烧瓶,分别浸泡于热水、冰水中 | 探究温度对该化学平衡状态的影响 |
D | 向两只同体积同浓度的K2Cr2O7溶液中,分别加入1mL同浓度的H2SO4、NaOH溶液 | 探究浓度对该化学平衡状态的影响 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com