
【题目】镁是一种银白色的碱土金属,镁元素在地壳中的含量约为2.00%,位居第八位,镁及其化合物在研究和生产中具有广泛用途。请回答下列问题:
(1)氮化镁(Mg3N2)是由氮和镁所组成的无机化合物。在室温下纯净的氮化镁为黄绿色的粉末,能与水反应,常用作触媒,实验室欲用如图1所示装置和药品制备少量氮化镁。

①A中盛装的是浓氨水,B中可盛装___,二者混合可制取氨气。
②按照气流的方向从左至右连接装置:a接___、___接___、___接___。
③已知氨气有还原性,能还原氧化铜,生成物之一是空气的主要成分,该反应的化学方程式为____________________。
④如果没有装有无水氯化钙的装置,可能发生反应的化学方程式为____________________。
(2)碳酸镁可用作耐火材料、锅炉和管道的保温材料,以及食品、药品、化妆品、橡胶、墨水等的添加剂。合成碳酸镁晶须的步骤如下:
步骤1:配制0.5 mol·L-1 MgSO4溶液和0.5 mol·L-1 NH4HCO3溶液。
步骤2:用量筒量取500 mL NH4HCO3溶液于1 000 mL四口烧瓶中,开启搅拌器,温度控制在50 ℃。
步骤3:将250 mL MgSO4溶液逐滴加入NH4HCO3溶液中,1 min内滴加完毕,然后用氨水调节溶液pH到9.5。
步骤4:放置1 h后,过滤,洗涤。
步骤5:在40 ℃的真空干燥箱中干燥10 h,得到碳酸镁晶须产品(MgCO3·nH2O,n=1~5)。
①配制0.5 mol·L-1 MgSO4溶液500 mL,需要的仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、_____。
②步骤3中加氨水后反应的离子方程式为______________。
测定合成的MgCO3·nH2O中的n值。
称量1.000 g碳酸镁晶须,放入图2所示的广口瓶中,加入适量水,滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5 h,后期将温度升到30 ℃,最后烧杯中的溶液用已知浓度的盐酸滴定,测得生成CO2的总量;重复上述操作2次。
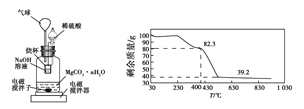
③图中气球的作用是__________________。
④上述反应后期要升温到30 ℃,主要目的是________________。
⑤若实验测得1.000 g碳酸镁晶须产生CO2的平均物质的量为a mol,则n为___(用含a的表达式表示)。
⑥称取100 g上述晶须产品进行热重分析,得到的热重曲线如图所示,则合成的晶须中n=______。
【答案】生石灰或氢氧化钠 d e c b f 2NH3+3CuO ![]() N2+3H2O+3Cu Mg3N2+6H2O
N2+3H2O+3Cu Mg3N2+6H2O![]() 3Mg(OH)2+2NH3↑ 500 mL容量瓶 Mg2++HCO3-HCO3-+NH3·H2O+(n-1)H2O
3Mg(OH)2+2NH3↑ 500 mL容量瓶 Mg2++HCO3-HCO3-+NH3·H2O+(n-1)H2O![]() MgCO3·nH2O↓+NH4+ 暂时储存CO2,有利于CO2被NaOH溶液吸收,且能保持装置中压强相对稳定 升高温度气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全
MgCO3·nH2O↓+NH4+ 暂时储存CO2,有利于CO2被NaOH溶液吸收,且能保持装置中压强相对稳定 升高温度气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全 ![]() 1
1
【解析】
(1)①浓氨水和生石灰或氢氧化钠固体混合放热,使一水合氨分解生成氨气,故答案为:
②根据实验目的及题给装置可知,按照气流的方向从左向右连接装置的顺序为:a接d,e接c,b接f,故答案为:
③氨气有还原性,能还原氧化铜,生成物之一是空气的主要成分氮气,则氨气与氧化铜反应的化学方程式为:2NH3+3CuO![]() N2+3H2O+3Cu,故答案为:d;e;c;b;f;
N2+3H2O+3Cu,故答案为:d;e;c;b;f;
④氮化镁能和水发生反应生成氢氧化镁和氨气,化学方程式为:Mg3N2+6H2O=3Mg(OH)2
+2NH3↑,故答案为:Mg3N2+6H2O=3Mg(OH)2+2NH3↑;
(2)①配制0.5 mol·L-1 MgSO4溶液500 mL,除提供的仪器外,还需要的仪器为500 mL容量瓶,故答案为:500 mL容量瓶;
②步骤3中加氨水后反应生成碳酸镁结晶水合物,反应的离子方程式为Mg2++HCO3—+NH3·H2O+(n-1)H2O=MgCO3·nH2O↓+NH4+,故答案为:Mg2++HCO3—+NH3·H2O+(n-1)H2O=
MgCO3·nH2O↓+NH4+;
③题图2装置中气球可以暂时储存CO2,有利于CO2被NaOH溶液吸收,且能保持装置中压强相对稳定,故答案为:暂时储存CO2,有利于CO2被NaOH溶液吸收,且能保持装置中压强相对稳定;
④题述反应后期将温度升到30 ℃,是为了使生成的二氧化碳全部逸出,便于其被氢氧化钠溶液完全吸收,从而减小测定产生的误差,故答案为:升高温度气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全;
⑤若实验测得1.000 g碳酸镁晶须产生的CO2的平均物质的量为a mol,依据碳元素守恒可知,晶须中碳酸镁的物质的量为a mol,根据MgCO3·nH2O中碳酸镁和结晶水的物质的量之比为1∶n,得到1∶n=a∶![]()
![]() ,得到n=
,得到n=![]()
![]() ,故答案为:
,故答案为:![]() ;
;
⑥由题图3知400 ℃时剩余质量为82.3 g,这是该晶须失去结晶水后的质量,则有100×![]()
![]() =100-82.3,解得n=1,故答案:1。
=100-82.3,解得n=1,故答案:1。


科目:高中化学 来源: 题型:
【题目】铜、硼、硅、砷等元素的化合物是制造新型激光武器和新型太阳能电池的重要材料。回答下列问题:
(1)基态硅原子电子占据的最高能层符号是_____,其中能量最高的电子所占据能级的原子轨道有_____个伸展方向,原子轨道呈_____形。
(2)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有____________。
(3)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的第一电离能从大到小的顺序为________(用元素符号表示)。H2SeO3的酸性_______H2SeO4(填“强于”或“弱于”),原因是___________(从分子结构的角度回答)。
(4)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。它的晶体结构如下左图所示。六方相氮化硼______π键(填“含有”或“不含”),其质地软的原因是_________。NaBH4是一种重要的储氢载体,阴离子的的立体结构为_______。
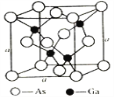
(5)砷化镓是优良的第三代半导体材料。如上图所示为GaAs的晶胞结构。
①与GaAs互为等电子体的一种原子晶体的化学式为________。
②已知晶胞的密度是ρ g·cm3,阿伏加德罗常数值为NA,棱长a=_____pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】城市地下潮湿的土壤中常埋有纵横交错的管道和输电线路,当有电流泄漏并与金属管道形成回路时,就会引起金属管道的腐蚀。原理如图所示,但若电压等条件适宜,钢铁管道也可能减缓腐蚀,此现象被称为“阳极保护”。下列有关说法不正确的是

A. 该装置能够将电能转化为化学能
B. 管道右端腐蚀比左端快,右端电极反应式为Fe-2e-![]() Fe2+
Fe2+
C. 如果没有外加电源,潮湿的土壤中的钢铁管道比较容易发生吸氧腐蚀
D. 钢铁“阳极保护”的实质是在阳极金属表面形成一层耐腐蚀的钝化膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能够鉴定氯乙烷中氯元素的存在的操作是 ( )
A.在氯乙烷中直接加入AgNO3溶液
B.加蒸馏水,充分搅拌后,加入AgNO3溶液
C.加入NaOH溶液,加热后加入稀硝酸酸化,然后加入AgNO3溶液
D.加入NaOH的乙醇溶液,加热后加入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在相应的条件下可能大量共存的是( )
A. 能使pH试纸变红的溶液中:CO![]() 、K+、Cl-、Na+
、K+、Cl-、Na+
B. 由水电离产生的c(OH-)=1×10-10mol·L-1的溶液中:NO![]() 、Mg2+、Na+、SO
、Mg2+、Na+、SO![]()
C. 在![]() =1×1012的溶液中:NH
=1×1012的溶液中:NH![]() 、Fe2+、Cl-、NO
、Fe2+、Cl-、NO![]()
D. ![]() =10-14mol·L-1的溶液中:Na+、HCO
=10-14mol·L-1的溶液中:Na+、HCO![]() 、Cl-、K+
、Cl-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的说法,正确的是( )
A.构成单质的分子中一定含有共价键
B.由非金属元素组成的化合物可能是离子化合物
C.非极性键只存在单质分子里
D.不同元素组成的多原子分子里的化学键一定是极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置电解硫酸钾溶液制取氢气,氧气,硫酸和氢氧化钾。从开始通电时,收集B和C逸出的气体。1 min后测得B口的气体体积为C口处的一半,下列说法不正确的是
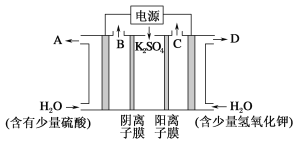
A. 电源左侧为正极
B. 电解槽左侧的电极反应方程式为2H2O-4e-==O2↑+4H+
C. D口导出的溶液为KOH溶液,且浓度比刚加入电解槽右侧时的浓度大
D. 标准状况下,若1 min后从C口处收集到的气体比B口处收集到的气体多2.24 L,则有0.1NA个SO42-通过阴离子膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com